
科目: 来源: 题型:
【题目】氮化碳结构如下图所示,其硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不正确的是 ( )
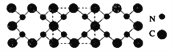
A. 氮化碳属于原子晶体
B. 氮化碳中碳显-4价,氮显+3价
C. 氮化碳的化学式为C3N4
D. 每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连
查看答案和解析>>
科目: 来源: 题型:
【题目】向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol·L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。下列判断正确的是( )

A. 原NaOH溶液的浓度为0.2 mol·L-1
B. 通入CO2在标准状况下的体积为448 mL
C. 所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3
D. 所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3)=1∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】溶液的配制过程能引起浓度偏高的是( )
A.用1g98%的浓硫酸加4g水配成19.6%的硫酸
B.配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,发现液面低于刻度
C.在80mL水中加入18.4mol/L的硫酸20mL,配制3.68mol/L的硫酸溶液
D.质量分数为5a%和a%的两种氨水等体积混合配成3a%的氨水
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
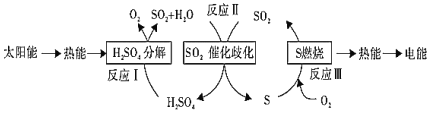
(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)![]() SO2(g) ΔH3=-297 kJ·mol-1
SO2(g) ΔH3=-297 kJ·mol-1
写出反应Ⅱ的热化学方程式:_____________________。
(2)歧化反应可简单理解为化学反应中同一反应物中某元素化合价同时出现升降。已知I-离子可以作为水溶液中SO2歧化反应的催化剂。有关离子方程式如下(未配平):
a.SO2+I-+H+→S↓+I2+H2O
b.I2+H2O+SO2→SO42-+H++I-
i.依据图示及以上离子方程式a、b,写出SO2歧化反应方程式:______________。
ii.探究a、b反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
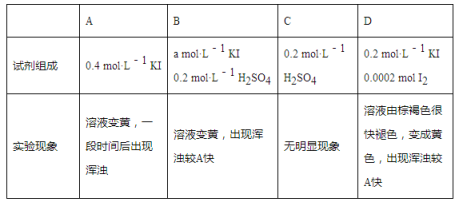
①B是A的对比实验,则a=__________。
②比较A、B、C,可得出的结论是______________________。
③实验表明,SO2的歧化反应速率D>A,结合①、②反应速率解释原因:________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】《我不是药神》中的“格列宁”是一种抗癌药。同样是抗癌药物"6-Azulenol”的结构简式如图所示,下列有关叙述错误的是 ( )
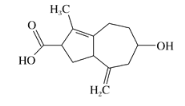
A.分子式为C13H18O3
B.能发生加成、氧化、酯化反应
C.能使溴水、酸性高锰酸钾溶液褪色
D.1mol该物质与足量的Na反应可产生11.2LH2(已换算成标准状况)
查看答案和解析>>
科目: 来源: 题型:
【题目】设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流是21世纪最富有挑战性的课题之一。最近有人设计了一种固体燃料电池,固体氧化铝——氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如右图所示,其中多孔电极a、b均不参与电极反应。下列判断不正确的是
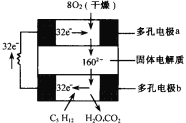
A.有O2放电的a极为电池的负极
B.b极对应的电极反应式为:C5H12+16O2--32e-=5CO2+6H2O
C.该电池的总反应方程式为:C5H12+8O2=5CO2+6H2O
D.汽油燃料电池最大的技术障碍是氧化反应不完全,产生炭粒堵塞电极的气体通道,从而使输电效能减弱
查看答案和解析>>
科目: 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
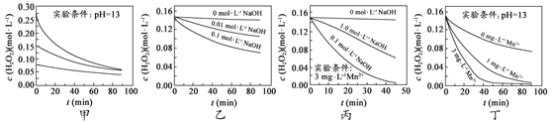
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目: 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:

A. 温度T下,该反应的平衡常数K=![]()
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,11.2LSO3中含有的分子数为0.5NA
B.常温常压下,46gNO2和N2O4的混合气体中含有原子总数为3NA
C.5.4g铝单质与足量NaOH溶液反应,转移电子数为0.3NA
D.常温下,1mol/L的MgCl2溶液中含Cl-数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com