
科目: 来源: 题型:
【题目】下列有关物质结构和性质的表述正确的是( )
A. 某微粒的结构示意图为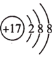 ,该元素位于周期表第三周期零族
,该元素位于周期表第三周期零族
B. 工业上用![]() 的反应来制备钾,是因为钠比钾更活泼
的反应来制备钾,是因为钠比钾更活泼
C. ![]() 的沸点高于
的沸点高于![]() 的沸点,原因与
的沸点,原因与![]() 分子间存在氢键有关
分子间存在氢键有关
D. 糖类物质溶液中,蛋白质溶液中加硫酸铵都会产生盐析现象
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式或离子方程式中,正确的是()
A.0.01mol·L﹣1NH4Al(SO4)2溶液与0.02mol·L﹣1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42﹣+2Ba2++4OH﹣=2BaSO4↓+Al(OH)3↓+NH3·H2O
B.一定条件下,将0.5molN2(g)和1.5molH2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g)△H=﹣38.6kJ·mol﹣1
2NH3(g)△H=﹣38.6kJ·mol﹣1
C.2H2(g)+O2(g)=2H2O(g)△H=﹣571.6kJ·mol﹣1,则H2的燃烧热为571.6kJ·mol﹣1
D.CO(g)的燃烧热是283.0kJ·mol﹣1,则CO2分解的热化学方程式为:2CO2(g)=2CO(g)+O2(g)△H=+283.0kJ·mol﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于实验原理或操作方法的叙述中,正确的是( )
A. 实验室用乙酸,乙醇和浓硫酸制乙酸乙酯时,必须将温度控制在170℃
B. 向滴有酚酞的![]() 溶液中逐滴加
溶液中逐滴加![]() 溶液,红色褪去,说明
溶液,红色褪去,说明![]() 在水溶液中存在水解平衡
在水溶液中存在水解平衡
C. 实验室金属钠应保存在煤油中,也可保存在无水酒精中
D. 可以用澄清石灰水鉴别失去标签的![]() 溶液和
溶液和![]() 溶液
溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是
A.1molMgCl2中含有的离子数为2NA
B.标准状况下,11.2LH2O中含有的原子数为1.5NA
C.标准状况下,22.4L氦气与22.4L氯气所含原子数均为2NA
D.常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在溶液中可发生以下反应:①16H++10Z-+2![]() ===2X2++5Z2+8H2O,②2M2++R2===2M3++2R-,③2R-+Z2===R2+2Z-,由此判断下列说法错误的是( )
===2X2++5Z2+8H2O,②2M2++R2===2M3++2R-,③2R-+Z2===R2+2Z-,由此判断下列说法错误的是( )
A.氧化性强弱顺序为:![]() <Z2<R2<M3+
<Z2<R2<M3+
B.还原性强弱顺序为:X2+<Z-<R-<M2+
C.Z元素在反应①中被氧化,在③中被还原
D.常温下可发生反应2M2++Z2===2M3++2Z-
查看答案和解析>>
科目: 来源: 题型:
【题目】下列条件下,两瓶气体所含原子数一定相等的是( )
A.同质量、同体积的N2和COB.同温度、同体积的H2和N2
C.同体积、同密度的C2H4和C3H4D.同压强、同体积的N2O和CO2
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯无水![]() 是电解法制镁的关键原料,有化工人员开发了以菱镁矿(主要成分是
是电解法制镁的关键原料,有化工人员开发了以菱镁矿(主要成分是![]() ,含少量
,含少量![]() 杂质)为原料,以乙二醇为溶剂,采用氨络合法制备
杂质)为原料,以乙二醇为溶剂,采用氨络合法制备![]() (白色块状固体或粉末,溶于水,易潮解),再转化为无水
(白色块状固体或粉末,溶于水,易潮解),再转化为无水![]() 的新工艺,其流程图如图:
的新工艺,其流程图如图:
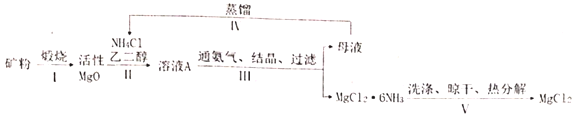
已知:①常压下,![]() 的初始分解温度为399℃,
的初始分解温度为399℃,![]() 的初始分解温度为896℃;
的初始分解温度为896℃;
②煅烧温度是影响MgO活性的关键因素;
③乙二醇的沸点197.3℃。
(1)步骤Ⅰ中工业上一般不选择800℃以上来完成这一步原因是_____。
(2)步骤Ⅱ中反应方程式为_____。
(3)步骤IV中蒸馏的目的是____。
(4)步骤V中的洗涤是为了除去晶体表面的杂质,最好选用下列哪种作为洗涤剂____。
A.氯化铵饱和溶液 B.乙二醇
C.冷水 D.氨气饱和的乙醇溶液
(5)实验过程需要测定![]() 浓度,可通过EDTA滴定(与
浓度,可通过EDTA滴定(与![]() 以1:1反应)来进行测定,若分下列步骤(未按顺序排列),为获得更可靠的实验结果,完整的操作顺序是c→___→e(用操作步骤前的字母表示)。
以1:1反应)来进行测定,若分下列步骤(未按顺序排列),为获得更可靠的实验结果,完整的操作顺序是c→___→e(用操作步骤前的字母表示)。
a.移取25.00mL待测溶液于锥形瓶中,加入10mL水,摇匀
b.用0.1000mol/L的EDTA标准溶液滴定至终点,记录消耗标准液的体积
c.称取一定质量的样品,配制250mL待测溶液
d.滴加1-2滴指示剂
e.舍弃不可靠数据、取平均值等
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
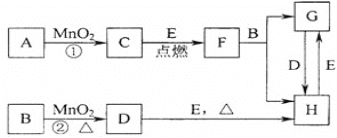
(1)写出有关物质的名称或化学式:F______,H_____。
(2)若反应①是在加热条件下进行,则A是___;若反应①是在常温条件下进行,则A是___。
(3)写出B与MnO2共热获得D的化学方程式______。
(4)写出D与E共热获得H的化学方程式________。
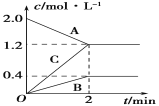
(5)如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:2min内,A物质的平均反应速率为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)把7.8g镁铝合金的粉末放入过量的盐酸中,得到8.96 LH2(标准状况下)。该合金溶于足量NaOH溶液,产生H2的体积(标准状况下)为____________ 。
(2)相同条件下,某Cl2与O2混合气体75mL恰好与100mL H2化合生成HCl和H2O,则混合气体的平均相对分子质量为____________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是2:5,则A的摩尔质量为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)④、⑥的元素符号分别是_____、______
(2)⑨元素氢化物的电子式是________
(3)⑧元素的原子结构示意图是__________
(4)元素①-⑨中原子半径最大的是_____;
(6)在盛有水的小烧杯中加入元素⑤的单质,发生反应的离子方程式为______;向上述反应后的溶液中加入元素⑥的单质,发生反应的化学方程式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com