
科目: 来源: 题型:
【题目】下列物质的转化在给定条件下不能实现的是
A. NH3![]() NO
NO![]() HNO3
HNO3
B. 浓盐酸![]() Cl2
Cl2![]() 漂白粉
漂白粉
C. Al2O3![]() AlCl3(aq)
AlCl3(aq)![]() 无水AlCl3
无水AlCl3
D. 葡萄糖![]() C2H5OH
C2H5OH![]() CH3CHO
CH3CHO
查看答案和解析>>
科目: 来源: 题型:
【题目】把500 mL有BaCl2和KCl的混合溶液分成2等份,一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
A.0.1(b-2a)mol/LB.0.4( 2a-b)mol/L
C.10(b-2a)mol/LD.4(b-2a)mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA 表示阿伏加德罗常数的值,下列说法正确的是
A.100 mL 0.1 mol·L-1的稀硫酸中含有SO42-个数为0.1NA
B.含1 mol HCl的盐酸与足量Fe反应,Fe所失去的电子总数为2 NA
C.4℃ 时,5.4 mL水中所含的水分子数是0.3 NA
D.标准状况下,22.4L氢气所含的质子数为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】KCl样品中含有少量KOH、K2SO4和不溶于水的杂质,为了提纯KCl,某同学先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作
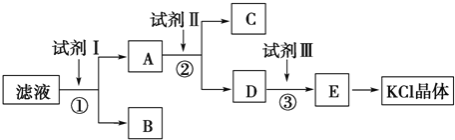
(1)试剂Ⅰ的化学式为__________,其作用是除去__________(填离子符号),
检验该离子完全除尽的操作是__________________________________________
(2)加入试剂Ⅱ时发生反应的化学方程式为_____________________________
(3)试剂Ⅲ的名称是__________,各步操作中所加试剂都必须过量,欲检验试剂Ⅲ已经过量,可以选用__________(填字母).
A.AgNO3 B.pH试纸 C.K2CO3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W是元素周期表中的短周期元素,它们的相对位置如下表所示,其中X、Y 元素均能形成10电子的氢化物,Z的原子序数是Y的2倍。请回答下列问题:
X | Y | |
Z | W |
(1)W的简单离子的结构示意图为______,Y元素在周期表中的位置是____。
(2)写出实验室制W元素单质的离子方程式:___________
(3)关于W同主族元素,下列说法正确的是:__________
A.从上到下密度逐渐增大
B.从上到下熔点和沸点都逐渐升高
C.从上到下元素的非金属性越来越强
D.同主族元素对应的单质中,只有W元素对应的单质在常态下为气态
(4)W与Z形成的液体化合物Z2W2,该物质可与水反应生成ZO2气体,1 mol Z2W2参加反应时转移1.5 mol电子,其中只有一种元素化合价发生改变,Z2W2与水反应的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组制备氢氧化亚铁沉淀。
实验1 |
| 实验现象 |
液面上方产生白色絮状沉淀,迅速变为灰绿色,振荡,试管壁上有红褐色沉淀生成。 |
(1)实验1中产生白色沉淀的离子方程式是_______。
(2)为了探究沉淀变灰绿色的原因,该小组同学展开如下探究:
①甲同学推测灰绿色物质为Fe(OH)2和Fe(OH)3混合物。查阅资料后根据调色原理认为白色和红褐色的调和色不可能是灰绿色,并设计实验证实灰绿色物质中不含有Fe(OH)3,方案是______。
②乙同学查阅文献:Fe(OH)2在大量SO42-存在的情况下形成Fe6(SO4)2(OH)4O3(一种灰绿色氧基碱式复盐)。并设计对比实验证实该假设:向试管中加入________,再往试管中加入_________,振荡,现象与实验1相同,结论是该假设不成立。
③乙同学继续查阅文献:Fe(OH)2沉淀具有较强的吸附性能,灰绿色可能是由Fe(OH)2表面吸附Fe2+引起。推测所用的硫酸亚铁溶液的浓度应越小越好;氢氧化钠溶液浓度应越大越好。设计了如下实验方案:
试管中10mLNaOH溶液 | 滴加FeSO4溶液 | 实验现象 | |
实验2 | 6 mol/LNaOH溶液 | 0.2mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有少量灰绿色),沉淀下沉后,大部分灰绿色变为白色沉淀 |
实验3 | 6 mol/LNaOH溶液 | 0.1mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有极少量灰绿色),沉淀下沉后,底部都为白色沉淀 |
该实验得出的结论是________。丙同学认为该实验方案不足以证明灰绿色是由Fe(OH)2表面吸附Fe2+引起的,还需补充的实验是__________,证明该假设成立。
(3)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件_____。
(4)下列情况会导致所配NaOH溶液的浓度偏高的是_______。
A.NaOH溶液未冷却至室温就进行定容 B.配制前容量瓶中有少量的水
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
查看答案和解析>>
科目: 来源: 题型:
【题目】被称之为“软电池”的纸质电池,其电池总反应为Zn+2MnO2+H2O![]() ZnO+2MnO(OH)。下列说法正确的是( )
ZnO+2MnO(OH)。下列说法正确的是( )
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.当65 g Zn完全溶解时,流经电极的电子为1mol
D.电池正极反应式为2MnO2+2e-+2H2O![]() 2MnO(OH)+2OH-
2MnO(OH)+2OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】用铂电极电解100mLHNO3 与AgNO3 的混合液,通电一段时间后,两极均收集到4.48L气体(标准状况),则原混合液中Ag+的物质的量浓度为( )
A. 1mol·L-1B. 2mol·L-1C. 2.5mol·L-1D. 4mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)将一块未打磨过的铝片放入装有少量NaOH溶液的试管中,会发现开始没有气泡,一段时间后才产生气泡。请写出发生反应的离子方程式:___________,___________。
(2)将8gFe2O3投入到150mL某浓度的稀H2SO4中,再投入7g铁粉收集到1.68LH2(标准状况),同时,Fe与Fe2O3均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗4mol/L的NaOH溶液150mL。则原硫酸的物质的量浓度为________。
(3)请写出制备漂白粉的离子方程式:____________。
(4)配平下列离子方程式:______Fe(OH)3+ClO-+OH-=FeO42-+Cl-+H2O。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究表明气孔的张开与保卫细胞膜上的H+—ATPase有着非常密切的关系。H+—ATPase被蓝光诱导激活后就会利用ATP水解释放的能量将H+分泌到细胞外,此时内向K+离子通道开启,细胞外的K+转移进保卫细胞;同时其他相关阴离子在H+协助下也进入保卫细胞,从而使气孔张开。气孔张开运动的相关机理如下图所示。
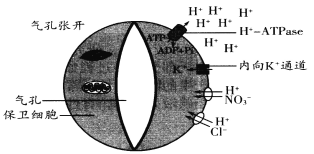
注:图中两个细胞贴近气孔部分细胞壁较厚,伸缩性较小,外侧较薄
(1)保卫细胞膜上的H+—ATPase被激活时,细胞内的H+通过____________的方式转移出保卫细胞;据细胞吸水与失水的原理推测,蓝光诱导后气孔张开的原因是__________________。
(2)植物有时为防止水分过度散失气孔会关闭,此时叶肉细胞仍可进行光合作用,消耗的CO2可来自___________和___________,但光合速率会明显减慢;气孔开启瞬间植物叶肉细胞消耗C5的速率会___________(填“增大”或“减小”或“不变”)。
(3)科研人员利用转基因技术在拟南芥保卫细胞中表达了由光控制的K+通道蛋白BL,试图提高气孔动力,即光照增强时气孔打开的更快,光照减弱时关闭的也更快。
①欲探究BL蛋白是否发挥了此功能,可在变化的光照强度和恒定光照强度下,分别测正常植株和转基因植株的气孔动力,该实验的自变量是_____________________。
②若实验表明BL蛋白发挥了预期的作用,而在恒定光照强度下生长的转基因株系生物量积累和用水效率方面,与正常植株无明显差异,说明____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com