
科目: 来源: 题型:
【题目】氯及其化合物在生产生活中都有重要的应用。
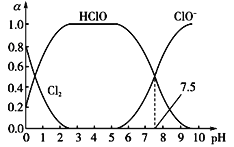
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气—氯水体系,该体系中Cl2、HClO和ClO-的物质的量分数(a)随pH变化的关系如图所示。由图分析,要使氯水的杀菌效果最好,应控制溶液的pH范围是_____________,当pH=7.5时,氯水中含氯元素的微粒有_____________________。
(2)工业上用氯气与石灰乳生产漂白粉的化学方程式为_______________________。
(3)二氧化氯(ClO2)是国际上公认的高效、安全的杀菌消毒剂。工业上制备ClO2的反应为2KClO3 + H2C2O4 + H2SO4 = K2SO4 + 2ClO2↑+ 2X + 2H2O。
①X的化学式为______________。
②ClO2和Cl2均是生活中常用的消毒剂,ClO2的消毒效率是Cl2的_______倍(消毒效率以物质单位物质的量得到的电子数表示,还原产物均为Cl-。)
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2S2O5可用作食品的抗氧化剂。为测定某葡萄酒中Na2S2O5残留量,取50.00 mL葡萄酒样品,用0.01000 mol·L1的碘的水溶液与其反应,恰好消耗10.00 mL。下列说法正确的是( )
A.反应的离子方程式为:S2O52- + I2 + 3H2O = 2SO42- + 2I-+ 6H+
B.该反应转移电子数为1×10-3NA
C.该样品中Na2S2O5的残留量,若以SO2计为0.128 g·L1
D.反应结束后,所得溶液的pH比原溶液增大
查看答案和解析>>
科目: 来源: 题型:
【题目】已知充分燃烧a g乙炔气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
A. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=+b kJ/mol
B. C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l);△H=+2b kJ/mol
O2(g)=2CO2(g)+H2O(l);△H=+2b kJ/mol
C. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=-2b kJ/mol
D. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=-4b kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】将2.56gCu和200mL某浓度的浓HNO3混合,随着反应的进行生成气体的颜色逐渐变浅,当Cu反应完全时,共收集到气体1.12L(标准状况)。
下列关于该反应的分析错误的是( )
A.该反应生成的NO2与NO的体积比为7 : 3
B.该反应转移电子数为0.04NA
C.该反应消耗HNO3的物质的量为0.13mol
D.反应结束后所得溶液中(忽略反应前后溶液体积的变化)c(NO3-) = 0.4 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知热化学方程式:C(金刚石,s)+O2(g)=CO2(g) △H1 ;
C(石墨,s)+O2(g)=CO2(g) △H2;
C(石墨,s)=C(金刚石,s)△H3=+1.9kJ/mol 下列说法正确的是
A. 金刚石比石墨稳定 B. △H1 > △H2
C. △H3=△H1 -△H2 D. 石墨转化成金刚石的反应是吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】利用如图装置制取下表中的四种气体(图中夹持仪器已略去;a、b、c表示相应仪器中加入的试剂),能达到实验目的的是( )
选项 | 气体 | a | b | c |
|
A | H2 | 稀硫酸 | Zn | 浓硫酸 | |
B | CO2 | 盐酸 | CaCO3 | 饱和碳酸氢钠溶液 | |
C | NH3 | 浓氨水 | CaO | 浓硫酸 | |
D | Cl2 | 浓盐酸 | MnO2 | 饱和食盐水 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
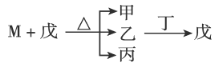
【题目】W、X、Y、Z为原子序数依次递增的短周期主族元素,其中X的某同位素可用于测量文物年代,M为由X元素构成的一种单质。甲和丁两种物质都由W和Y元素组成,乙由Y和Z元素组成,常温下为气体,具有漂白性,戊为二元强酸。它们之间的转化关系如下,下列叙述正确的是( )
A.气态氢化物的稳定性:X>Y>ZB.原子半径顺序:Z>Y>X>W
C.丁的水溶液适用于医用伤口消毒及环境消毒D.常温常压下,M能和丙发生化合反应
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.氢气用于工业合成氨 N2(g) + 3H2(g) ![]() 2NH3(g);ΔH = -92.2 kJ·mol-1。一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t5 ﹑t7时刻所对应的实验条件改变分别是
2NH3(g);ΔH = -92.2 kJ·mol-1。一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t5 ﹑t7时刻所对应的实验条件改变分别是
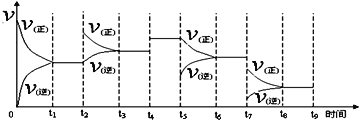
t5 ___________________。t7___________________。
Ⅱ.已知化学反应①:Fe(s)+CO2(g) ![]() FeO(s)+CO(g), 其平衡常数为K1;
FeO(s)+CO(g), 其平衡常数为K1;
化学反应②:Fe(s)+H2O(g) ![]() FeO(s)+H2(g),其平衡常数为K2。
FeO(s)+H2(g),其平衡常数为K2。
在温度973K和1173K情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973K | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
(1)1173K时,若c(CO2)=2mol/L,c(CO) =5mol/L,则此时反应①平衡向__________(填“正”或“逆”)反应方向移动。
(2)现有反应③CO2(g)+H2(g) ![]() CO(g)+H2O(g),写出该反应的平衡常数K3的表达式:K3=_______________________(用K1 、 K2表示)。据此关系式及上表数据,能推断出反应③是______(填“吸热”或“放热”)反应。要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施是______(填写序号)。
CO(g)+H2O(g),写出该反应的平衡常数K3的表达式:K3=_______________________(用K1 、 K2表示)。据此关系式及上表数据,能推断出反应③是______(填“吸热”或“放热”)反应。要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施是______(填写序号)。
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度
D.升高温度 E.使用合适的催化剂 F.设法减少CO的量
能判断反应③已达平衡状态的是_______________________________。
A.恒容容器中压强不变 B.混合气体中c(CO)不变
C.![]() (H2)==
(H2)==![]() (H2O) D.c(CO2)==c(CO)
(H2O) D.c(CO2)==c(CO)
(3)723K时,0.2molCO2和0.1molH2通入抽空的1L恒容密闭容器中,发生反应③,达到平衡后水的物质的量分数为0.1。则H2的转化率α(H2)=___________%。723K该反应的平衡常数为K=________________。(结果保留两位有效数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】Z是合成某药物的中间体,其合成原理如下:
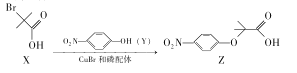
下列说法正确的是.
A.用NaHCO3溶液可以鉴别X和ZB.X、Y、Z都能发生取代反应
C.X分子所有碳原子可能共平面D.与X具有相同官能团的同分异构体还有5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com