
科目: 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是

A. 断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl—![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl—
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目: 来源: 题型:
【题目】某充电宝锂离子电池的总反应为:xLi+Li1-xMn2O4 ![]() LiMn2O4,某手机镍氢电池总反应为: NiOOH+MH ==== M+Ni(OH)2(M为充电储氧金属或合金),有关上述两种电池的说法不正确的是( )
LiMn2O4,某手机镍氢电池总反应为: NiOOH+MH ==== M+Ni(OH)2(M为充电储氧金属或合金),有关上述两种电池的说法不正确的是( )
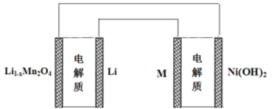
A. 锂离子电池放电时Li+向正极迁移
B. 镍氢电池放电时,正极的电极反应式NiOOH+H2O+e-Ni(OH)2+OH-
C. 上图表示用锂离子电池给镍氢电池充电
D. 锂离子电池充电时,阴极的电极反应式LiMn2O4-xe-=Li1-xMn2O4+xLi+
查看答案和解析>>
科目: 来源: 题型:
【题目】硼酸在生活中应用广泛,H3BO3可以通过电解NaB(OH)4溶液的方法制备,其工作原理如图,a、c为阳离子交换膜,且H+可B(OH)4-与反应生成H3BO3,下列叙述错误的是( )
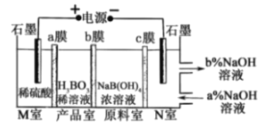
A. M室发生的电极反应式为:2H2O-4e-=O2↑+4H+
B. N室中:a%<b%
C. b膜为阴离子交换膜,产品室发生反应的化学原理为强酸制弱酸
D. 理论上每生成1mol产品,阴极室可生成标准状况下5.6L气体
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是( )
A.能使酚酞变红的溶液:Na+、Al3+、SO42-、NO3-
B.![]() =10-12的溶液:NH4+、Na+、SO42-、Cl-
=10-12的溶液:NH4+、Na+、SO42-、Cl-
C.0.1 mol·L-1Na2SO3溶液:NH4+、K+、ClO-、Cl-
D.0.1 mol·L-1 FeCl3溶液:Mg2+、Al3+、MnO4-、SCN-
查看答案和解析>>
科目: 来源: 题型:
【题目】一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸(H3BO3)及轻质氧化镁的工艺流程如下:
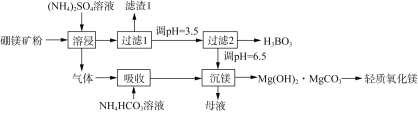
回答下列问题:
(1)“溶浸”硼镁矿粉过程中,提高B、Mg元素的浸出率可以采用什么措施________(填写两点)。
(2)“溶浸”后产生的气体是__________(填化学式)。
(3)为检验“过滤1”后的滤液中是否含有Fe3+,可选用的化学试剂是______________溶液(填化学式)。
(4)根据H3BO3的解离反应:H3BO3+H2O![]() H++B(OH)4,Ka=5.81×10-10,写出H3BO3与NaOH反应的离子方程式________________________________________。
H++B(OH)4,Ka=5.81×10-10,写出H3BO3与NaOH反应的离子方程式________________________________________。
(5)写出“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式以及将碱式碳酸镁高温灼烧制备轻质氧化镁的化学方程式________________、____________。
查看答案和解析>>
科目: 来源: 题型:
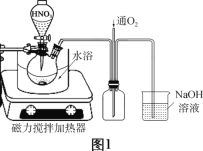
【题目】实验室以废铜屑(含少量Fe、不溶性杂质)为原料制取CuSO4·5H2O晶体和[Cu(NH3)4]SO4·H2O晶体,其实验流程如下:
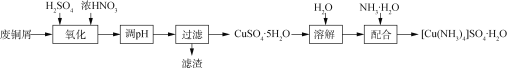
(1)氧化时先加入一定量3 mol/L H2SO4,再调节浓硝酸的用量至![]() 为2.0左右时,铜粉和浓硝酸完全反应,主要反应的化学方程式为_______。
为2.0左右时,铜粉和浓硝酸完全反应,主要反应的化学方程式为_______。
硝酸过量对产品的影响为________________________________。
(2)废铜屑的氧化在如图1所示的装置中进行。从长导管中通入氧气的作用是___________。保持试剂的用量不变,实验中提高Cu转化率的操作有____________(写一种)。
(3)调节溶液pH应在3.5~4.5范围的原因是______________________。
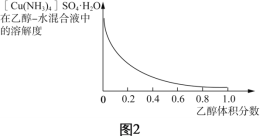
(4)已知:[Cu(NH3)4]2+![]() Cu2++4NH3;CuSO4、(NH4)2SO4难溶于乙醇。结合图2,[Cu(NH3)4]SO4·H2O在乙醇水混合液中的溶解度随乙醇浓度变化曲线,补充完整由加足量氨水后所得的[Cu(NH3)4]SO4溶液制备[Cu(NH3)4]SO4·H2O晶体的实验方案:______________ (实验中必须使用的试剂和仪器:无水乙醇、乙醇-水混合液、BaCl2溶液、真空干燥箱)。
Cu2++4NH3;CuSO4、(NH4)2SO4难溶于乙醇。结合图2,[Cu(NH3)4]SO4·H2O在乙醇水混合液中的溶解度随乙醇浓度变化曲线,补充完整由加足量氨水后所得的[Cu(NH3)4]SO4溶液制备[Cu(NH3)4]SO4·H2O晶体的实验方案:______________ (实验中必须使用的试剂和仪器:无水乙醇、乙醇-水混合液、BaCl2溶液、真空干燥箱)。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.4.0g重水(D2O)中所含质子数为0.4NA
B.4.48L N2与CO的混合物中所含分子数为0.2NA
C.常温下,7.1g Cl2与足量NaOH溶液反应转移的电子数约为0.1NA
D.0.2mol Na2O2中含有离子总数为0.8NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知有位于元素周期表前四周期的元素X、Y、Z、T、W、Q,其部分信息如下表:
X | 宇宙中含量最丰富的元素 |
Y | 植物生长所必需的三种营养元素中,电负性最大的 |
Z | 原子最外层电子数是其电子层数的3倍 |
Q | 其气态氢化物与其低价氧化物常温下能反应,生成该元素的单质 |
T | 最高正价与最低负价代数和为6,其单质能与强碱溶液反应制消毒液 |
W | 其+2价阳离子的价电子排布为3d9 |
请回答下列问题:
(1)W元素位于周期表的第___周期___族,W2+能与X、Y形成的简单分子结合生成一种深蓝色的离子,其离子符号为___。
(2)X与Z按原子个数比为1:1组合得到的一种物质甲,它能用于杀菌消毒,物质甲的电子式为___;Q与T也能按原子个数比为1:1组合,得到一种暗黄色的液体乙,其结构与甲相似,则乙中存在的化学键类型有___和___;乙遇水发生歧化反应,得到一种淡黄色的固体和两种具有刺激性气味的气体,该反应的化学反应方程式为___。
(3)元素Q的简单离子半径___元素T的简单离子半径(填“>”“<”或“=”);元素T能形成多种含氧酸:HTO、HTO2、HTO3、HTO4,其酸性由强到弱的顺序为___(用化学式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与硼(5B)同主族,与铷(37Rb)同周期。下列说法不正确的是
A.In是第五周期第ⅢA族元素B.![]() 的中子数与电子数的差值为17
的中子数与电子数的差值为17
C.原子半径:In>AlD.碱性:In(OH)3>RbOH
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,E为固体,F为有磁性的化合物。它们之间存在如下关系(反应中生成的水及次要产物均已略去):
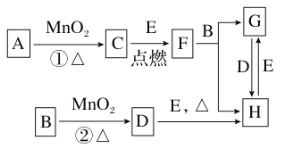
(1)写出下列物质的化学式:B________,E________。
(2)指出MnO2在相关反应中的作用:反应①中是________剂,反应②中是________剂。
(3)若反应①是在加热条件下进行,则A是________(填化学式);若反应①是在常温条件下进行,则A是________(填化学式);如在上述两种条件下得到等质量的C单质,反应中转移的电子数之比为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com