
科目: 来源: 题型:
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是
3C(g)+4D(g)反应中,表示该反应速率最快的是
A. v(A)=0.5mol/(L·s)B. v(B)=0.3mol/(L·s)
C. v(C)=0.8mol/(L·s)D. v(D)=1.0mol/(L·s)
查看答案和解析>>
科目: 来源: 题型:
【题目】利用如图装置可以验证非金属性的变化规律。
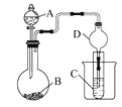
(1)仪器A的名称为________,干燥管D的作用是________________。
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为_________________,离子方程式为______。
(3)若要证明非金属性:S>C>Si,则A中加________、B中加Na2CO3、C中加________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。

(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是__________。
②称取样品,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为________、________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是_______________。
②E处干燥管中盛放的药品是碱石灰,其作用是_____________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量_____________(填“偏大”“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1g、m2g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】不同波长的光可以使有机化合物之间相互转化。如俘精酸酐类化合物甲、乙可以发生如下转化:
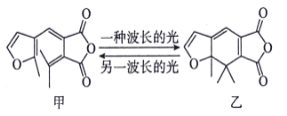
下列说法错误的是( )
A.甲与乙互为同分异构体
B.甲生成乙的反应类型为加成反应
C.甲、乙两种分子中均没有手性碳原子
D.1mol甲分子与足量NaOH溶液反应时消耗2mo1NaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】可通过下列流程回收废旧锂离子电池正极材料(LiCoO2,含少量Al、Fe)中的钴和锂。
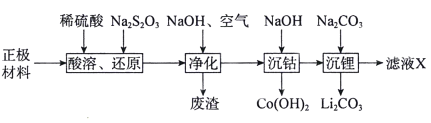
回答下列问题:
(1)“酸溶、还原”过程中S2O32-转化为SO42-,LiCoO2参与反应的离子方程式为____________________________________。
(2)“废渣”的主要成分为___________________。
(3)“沉钴”过程中,当溶液的pH=10时,c(Co2+)=______mol· L-1(已知常温下KSP[Co(OH)2]=1.58×10-15)。
(4)在空气中加热Co(OH)2,固体残留率随温度的变化如图所示。

290℃时,完全脱水变为Co2O3,反应的化学方程式为_______________;500℃时的主要产物为_____________(填化学式);将1000℃时的分解产物1mol与2.2mol Na2O(稍过量)在充氩封闭管中共热,会生成鲜红色的晶体,该晶体的阴离子为正三角形结构,晶体的化学式为__________________。
(5)“滤液X”中最主要的溶质是_______________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(s)的能量变化如图所示,下列叙述正确的是

A. 该反应为放热反应
B. A—B的键能为bkJmol-1
C. 加催化剂能降低该反应焓变
D. 该反应的反应热为△H=(a-b)kJmol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】电子工业上使用的印刷电路板,是在敷有铜膜的塑料板上以涂层保护所要的线路,然后用三氯化铁浓溶液作用掉(腐蚀)未受保护的铜膜后形成的。某工程师为了从使用过的腐蚀废液(含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费)中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用,准备采用下列步骤:
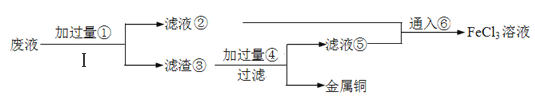
(1)步骤Ⅰ的操作名称:________;所需玻璃仪器:_________、_________、__________。
(2)写出FeCl3溶液与铜箔发生反应的离子方程式:______________________。
(3)检验废腐蚀液中是否含有Fe3+所需试剂名称:___________、实验现象:__________。
(4)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:________________,此转化的化学方程式为:______________________________。
(5)写出③中所含物质:_________⑥发生反应的离子方程式:_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】酮洛芬是临床用于治疗疼痛的药物。合成酮洛芬的一种路线如下:

(1)F中含氧官能团的名称为____________________(写两种)。
(2) 与(CH3)2SO4反应也可以直接得到酮洛芬,该反应的类型为____________。
与(CH3)2SO4反应也可以直接得到酮洛芬,该反应的类型为____________。
(3)B的分子式为C10H11NO4,写出B的结构简式:____________________。
(4)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______________________。
①能与FeCl3溶液发生显色反应,且分子中有一个手性碳原子;
②碱性条件水解后酸化,产物之一是α-氨基酸,另一水解产物分子中只有3种不同化学环境的氢。
(5)已知:NO2![]() NH2。
NH2。
请写出以 和ClCH2COOC2H5为原料制备H3COCH3CHO的合成路线流程图___________(无机试剂任用,合成路线流程图示例见本题题干)。
和ClCH2COOC2H5为原料制备H3COCH3CHO的合成路线流程图___________(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol1
O2(g)=H2O(g) ΔH1=akJ·mol1
②2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol1
O2(g)=H2O(l) ΔH3=ckJ·mol1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol1
下列关系式中正确的是
A.a<c<0B.b>d>0C.2a=b<0D.2c=d>0
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应不仅有物质变化,同时还伴随着能量的变化,化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1)在25℃、101KPa下,1gCH3OH与氧气充分反应,生成二氧化碳气体和水时释放出22.68kJ的热量,则表示甲醇燃烧热的热化学方程式为:_____。
(2)已知已知葡萄糖的燃烧热是2804kJ/mol,当它氧化生成1g液态水时放出的热量是__________ kJ(结果保留两位小数)
(3)已知热化学方程式C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2220 kJ/mol,2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ/mol
①现有H2和C3H8的混合气体共5mol,完全燃烧时放热3472.9kJ,则混合气体中H2和C3H8的体积比为__________。
②1mol H2和2 mol C3H8组成的混合气体共完全燃烧时放热_________ kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com