
科目: 来源: 题型:
【题目】氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质作用(四种物质与氯水的重合部分代表物质间的反应,且氯水足量),请回答下列问题:

(1)反应d中,将氯水滴加到一张蓝色石蕊试纸上,试纸上会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,下列有关说法中错误的是___

A.此实验表明氯水具有酸性、漂白性
B.内环呈白色外环呈红色或浅红色
C.内外环上颜色的差异表明此变化过程中,酸使指示剂的颜色变化比氧化还原反应慢
D.氯气与水反应中氧化产物是HClO
(2)反应e的离子方程式为___。
(3)反应b有气体产生,生成该气体反应的化学方程式为___。
(4)久置的氯水最终会变成___(填名称),则反应a的化学方程式表示为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、Cl-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
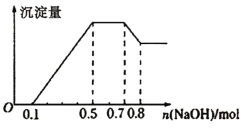
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中一定不含CO32-和SO42-,可能含有Cl-
C.溶液中n(Mg2+)=0.1mol
D.n(H+) :n(NH4+) : n(Al3+) : n(Mg2+)=2:4:2:1
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用如下反应制取P4:2Ca(PO4)2 +6SiO2+10C![]() 6CaSiO3+P4+10CO
6CaSiO3+P4+10CO
回答下列问题:
(1)基态硅原子的核外电子排布式为___。
(2)Si、P、S元素第一电离能大小关系为___。
(3)P4中P原子的杂化方式是___ ,P4的空间结构为___ ,键角∠PPP=___。
(4)与CO互为等电子的阴离子是___ (填化学式)。
(5)晶体硅与金刚石结构相似,下图为晶体硅的晶胞结构。已知硅原子的半径为r nm,晶体硅的密度是___g/cm3。
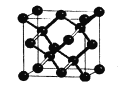
(6)硅的含氧化合物都以硅氧四面体(SiO4)作为基本结构单元,如图a所示,可简化为图b。

硅、氧原子通过共用氧原子形成各种不同的硅酸根负离子,如图c和图d,图c的化学式____________。在无限长链的硅酸根中硅氧原子之比为____。

硅、氧原子除可形成长链外,也可形成层状和立体网状结构。在立体网状结构中,硅、氧原子数之比为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】25 °C时,用氢氧化钠调节浓度为2.0×10-3mol L-1的氢氟酸溶液的pH (忽略体积 变化),溶液中c(HF)、c(F- )与pH的变化关系如下图所示。下列说法不正确的是

A. abd曲线代表c(F-)随pH的变化
B. 25 °C时,HF电离平衡常数的数值Ka=10-3.6
C. 从b点到c点发生的离子反应方程式是:HF + OH- = H2O+ F-
D. 图中a点溶液粒子浓度大小是:c(HF)>c(H+)>c(F-)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解槽装置如左图,用Cu-Si合金作硅源,在950℃利用三层液熔盐进行电解精炼,并利用某CH4燃料电池(右图)作为电源。有关说法不正确的是

A. 电极c与a相连,d与b相连
B. 左侧电解槽中:Si 优先于Cu被还原,Cu优先于Si被氧化
C. 三层液熔盐的作用是增大电解反应面积,提高硅沉积效率
D. 相同时间下,通入CH4、O2的体积不同,会影响硅提纯速率
查看答案和解析>>
科目: 来源: 题型:
【题目】萝卜硫素(结构如图)是具有抗癌和美容效果的天然产物之一,在一些十字花科植物中含量较丰富。该物质由五种短周期元素构成,其中W、X、Y、Z的原子序数依次增大,Y、Z原子核外最外层电子数相等。下列叙述一定正确的是( )
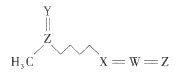
A.原子半径的大小顺序为Z>W>X>Y
B.X的简单氢化物与W的氢化物反应生成离子化合物
C.萝卜硫素中的各元素原子最外层均满足8电子稳定结构
D.Y、Z形成的二元化合物的水化物为强酸
查看答案和解析>>
科目: 来源: 题型:
【题目】目前工业上可利用 CO 或 CO2 来生产燃料甲醇,某研究小组对下列有关甲醇制取的三 个化学反应进行了探究。已知在不同温度下的化学平衡常数(K1、K2、K3)如表所示。
化学反应 | 焓变 | 平衡 常数 | 温度/℃ | ||
500 | 700 | 800 | |||
①2H2(g)+CO(g) | ΔH1 | K1 | 2.5 | 0.34 | 0.15 |
②CO2(g)+H2(g) | ΔH2 | K2 | 1.0 | 1.70 | 2.52 |
③CO2(g)+3H2(g) | ΔH3 | K3 | |||
请回答下列问题:
(1)反应②是_____(填“吸热”或“放热”)反应;反应③的平衡常数表达式为 K=_____;
(2)根据反应①与②可推导出 K1、K2 与 K3 之间的关系,则 K3=_____(用 K1、K2 表示);根据反应③判断ΔS_____(填“>”“=”或“<”)0,在_____(填“较高”或“较低”)温度下有利于该反应自 发进行。
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有___________ (填字母,后同)。
A.缩小反应容器的容积 B.增大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.从平衡体系中及时分离出 CH3OH
(4)500 ℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为 0.1 mol·L-1、0.8 mol·L-1、0.3 mol·L-1、0.15 mol·L-1,则此时 v(正)__________ v(逆)(填“>”“=”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关铁的化合物的说法不正确的是
A.实验室为了暂时妥善保存硫酸亚铁溶液,常加入少量的铁粉
B.某溶液若加入KSCN溶液,无变化,但通入Cl2后变血红色,说明原溶液中含有Fe2+
C.欲检验FeSO4溶液是否全部变质,可加入少量酸性高锰酸钾溶液观察紫色是否褪去
D.将适量铁粉放入FeCl3溶液中完全反应后,溶液中Fe2+和Fe3+的浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示 3 套实验装置,分别回答下列问题。

(1)装置 1 为铁的吸氧腐蚀实验。向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶 液变红,该电极反应式为_____。
(2)装置 2 中左池为氯化铁溶液,右池为硫酸铜溶液,一段时间后右池溶液中 c(Cu2+)_____(填“增大”、“减小”或“不变”),若该装置的盐桥中盛装的是 NH4NO3 的琼脂溶液,则盐桥中的_____离子(填“NH4+ ”或“NO3-”)向氯化铁溶液迁移。
(3)装置 3 中甲烧杯盛放 100mL 0.2mol/L 的 NaCl 溶液,乙烧杯盛放 100mL 0.5mol/L 的 CuSO4 溶 液。反应一段时间后,观察到乙烧杯的石墨电极上有气泡生成。
①电源的 M 端为电源_____极。
②乙烧杯中电解反应的离子方程式为_____。
③停止电解,取出 Cu 电极,洗涤、干燥、称量,电极增重 0.32g,甲烧杯中产生的气体标准状况下体积为_________mL。
④若要将乙池设计成电解精炼铜的装置,则乙池的石墨应改成____(填“粗铜”或“精铜”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中的一定量的混合气体发生反应:xA(g)+yB(g)![]() zC(g)平衡时测得C的浓度为1 mol·L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达到平衡时,测得C的浓度为0.6 mol·L-1,下列有关判断正确的是( )
zC(g)平衡时测得C的浓度为1 mol·L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达到平衡时,测得C的浓度为0.6 mol·L-1,下列有关判断正确的是( )
A. x+y>zB. 平衡向逆反应方向移动
C. B的转化率降低D. A的体积分数减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com