
科目: 来源: 题型:
【题目】某科研团队研究发现硼氢化钠(NaBH4)在催化剂Ru表面与水反应可生成H2,其反应机理如图所示:
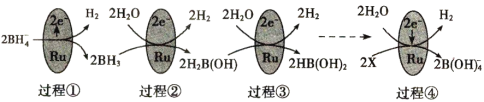
根据以上信息判断,下列叙述错误的是
A.过程①至过程④中硼元素的化合价不变
B.X是H3BO3,H3BO3和BH3两分子中H的化合价相等
C.过程③和过程④各产生1molH2时转移的电子数不相等
D.0.25molNaBH4的还原能力与标准状况下22.4LH2的还原能力相当(还原能力即生成H+失去电子的量)
查看答案和解析>>
科目: 来源: 题型:
【题目】Cu2O在涂料、有色玻璃和催化剂等领域有着广泛的用途。Cu2O为红色粉末,不溶于水,易溶于盐酸和稀硫酸。可用电解法制备氧化亚铜:用铜作阳极,钛片作阴极,电解液为一定浓度的NaCl和NaOH的混合溶液;阳极及其溶液中有关转化如图所示。下列说法错误的是

A.电解液中的NaOH不能用盐酸代替
B.过程①中Cu被氧化生成CuCl-
C.过程④的离子方程式为2Cu(OH)Cl-=Cu2O+2Cl-+H2O
D.当电路中有0.05mol e-通过时,消耗0.32g Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】白银(Ag)是高新技术产业的基础材料之一。在一种光盘金属层中回收少量白银(金属层中其他金属含量过低,对实验的影响可忽略)的流程如下:
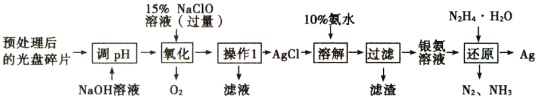
已知:NaC1O溶液在受热或酸性条件下易分解。
下列叙述正确的是
A.“氧化”过程若在加强热和强酸性条件下进行时可提高氧化速率
B.“操作1”所用到的玻璃仪器是玻璃棒、烧杯、分液漏斗
C.若“还原”过程通过原电池来实现,则N2为正极产物
D.“还原”过程中参加反应的n[Ag(NH3)![]() ]:n[N2H4·H2O]=4:1
]:n[N2H4·H2O]=4:1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作能够达到实验目的的是( )
A.液溴易挥发,在存放液溴的试剂瓶中应加入少量水
B.实验室采用如图所示装置收集Cl2
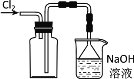
C.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤
D.用酒精萃取碘水中的碘单质
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钾(K2FeO4)是优良的多功能、绿色水处理剂。制备高铁酸钾的装置如图:
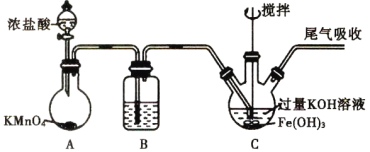
资料:①K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中比较稳定。②制备K2FeO4的反应为放热反应。下列叙述正确的是
A.装置A中的KMnO4可以用MnO2代替
B.装置B中的试剂为饱和碳酸氢钠溶液,目的是除去C12中的HC1
C.装置C中生成K2FeO4的关键操作是要缓慢通入Cl2且不能过量
D.K2FeO4做水处理剂时能杀菌消毒、吸附悬浮物与Cl2作用相同
查看答案和解析>>
科目: 来源: 题型:
【题目】已知3.25g金属Zn恰好与250mL某浓度的盐酸完全反应,计算:
(1)该盐酸的物质的量浓度;___________
(2)标准状况下,该反应生成的气体的体积。_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下存在反应:H2(g) + I2(g)![]() 2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
A. 容器Ⅰ、Ⅱ中正反应速率相同
B. 容器Ⅰ、Ⅲ中反应的平衡常数相同
C. 容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深
D. 容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21。下列说法不正确的是
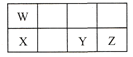
A.原子半径大小:X > Y > Z
B.W、Y两种元素都能与氧元素形成化合物WO2、YO2
C.氧化物对应水化物的酸性: Z > Y > W
D.Y能形成H2Y、H2YO4的化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器.当其它条件相同时,在Ⅰ、Ⅱ中分别加入2molX和2molY,开始时容器的体积均为VL,发生如下反应并达到平衡状态(提示:物质X、Y的状态均未知,物质Z的状态为气态):2X(?)+Y(?)aZ(g)此时Ⅰ中X、Y、Z的物质的量之比为1:3:2。下列判断正确的是( )
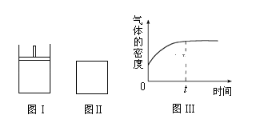
A.物质Z的化学计量数a=2
B.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y中只有一种为气态
C.若X、Y均为气态,则在平衡时X的转化率:Ⅰ<Ⅱ
D.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X是金属元素,W、Y是不同主族的非金属元素且最外层电子数为偶数,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如下图所示。下列叙述正确的是
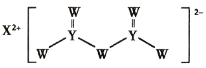
A.W、X离子半径比较:X>W
B.Y、Z的氢化物稳定性比较:Y>Z
C.1mol YW2晶体中含有4mol Y—W键
D.工业上可通过电解熔融XW来生产X的单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com