
科目: 来源: 题型:
【题目】下列事实不能用电化学原理解释的是( )
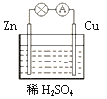
A.可将地下输油钢管与外加直流电源的负极相连以保护钢管不受腐蚀
B.常温条件下,铝在空气中不易被腐蚀
C.镀层破坏后,白铁(镀锌的铁)比马口铁(镀锡的铁)更耐腐蚀
D.用锌与稀硫酸刮氢气时,往稀硫酸中滴少量硫酸铜溶液能加快反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以锈蚀程度很大的废铁屑为原料制备FeCl3·6H2O晶体的流程可简要表示如下:
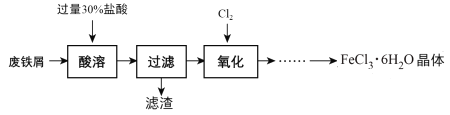
已知:在水溶液中Fe2+能与K3Fe(CN)6生成蓝色沉淀Fe3[Fe(CN)6]2。
试回答下列问题:
(1)“酸溶”过程中发生主要反应有:
①Fe +2H+=Fe2++H2↑;②Fe2O3+ 6H+=2Fe3++3H2O;③___。(用离子方程式表示)
(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是____。
(3)“过滤”需要的玻璃仪器除烧杯外还有___。
(4)“氧化”过程可在如图所示装置中进行。
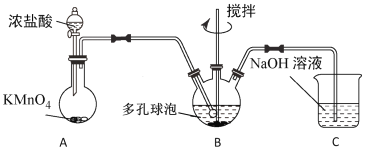
①装置A中KMnO4与浓盐酸反应生成MnCl2和Cl2,其离子方程式为___。
②装置C的作用是____。
③为使Cl2能充分发生反应,除在B中使用多孔球泡和搅拌外,实验中可采取的措施是___。
④证明装置B溶液中Fe2+已完全被氧化成Fe3+的实验方案是___。
查看答案和解析>>
科目: 来源: 题型:
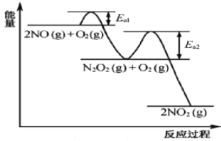
【题目】NO氧化反应:![]() 分两步进行,其反应过程能量变化示意图如图,下列说法不正确的是( )
分两步进行,其反应过程能量变化示意图如图,下列说法不正确的是( )
I.![]() H1;II.
H1;II.![]() H2
H2
A.由于![]() ,决定化学反应速率快慢的是反应Ⅱ
,决定化学反应速率快慢的是反应Ⅱ
B.图示过程中,反应物断键吸收能量小于生成物形成所释放的能量
C.升高温度,2NO(g)+O2(g)![]() 2NO2(g)反应速率一定加快
2NO2(g)反应速率一定加快
D.其它条件不变,升高温度,![]() 平衡一定逆向移动
平衡一定逆向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于化学反应速率和化学反应限度的说法中正确的是( )
A.化学反应速率是衡量化学反应进行快慢程度的物理量
B.化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示
C.当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度,即使条件改变,该限度都不改变
D.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
A. K=![]()
B. K=![]()
C. 增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D. 改变反应的温度,平衡常数不一定变化
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习兴趣小组为测定某葡萄酒中SO2的含量,设计了如图所示的装置:
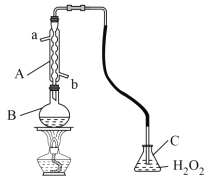
实验步骤如下:在B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应。除去C中剩余的H2O2后,用0.0900mol·L-1NaOH溶液测定反应生成的酸,消耗NaOH溶液25.00mL。
(1)C中通入SO2发生反应的化学方程式为___。
(2)通过计算求出该葡萄酒中SO2的含量(以g·L-1为单位,即每升葡萄酒中含有SO2的质量) ___。(写出计算过程)
(3)该测定结果比实际值偏高,可能的原因是____。针对此原因提出一条改进措施:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.Ca(OH)2![]() Ca(ClO)2(aq)
Ca(ClO)2(aq)![]() HClO(aq)
HClO(aq)
B.Fe(s)![]() Fe2O3(s)
Fe2O3(s)![]() FeCl3(aq)
FeCl3(aq)
C.S(s)![]() SO2(g)
SO2(g)![]() BaSO3(s)
BaSO3(s)
D.NH3(g)![]() NO(g)
NO(g)![]() HNO3(aq)
HNO3(aq)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应![]() 在四个不同条件下进行。B、D起始为0,反应物A的浓度
在四个不同条件下进行。B、D起始为0,反应物A的浓度![]() 随反应时间
随反应时间![]() 变化情况如下表:
变化情况如下表:
实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800℃ | 1.0 | 0.8 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ |
| 0.8 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
3 | 800℃ |
| 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
下列说法不正确的是( )
A.实验1,反应在10至![]() 内
内![]()
B.实验2,A的初始浓度![]() ,还隐含的条件是加入了催化剂
,还隐含的条件是加入了催化剂
C.实验3的反应速率v3<实验1的反应速率v1
D.比较实验4和实验1,可推测该反应为吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上由含铜废料(含有Cu、CuS、CuSO4等)制备硝酸铜晶体的流程如图:
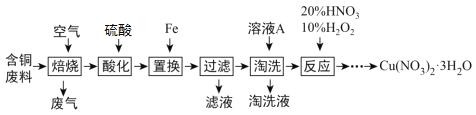
(1)“焙烧”时CuS转化为CuO和SO2,反应的化学方程式为___。
(2)“酸化”步骤反应的离子方程式为___。
(3)“过滤”所得滤液中溶质的主要成分为___。
(4)“淘洗”所用的溶液A应选用___(填序号)。
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”一步的过程中无红棕色气体生成。
①理论上消耗HNO3和H2O2的物质的量之比为___。
②若不加10% H2O2,只用浓HNO3,随着反应的进行,容器内持续出现大量红棕色气体,写出该反应的离子方程式____。
(6)由“反应”所得溶液中尽可能多地析出Cu(NO3)2·3H2O晶体的方法是___。(相关物质的溶解度曲线如图所示)
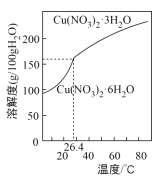
查看答案和解析>>
科目: 来源: 题型:
【题目】标况下将8.96 L氯化氢气体溶于水形成100 mL溶液,然后与足量的铁屑反应。
(1)所得盐酸溶液的物质的量浓度是多少________?
(2)参加反应的铁的质量是多少________?
(3)标况下生成氢气的体积是多少________?
(4)将生成的氯化亚铁配成400 mL溶液,此溶液中氯化亚铁的物质的量浓度是多少________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com