
����Ŀ��ijѧϰ��ȤС��Ϊ�ⶨij���Ѿ���SO2�ĺ������������ͼ��ʾ��װ�ã�
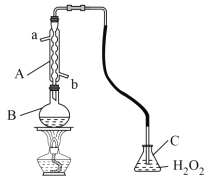
ʵ�鲽�����£���B�м���300.00mL���Ѿƺ��������ᣬ����ʹSO2ȫ���ݳ�����C��H2O2��ȫ��Ӧ����ȥC��ʣ���H2O2����0.0900mol��L-1NaOH��Һ�ⶨ��Ӧ���ɵ��ᣬ����NaOH��Һ25.00mL��
��1��C��ͨ��SO2������Ӧ�Ļ�ѧ����ʽΪ___��
��2��ͨ��������������Ѿ���SO2�ĺ���(��g��L-1Ϊ��λ����ÿ�����Ѿ��к���SO2������) ___��(д���������)
��3���òⶨ�����ʵ��ֵƫ�ߣ����ܵ�ԭ����____����Դ�ԭ�����һ���Ľ���ʩ��___��
���𰸡�SO2+H2O2=H2SO4 0.24 g/L �����ӷ������Ȼ������װ��C�� B���ò��ӷ���ǿ���������������
��������
(1)����������л�ԭ�ԣ��ܹ���˫��ˮ��Ӧ�������ᣬ�ݴ�д����Ӧ�Ļ�ѧ����ʽ��
(2)���ݹ�ϵʽ2NaOH��H2SO4��SO2���������Ƶ����ʵ������������������������ټ���������Ѿ��еĶ�����������
(3)�����ǻӷ����ᣬ�ӷ����������������ƣ��ݴ˷������
(1)˫��ˮ���������ԣ��ܹ��������������������ᣬ��Ӧ�Ļ�ѧ����ʽΪ��SO2+H2O2=H2SO4���ʴ�Ϊ��SO2+H2O2=H2SO4��
(2)����2NaOH��H2SO4��SO2��֪SO2������Ϊ��![]() ��(0.0900mol/L��0.025L)��64g/mol=0.072g�������Ѿ��еĶ���������Ϊ��
��(0.0900mol/L��0.025L)��64g/mol=0.072g�������Ѿ��еĶ���������Ϊ��![]() =0.24g/L���ʴ�Ϊ��0.24 g/L��
=0.24g/L���ʴ�Ϊ��0.24 g/L��
(3)���������ǻӷ����ᣬ�ӷ������ܹ������������ƣ�ʹ�����ĵ�����������Һ������ⶨ���ƫ�ߣ���˿����ò��ӷ���ǿ�ᣬ������������ᣬ�ʴ�Ϊ�������ӷ������Ȼ������װ��C�У�B���ò��ӷ���ǿ��������������ᡣ


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС���ͬѧ��һ��������Ʒ(�������ʣ����ʲ�����ˮ��Ҳ����ϡ���ᷴӦ)���з������ס��ҡ�����λͬѧ�ֱ����ʵ�飬����һλͬѧ���õ�ϡ����������Ʒǡ����ȫ��Ӧ��ʵ���������±���
�� | �� | �� | |
�ձ�+ϡ���������/g | 200 | 150 | 150 |
����������Ʒ������/g | 9 | 9 | 14 |
��ַ�Ӧ���ձ�+ʣ���������/g | 208.7 | 158.7 | 163.7 |
��������������ݣ��ش��������⣺
��1����λͬѧ���õ�ϡ������������Ʒǡ����ȫ��Ӧ_____��
��2������������Ʒ��������������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ������������������й㷺���ڡ�
��1�������ǽ�1mol�����������AB��Ϊ������̬ԭ��A��B�������������֪���л�ѧ���ļ������±���
![]()
д��1mol��̬��(H2N-NH2)ȼ�����ɵ�����ˮ�������Ȼ�ѧ����ʽ________________��
��2���ý�̿��ԭNO�ķ�ӦΪ��2NO(g)+C(s)![]() N2(g)+CO2(g)�����ݻ���Ϊ1L�ļס��ҡ����������ݺ���(��Ӧ�¶ȷֱ�Ϊ400�桢400�桢T��)�����зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
N2(g)+CO2(g)�����ݻ���Ϊ1L�ļס��ҡ����������ݺ���(��Ӧ�¶ȷֱ�Ϊ400�桢400�桢T��)�����зֱ���������Ľ�̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��

�ٸ÷�ӦΪ________(��������������������)��Ӧ��
����������60minʱ�ﵽƽ��״̬����0��60min����NO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(NO)=____________��
��3���ý�̿��ԭNO2�ķ�ӦΪ��2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)���ں��������£�1molNO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)���ں��������£�1molNO2������C�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��

��A��C�����Ũ��ƽ�ⳣ����ϵ��Kc(A)________Kc(C)(����<������>������=��)��
��A��B��C������NO2��ת������ߵ���________(����A������B������C��)�㡣
�ۼ���B��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp(B)=________(Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ρ������ڹ�ũҵ�����������ˮ�����ȷ������ż���㷺��Ӧ�ã�������м�����ᷴӦ�Ʊ�����������
��֪����4Fe2����O2��4H��===4Fe3����2H2O
������������ˮ�е��ܽ������ͼ��
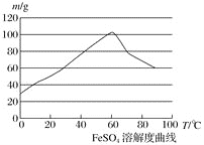
(1)���ȣ�����м����̼������Һ����г����ۣ������Һ�壬��ˮϴ����м���˲����У������Һ��ķ���ͨ�����ù��ˣ�ʹ�õIJ�����____________(��д��������)��
(2)����������м�м������������ᣬ��һ���¶���ʹ�䷴Ӧ�����ٲ������壬���ȹ��ˣ�������������Һ��
������Ũ��Ӧѡ��(����ĸ���)__________����������������������������������������
A��Ũ���� B��10 moL��L��1����
C��3 moL��L��1���� D������Ũ������
���¶��˿�����________�����ȵ�ͬʱ���ʵ�����ˮ��ԭ����___________________��
�۷�Ӧ��Ӧ����![]() _________ (���������������) 1��
_________ (���������������) 1��
(3)�������ڿ������ױ����������γɸ��ο��ȶ����ڣ��硰Ħ���Ρ�����(NH4)2SO4��FeSO4��6H2O(���������)������������������Һ�м�������ϡ������Һ���ټ��뱥���������Һ������_______��_______��_______��_______��һϵ�в��������á�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��25ʱ�棬0.2 mol/L��HF��Һ�д�������ƽ�⣺HF![]() H++F-����һ����������ˮ��ƽ�⽫____���������������������������������ƶ�����Һ�е�c(H+)��___������������������С������������������������0.2mol/L�����ᣬ��___�������ٽ���������������HF�ĵ��룬HF�ĵ���ƽ�ⳣ��K��___������������������С����������������
H++F-����һ����������ˮ��ƽ�⽫____���������������������������������ƶ�����Һ�е�c(H+)��___������������������С������������������������0.2mol/L�����ᣬ��___�������ٽ���������������HF�ĵ��룬HF�ĵ���ƽ�ⳣ��K��___������������������С����������������
��2�������������ڵ���ʵ���____�����ڷǵ���ʵ���____���ܵ����������____����ˮ��Һ�ܹ����������____��
��CO2 ��ͭ ���ռ� ��NH3.H2O ��ʯī ��̼���� ��CH3COOH ������ ������ ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�����õ绯ѧԭ�����͵��ǣ�������
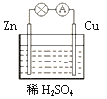
A.�ɽ��������ֹ������ֱ����Դ�ĸ��������Ա����ֹܲ��ܸ�ʴ
B.���������£����ڿ����в��ױ���ʴ
C.�Ʋ��ƻ���������п������������������������������ʴ
D.��п��ϡ���������ʱ����ϡ�����е���������ͭ��Һ�ܼӿ췴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȷ��ȡ6.0 g��������Ʒ(��Ҫ�ɷ�ΪAl2O3,��Fe2O3����)������100 mLϡ�����У���ַ�Ӧ������Һ�м���10 mol��L��1NaOH��Һ�����������������ͼ���NaOH��Һ���֮��Ĺ�ϵ��ͼ��ʾ���������������ʵ���Ũ��Ϊ�� ��

A. 3.50 mol��L��1
B. 1.75 mol��L��1
C. 0.85 mol��L��1
D. ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1molN2�����3molH2������2L�ĺ��������У�����һ�������·������·�Ӧ��N2(g)+3H2(g) ![]() 2NH3(g)������2s����NH3��Ũ��Ϊ0.6mol��L-1���������м���˵�������в���ȷ����
2NH3(g)������2s����NH3��Ũ��Ϊ0.6mol��L-1���������м���˵�������в���ȷ����
A. ��N2��ʾ�ķ�Ӧ����Ϊ0.15mol��L-1��s-1 B. 2sʱH2��ת����Ϊ40��
C. 2sʱN2��H2��ת������� D. 2sʱH2��Ũ��Ϊ0.6mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ͨ�����ijɷ�ΪNa2O��13%��CaO��11.7%��SiO2��75.3%��ij����������ʯ��ʯ500 t������2 400 t����������ԭ����������ͨ����_________�֣�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com