
科目: 来源: 题型:
【题目】亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性。
(1).写出亚硒酸电离方程式_______________________。
(2).将亚硒酸与高锰酸钾共热可制得硒酸(H2SeO4),配平该反应方程式___,并用单线桥法标出电子转移的方向和数目___。
H2SeO3 + KMnO4 → K2SeO4+ MnSeO4+ H2SeO4+
与硫同族的元素Te,最高价氧化物的水化物碲酸(H6TeO6)的酸性比H2SO4______(选填“强”或“弱”),其氧化性比硫酸强。
向碲酸中通入SO2气体,若反应中生成的TeO2与Te的物质的量之比为2:1,写出该反应的化学方程式_________________。当6mol碲酸与一定量SO2恰好完全反应,所得溶液体积为20L,则所得溶液的pH为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 时,相同pH的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示。下列说法正确的是( )
时,相同pH的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示。下列说法正确的是( )
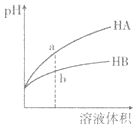
A.水的电离程度:a点小于b点
B.a点溶液的导电性大于b点溶液
C.恰好完全中和时,所需NaOH物质的量:![]()
D.HA的酸性强于HB
查看答案和解析>>
科目: 来源: 题型:
【题目】在“绿色化学工艺”中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子利用率为100%——即“原子经济性”。下列反应能体现原子经济性的是( )
A. CH3CH3+Br2![]() CH3CH2Br + HBr
CH3CH2Br + HBr
B. CH2=CH2+Br2![]() CH2BrCH2Br
CH2BrCH2Br
C. CH3CH2Br+NaOH![]() CH2=CH2+NaBr+H2O
CH2=CH2+NaBr+H2O
D. CH3CH2OH+CH3COOH![]() H2O+CH3COOCH2CH3
H2O+CH3COOCH2CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的原子经济性反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放。下列几种生产乙苯的方法中,最符合原子经济性要求的是(反应均在一定条件下进行)( )
A.![]() +C2H5OH
+C2H5OH![]()
![]() +HCl
+HCl
B.![]() +C2H5OH
+C2H5OH![]()
![]() +H2O
+H2O
C.![]() +CH2=CH2
+CH2=CH2![]()
![]()
D.![]() +NaH
+NaH![]()
![]() +NaBr
+NaBr
查看答案和解析>>
科目: 来源: 题型:
【题目】I.工业上可由氢气、氮气合成氨气,溶于水形成氨水。盐酸和氨水是实验室常见的电解质溶液。一定温度下,向2L 密闭容器中加入N2(g) 和H2(g),发生反应:N2(g)+3H2(g)2NH3(g) △H=—Q kJ/mol(Q>0),NH3物质的量随时间的变化如图所示。
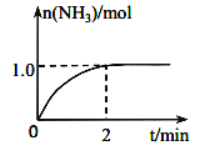
(1)0到2 min 内的平均反应速率 v(H2)=________。
(2)该温度下,反应 N2(g)+3H2(g)![]() 2NH3(g) △H = —Q kJ/mol(Q>0)的平衡常数表达式K=________________。其平衡常数K与温度T的关系如下表:
2NH3(g) △H = —Q kJ/mol(Q>0)的平衡常数表达式K=________________。其平衡常数K与温度T的关系如下表:
T/ ℃ | 25 | 125 | 225 |
平衡常数 K | 4×106 | K1 | K2 |
试判断K1_______K2(填写“>”“=”或“<”)。
(3)若反应是在固定体积的密闭容器中进行,下列能说明合成氨反应已达到平衡状态的是___(填字母)
A.3v(N2) = v(H2)
B.容器内压强保持不变
C.混合气体的密度保持不变
D.25℃时,测得容器中c(NH3)=0.2 mol·L-1, c(H2) =c(N2) =0.01 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念.在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得产物,即原子的利用率为100%.在用丙炔合成甲基丙烯酸甲酯![]() 的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是
的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是
A. CH2=CH2和CO B. CO和CH3OH C. CH3OH和H2 D. CO2和H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以食盐、氨气、二氧化碳等物质为原料制取纯碱。
(1)实验室提纯粗盐的一个重要环节是除去粗盐水中的杂质阳离子(主要含Ca2+、Mg2+),提纯该粗盐时,可考虑在粗盐水中依次加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。A____ 、B_____。
(2)氨气分子的空间构型为_____,其中N原子采用_____杂化方式,二氧化碳中心原子C采用_____杂化方式。
(3)上述实验涉及的元素中,Ca基态原子电子排布式为__________________。
(4)上述实验涉及的元素中,O2-、Na+、Cl-中半径最小的是__________。
(5)制取纯碱时,向饱和食盐水中通入气体,即可得到小苏打的沉淀物,氨气与二氧化碳通入的先后顺序是:_________,因为:___________
(6)写成工业上以食盐、氨气、二氧化碳等物质为原料制取小苏打反应的化学方程式:______
查看答案和解析>>
科目: 来源: 题型:
【题目】下列粒子在相应条件下可大量共存的是( )
A.0.1 mol·L-1FeCl3溶液中:K+、Na+、SO![]() 、AlO
、AlO![]()
B.![]() =1的溶液中:Fe2+、NO
=1的溶液中:Fe2+、NO![]() 、Al3+、Cl-
、Al3+、Cl-
C.0.1 mol·L-1盐酸的澄清透明溶液中:Fe3+、K+、SO![]() 、Br-
、Br-
D.含有0.1 mol·L-1Ca2+的溶液中:Na+、Cu2+、SiO![]() 、NO
、NO![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是

A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.为保护好环境,工业生产应从源头上减少或尽量消除生产对环境的污染
B.在某爆炸事故救援现场,消防员发现存放金属钠、电石、甲苯二异氰酸酯 等化学品的仓库起火,应立即用泡沫灭火器将火扑灭
C.世界卫生组织认为青蒿素(结构如图所示)联合疗法是当下治疗疟疾最 有效的手段,已经拯救了上百万生命,靑蒿素属于烃类物质
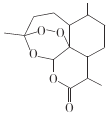
D.某品牌化妆品在广告中反复强调:“十年专注自然护肤”,该产品中不含任何化学成分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com