
ЁОЬтФПЁПбЧЮјЫс(H2SeO3)вВЪЧвЛжжЖўдЊШѕЫсЃЌГЃЮТЯТЪЧвЛжжЮоЩЋЙЬЬхЃЌвзШмгкЫЎЃЌгаНЯЧПЕФбѕЛЏадЁЃ
(1).аДГібЧЮјЫсЕчРыЗНГЬЪН_______________________ЁЃ
(2).НЋбЧЮјЫсгыИпУЬЫсМиЙВШШПЩжЦЕУЮјЫс(H2SeO4)ЃЌХфЦНИУЗДгІЗНГЬЪН___ЃЌВЂгУЕЅЯпЧХЗЈБъГіЕчзгзЊвЦЕФЗНЯђКЭЪ§ФП___ЁЃ
H2SeO3 + KMnO4 Ёњ K2SeO4+ MnSeO4+ H2SeO4+
гыСђЭЌзхЕФдЊЫиTeЃЌзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяэкЫс(H6TeO6)ЕФЫсадБШH2SO4______(бЁЬюЁАЧПЁБЛђЁАШѕЁБ)ЃЌЦфбѕЛЏадБШСђЫсЧПЁЃ
ЯђэкЫсжаЭЈШыSO2ЦјЬхЃЌШєЗДгІжаЩњГЩЕФTeO2гыTeЕФЮяжЪЕФСПжЎБШЮЊ2ЃК1ЃЌаДГіИУЗДгІЕФЛЏбЇЗНГЬЪН_________________ЁЃЕБ6molэкЫсгывЛЖЈСПSO2ЧЁКУЭъШЋЗДгІЃЌЫљЕУШмвКЬхЛ§ЮЊ20LЃЌдђЫљЕУШмвКЕФpHЮЊ______ЁЃ
ЁОД№АИЁПH2SeO3HSeO![]() + H+ 5ЁЂ2ЁЂ1ЁЂ2ЁЂ2ЁЂ3H2O
+ H+ 5ЁЂ2ЁЂ1ЁЂ2ЁЂ2ЁЂ3H2O  Шѕ 5SO2 + 3H6TeO6 = 2TeO2 + Te +5H2SO4+ 4H2O 0
Шѕ 5SO2 + 3H6TeO6 = 2TeO2 + Te +5H2SO4+ 4H2O 0
ЁОНтЮіЁП
(1)бЧЮјЫсЪЧвЛжжЖўдЊШѕЫсЃЌжївЊвдЕквЛВНЕчРыЮЊжїЃЌЕчРыЗНГЬЪНЮЊH2SeO3HSeO![]() + H+ЃЛ
+ H+ЃЛ
(2) SeЕФЛЏКЯМлгЩ+4Щ§ИпЕН+6ЃЌMnЕФЛЏКЯМлгЩ+7НЕЕЭЕН+2ЃЌИљОнЛЏКЯМлЩ§НЕЪиКуЃЌРћгУзюаЁЙЋБЖЪ§ЗЈЃЌH2SeO3ЛЏбЇМЦСПЪ§ЮЊ5ЃЌKMnO4ЛЏбЇМЦСПЪ§ЮЊ2ЃЌдйИљОндзгЪиКуЃЌНјааХфЦНЃЌЕУЗНГЬЪНЮЊ5H2SeO3 +2KMnO4=1K2SeO4+2MnSeO4+2H2SeO4+3H2OЃЛЕЅЯпЧХБэЪОЪБЃЌH2SeO3ЛЏКЯМлЩ§ИпЃЌЪЇШЅЕчзгЃЌKMnO4ЛЏКЯМлНЕЕЭЃЌЕУЕчзгЃЌMnЕФЛЏКЯМлгЩ+7НЕЕЭЕН+2ЃЌЫљвдУПИіMnЕУ5ИіЕчзгЃЌ2ИіKMnO4ЕУ10ИіЕчзгЃЌМДЕЅЯпЧХБэЪОЮЊ ЃЛ
ЃЛ
ЭЌжїзхДгЩЯЕНЯТЃЌЗЧН№Ъєадж№НЅМѕШѕЃЌдђЗЧН№ЪєадTe<SЃЌЗЧН№ЪєаддНШѕЦфзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяЫсаддНШѕЃЌЫљвдЫсадH6TeO6БШH2SO4ШѕЃЛ
ЯђэкЫсжаЭЈШыSO2ЦјЬхЃЌSO2БЛбѕЛЏГЩH2SO4ЃЌИљОнH6TeO6ЩњГЩЕФTeO2гыTeЕФЮяжЪЕФСПжЎБШЮЊ2ЃК1ЃЌИљОнЛЏКЯМлЩ§НЕЪиКуКЭдзгЪиКуЃЌЕУЕНЛЏбЇЗНГЬЪНЮЊ5SO2 + 3H6TeO6 = 2TeO2 + Te +5H2SO4+ 4H2OЃЛИљОнЛЏбЇЗНГЬЪНЃЌ6molэкЫсгывЛЖЈСПSO2ЧЁКУЭъШЋЗДгІЃЌЩњГЩH2SO4ЮЊ10molЃЌЫљЕУШмвКH2SO4ЕФХЈЖШЮЊ![]() ЃЌЧтРызгХЈЖШЮЊ2ЁС0.5mol/L=1mol/LЃЌpHЮЊ0ЁЃ
ЃЌЧтРызгХЈЖШЮЊ2ЁС0.5mol/L=1mol/LЃЌpHЮЊ0ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПН№ЪєюбвђОпгаЧПЖШИпЁЂФЭЪДадКУЁЂФЭШШадИпЕШЬиЕуЖјБЛЙуЗКгУгкИїИіСьгђЁЃ
(1)ЛљЬЌ Ti дзгКЫЭтЕчзгХХВМЕФзюИпФмМЖЗћКХЪЧ____ЁЃгыюбЭЌжмЦкЕФдЊЫижаЛљЬЌдзгЮДГЩЖдЕчзгЪ§гыюбЯрЭЌЕФга__________жжЁЃ
(2)юбБШИжЧсЃЌБШТСгВЃЌЪЧвЛжжаТаЫЕФНсЙЙВФСЯЁЃюбгВЖШБШТСДѓЕФдвђЪЧ_____ЁЃ
(3)АыМааФНсЙЙДпЛЏМС M ЦфНсЙЙШчЭМЫљЪОЃК
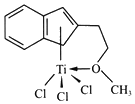
ЂйзщГЩИУЮяЕФжЪдЊЫижаЃЌЕчИКадзюДѓЕФЪЧ___________(ЬюдЊЫиЗћКХ)
ЂкMжаВЛКЌ_________(ЬюБъКХ)
a.ІаМќ b.ІвМќ c.ХфЮЛМќ d.РызгМќ e.ЧтМќ
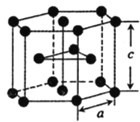
(4)TiO2ФмШмгкХЈСђЫсВЂЮіГівЛжжРызгОЇЬхЃЌвбжЊЦфжабєРызгЪЧвдСДзДОлКЯЮяаЮЪНДцдкЕФюбѕЃбєРызгЃЌЦфНсЙЙШчЭМЫљЪОЃЌЦфЛЏбЇЪНЪЧ______ аДГівЛжжгывѕРызг![]() ЛЅЮЊЕШЕчзгЬхЕФЗжзг______ ЁЃ
ЛЅЮЊЕШЕчзгЬхЕФЗжзг______ ЁЃ

(5)юбЕЅжЪЕФОЇАћШчЭМЫљЪОЃЌИУОЇАћЮЊ______ЖбЛ§(ЬюЖбЛ§ЗНЪН)ЃЌюбдзгЕФХфЮЛЪ§ЪЧ_______ЃЌЫШжЊОЇАћВЮЪ§ЃКa=0.295nmЃЌc=0.469nmЁЃдђИУюбОЇЬхЕФУмЖШЮЊ___________gЁЄcm-3(NAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФЪ§жЕЃЌСаГіМЦЫуЪНМДПЩ)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбаОПадбЇЯАаЁзщгћВтЖЈЪвЮТЯТ(25ЁцЁЂ101kPa)ЕФЦјЬхФІЖћЬхЛ§ЃЌЧыЛиД№вдЯТЮЪЬтЁЃИУаЁзщЩшМЦЕФМђвзЪЕбщзАжУШчЭМЫљЪОЃК
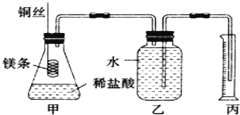
ИУЪЕбщЕФжївЊВйзїВНжшШчЯТЃК
ЂйгУвбжЊХЈЖШЕФХЈбЮЫсХфжЦ100mL 1.0mol/LЕФбЮЫсШмвКЃЌашвЊгУЕНЕФвЧЦїгаСПЭВЁЂЩеБЁЂВЃСЇАєЁЂНКЭЗЕЮЙмЁЂ______ЃЛ
ЂкгУ10mLСПЭВСПШЁ8.0mL 1.0mol/LЕФбЮЫсШмвКМгШызЖаЮЦПжаЃЛ
ЂлзМШЗГЦШЁa gвбГ§ШЅБэУцбѕЛЏФЄЕФУОЬѕЃЌВЂЯЕгкЭЫПФЉЖЫЃЌЮЊЪЙHClШЋВПВЮМгЗДгІЃЌaЕФЪ§жЕжСЩйЮЊ______ЃЛ
ЂмЭљЙуПкЦПжазАШызуСПЫЎЃЌАДЩЯЭМСЌНгКУзАжУЃЌМьВщзАжУЕФЦјУмадЃЛ
ЂнЗДгІНсЪјКѓД§ЬхЯЕЮТЖШЛжИДЕНЪвЮТЃЌКіТдЕМЙмжаЕФЫЎЃЌЖСГіСПЭВжаЫЎЕФЬхЛ§ЮЊVmLЁЃ
ЧыЛиД№ЯТСаЮЪЬтЁЃ
(1)ВНжшЂйжаЃЌХфжЦ100mL 1.0mol/LЕФбЮЫсШмвКЪБЃЌЯТСаФФаЉВйзїЛсЪЙХфжЦХЈЖШЦЋЕЭ_____(ЬюаДзжФИ)
A. гУСПЭВСПШЁХЈбЮЫсЪБЃЌИЉЪгСПЭВЕФПЬЖШ
B. ШнСПЦПЮДИЩдяМДгУРДХфжЦШмвК
C. ЮДЯДЕгЩеБКЭВЃСЇАє
D.ЖЈШнЭъГЩКѓЃЌНЋШнСПЦПЕЙжУвЁдШКѓЃЌЗЂЯжвКУцЕЭгкПЬЖШЯп
E.дкШнСПЦПжаЖЈШнЪБИЉЪгШнСПЦППЬЖШЯп
(2)ЧыЬюаДВйзїВНжшжаЕФПеИёЃКВНжшЂй__________ЁЁВНжшЂл__________
(3)ЪЕбщВНжшЂнжагІбЁгУ________ЕФСПЭВ(ЬюзжФИ).
A.100mLЁЁЁЁЁЁЁЁЁЁB.200mLЁЁЁЁЁЁЁЁЁЁC.500mL
(4)ЖСЪ§ЪБашвЊзЂвт(жСЩйаДСНЕу)____________
(5)КіТдЫЎеєЦјгАЯьЃЌдкИУЬѕМўЯТВтЕУЦјЬхФІЖћЬхЛ§ЮЊVm=____L/molЁЃ(гУКЌVЕФЪНзгБэЪО)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЁАТЬЩЋЛЏбЇЁБЕФРэЯызДЬЌЪЧЗДгІЮяЕФдзгШЋВПзЊЛЏЮЊФПБъВњЮяЁЃвдЯТЗДгІВЛЗћКЯТЬЩЋЛЏбЇддђЕФЪЧЃЈ ЃЉ
A.ЙЄвЕЩњВњЛЗбѕввЭщЃК![]()
B.ЫЎУКЦјКЯГЩМзДМЃКCO + 2H2 CH3OH
CH3OH
C.жЦШЁСђЫсЭЃКCu + 2H2SO4ЃЈХЈЃЉ![]() CuSO4 + SO2Ёќ+ 2H2O
CuSO4 + SO2Ёќ+ 2H2O
D.КЯГЩМзЛљБћЯЉЫсМзѕЅЃКCH3CЁдCH + CO + CH3OH![]() CH2=CЃЈCH3ЃЉCOOCH3
CH2=CЃЈCH3ЃЉCOOCH3
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЁАТЬЩЋЛЏбЇЁБЪЧЕБНёЩчЛсЬсГіЕФвЛИіаТИХФюЃЎдкЁАТЬЩЋЛЏбЇЙЄвеЁБжаЃЌРэЯызДЬЌЪЧЗДгІжадзгШЋВПзЊЛЏЮЊгћжЦЕУВњЮяЃЌМДдзгЕФРћгУТЪЮЊ100%ЃЎдкгУБћШВКЯГЩМзЛљБћЯЉЫсМзѕЅ![]() ЕФЙ§ГЬжаЃЌгћЪЙдзгЕФРћгУТЪДяЕНзюИпЃЌдкДпЛЏМСзїгУЯТЛЙашвЊЦфЫћЕФЗДгІЮяЪЧ
ЕФЙ§ГЬжаЃЌгћЪЙдзгЕФРћгУТЪДяЕНзюИпЃЌдкДпЛЏМСзїгУЯТЛЙашвЊЦфЫћЕФЗДгІЮяЪЧ
A. CH2=CH2КЭCO B. COКЭCH3OH C. CH3OHКЭH2 D. CO2КЭH2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП2018Фъ5дТУРЙњбаОПШЫдБГЩЙІЪЕЯждкГЃЮТГЃбЙЯТгУЕЊЦјКЭЫЎЩњВњАБЃЌдРэШчЯТЭМЫљЪОЃК
ЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ

A. ЭМжаФмСПзЊЛЏЗНЪНжЛга2жж
B. H+ЯђaМЋЧјвЦЖЏ
C. bМЋЗЂЩњЕФЕчМЋЗДгІЮЊЃКN2+6H++6eЃ=2NH3
D. aМЋЩЯУПВњЩњ22.4LO2СїЙ§ЕчМЋЕФЕчзгЪ§вЛЖЈЮЊ4ЁС6.02ЁС1023
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪЕбщНсЙћВЛФмзїЮЊЯргІЖЈТЩЛђдРэЕФжЄОнжЎвЛЕФЪЧЃЈ ЃЉ
ЃЈАЂЗќМгЕТТоЖЈТЩЃКдкЭЌЮТЭЌбЙЯТЃЌЯрЭЌЬхЛ§ЕФШЮКЮЦјЬхКЌгаЯрЭЌЪ§ФПЕФЗжзгЃЉ
A | B | C | D | |
РеЯФЬиСадРэ | дЊЫижмЦкТЩ | ИЧЫЙЖЈТЩ | АЂЗќйЄЕТТоЖЈТЩ | |
ЪЕбщЗНАИ |
|
|
|
|
НсЙћ | зѓЧђЦјЬхбеЩЋМгЩю гвЧђЦјЬхбеЩЋБфЧГ | ЩеЦПжаУАЦјХн ЪдЙмжаГіЯжЛызЧ | ВтЕУ |
|
A. AB. BC. CD. D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгЩ![]() єЧЛљЖЁЫсЩњГЩ
єЧЛљЖЁЫсЩњГЩ![]() ЖЁФкѕЅЕФЗДгІШчЯТЃКHOCH2CH2CH2COOH
ЖЁФкѕЅЕФЗДгІШчЯТЃКHOCH2CH2CH2COOH![]() +H2O
+H2O
дк298KЯТЃЌ![]() єЧЛљЖЁЫсЫЎШмвКЕФГѕЪМХЈЖШЮЊ
єЧЛљЖЁЫсЫЎШмвКЕФГѕЪМХЈЖШЮЊ![]() ЃЌВтЕУ
ЃЌВтЕУ![]() ЖЁФкѕЅЕФХЈЖШЫцЪБМфБфЛЏЕФЪ§ОнШчБэЫљЪОЁЃЛиД№ЯТСаЮЪЬтЃК
ЖЁФкѕЅЕФХЈЖШЫцЪБМфБфЛЏЕФЪ§ОнШчБэЫљЪОЁЃЛиД№ЯТСаЮЪЬтЃК
| 21 | 50 | 80 | 100 | 120 | 160 | 220 |
|
| 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
(1)ИУЗДгІдк50ЁЋ80minФкЕФЦНОљЗДгІЫйТЪЮЊ_____![]() ЁЃ
ЁЃ
(2)120minЪБ![]() єЧЛљЖЁЫсЕФзЊЛЏТЪЮЊ______ЁЃ
єЧЛљЖЁЫсЕФзЊЛЏТЪЮЊ______ЁЃ
(3)298KЪБИУЗДгІЕФЦНКтГЃЪ§![]() _____ЁЃ
_____ЁЃ
(4)ЮЊЬсИп![]() єЧЛљЖЁЫсЕФЦНКтзЊЛЏТЪЃЌГ§ЪЪЕБПижЦЗДгІЮТЖШЭтЃЌЛЙПЩВЩШЁЕФДыЪЉЪЧ______ЁЃ
єЧЛљЖЁЫсЕФЦНКтзЊЛЏТЪЃЌГ§ЪЪЕБПижЦЗДгІЮТЖШЭтЃЌЛЙПЩВЩШЁЕФДыЪЉЪЧ______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊШШЛЏбЇЗНГЬЪНЃКдђЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЂйCOЃЈgЃЉ+![]() O2ЃЈgЃЉЃНCO2ЃЈgЃЉ ІЄH=Ѓ283.0kJЁЄmol-1
O2ЃЈgЃЉЃНCO2ЃЈgЃЉ ІЄH=Ѓ283.0kJЁЄmol-1
ЂкH2ЃЈgЃЉ+![]() O2ЃЈgЃЉЃНH2OЃЈgЃЉ ІЄH=Ѓ241.8kJЁЄmol-1
O2ЃЈgЃЉЃНH2OЃЈgЃЉ ІЄH=Ѓ241.8kJЁЄmol-1

A. H2ЕФШМЩеШШЮЊ241.8kJЁЄmol-1
B. гЩЗДгІЂйЁЂЂкПЩжЊШчЭМЫљЪОЕФШШЛЏбЇЗНГЬЪНЮЊCOЃЈgЃЉ+H2OЃЈgЃЉ=CO2ЃЈgЃЉ+H2ЃЈgЃЉ ІЄH =Ѓ41.2kJЁЄmol-1
C. H2ЃЈgЃЉзЊБфГЩH2OЃЈgЃЉЕФЛЏбЇЗДгІвЛЖЈвЊЪЭЗХФмСП
D. ИљОнЂкЭЦжЊЗДгІH2ЃЈgЃЉ +1/2O2ЃЈgЃЉЃНH2OЃЈlЃЉЃКІЄHЃОЃ241.8 kJЁЄmol-1
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com