
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列说法不正确的是 ( )
A.25℃、101Kpa时,64g SO2中含有的原子数为3NA
B.常温常压下,1mol氢气含有的原子数为2NA
C.在标准状况下,11.2L H2O含有的分子数0.5NA
D.5.6g金属铁与足量盐酸反应,失去的电子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。
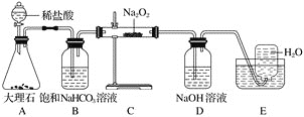
(1)A装置为CO2的发生装置,反应的离子方程式为____________________。
(2)B装置可除去A装置中可能挥发出的___________,反应的离子方程式为_______________。
(3)C装置为O2的发生装置,反应的化学方程式为__________________、________________。
(4)D装置可除去C装置中未反应的__________,反应的离子方程式为____________________。
(5)E装置为排水法收集O2的装置,检验所收集的气体为O2的方法为_____________________。
(6)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为取少量C装置中反应后的固体溶于水,向溶液中滴入过量___溶液,若有白色沉淀生成,则证明固体中含有___;过滤,向滤液中滴入几滴酚酞溶液,若__且不褪色,则证明固体中含有__。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.在标准状况下,78.0 g苯中含有碳碳双键的数目为3NA
B.22.4 L(标准状况)氩气含有的质子数为18NA
C.在标准状况下,2.24 L CHCl3中所含碳氢键的数目为0.1NA
D.0.1 molL-1的Na2CO3溶液中,![]() 的数目小于0.1NA
的数目小于0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】对于放热反应Zn+H2SO4=ZnSO4+H2↑,下列叙述正确的是( )

A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则其能量转化形式为电能转化为化学能
D. 若将其设计为原电池,当有32.5gZn溶解时,正极放出的气体一定为11.2L.
查看答案和解析>>
科目: 来源: 题型:
【题目】根据热化学方程式N2(g)+3H2(g)![]() 2NH3(g)+92kJ,下列有关图像和叙述中正确的是
2NH3(g)+92kJ,下列有关图像和叙述中正确的是
A.  B.
B. 
C. 向密闭容器中通入1mol氮气和3mol氢气发生反应放出92kJ的热量D. 形成1mol氮氮键和3mol氢氢键所放出的能量比拆开6mol氮氢键所吸收的能量多92kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】诺贝尔奖获得者屠呦呦带领团队发现了青蒿素,为中国医药科技创新和人类健康事业作出了巨大贡献,我国化学家在确认青蒿素分子结构后实现了青蒿素的全合成。一种以香茅醛为原料合成青蒿素的流程如图:
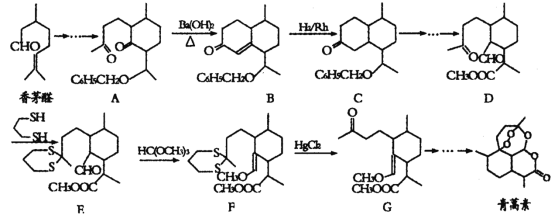
已知:羰基α—H可发生反应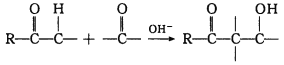
回答下列问题:
(1)青蒿素的分子式为__。根据青蒿素所含官能团,推测其可能具有的性质有___。
a.易溶于水 b.具有氧化性 c.可发生水解反应
(2)香茅醛的同分异构体X含有醛基和六元碳环,且环上只有一个支链,满足上述条件的X有__种,其中核磁共振氢谱峰数最少的物质结构简式为__。
(3)反应A→B实际上可看作两步进行,依次发生的反应类型是__、__。
(4)C中所含官能团名称为__。
(5)通过D→E的反应,分子中引入了硫醚基团,而F→G的反应,分子中硫醚基团又被脱去,这样做的目的是__。
(6)写出由苯甲醛和氯乙烷为原料,制备苄基乙醛(![]() )的合成路线流程__(无机试剂任选)。
)的合成路线流程__(无机试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法一定正确的是
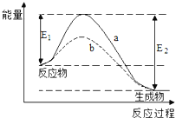
A. 该反应为吸热反应
B. a与b相比,a的反应速率更快
C. a与b相比,反应的平衡常数一定不同
D. 反应物吸收的总能量小于生成物释放的总能量
查看答案和解析>>
科目: 来源: 题型:
【题目】已知拆开1molH2(g)中的H-H键需要消耗436kJ能量,如图反应3H2(g)+N2(g) ![]() 2NH3(g)的能量变化示意图.下列说法不正确的是
2NH3(g)的能量变化示意图.下列说法不正确的是

A. 断开1 mol N2(g)中的N![]() N键要吸收941 kJ能量
N键要吸收941 kJ能量
B. 生成2mol NH3(g)中的N-H键吸收2346 kJ能量
C. 3H2(g) + N2(g) ![]() 2NH3(g) △H=-97
2NH3(g) △H=-97![]()
D. NH3(g) ![]() 3/2H2(g) +1/2 N2(g) △H=48.5
3/2H2(g) +1/2 N2(g) △H=48.5 ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O,M=392g·mol-1],俗称莫尔盐,是一种蓝绿色的无机复盐,易溶于水,在100℃~110℃时分解。
回答下列问题:
Ⅰ.探究莫尔盐强热时的分解产物
某同学认为莫尔盐分解的产物中可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,该同学用下列装置进行实验。
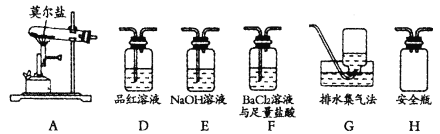
(1)该同学的实验中,装置依次连接的合理顺序为A→H→___→G。
(2)证明分解产物中含有SO3的实验现象是__。
Ⅱ.探究莫尔盐的纯度
某学生取mg莫尔盐样品配制成500mL溶液,根据物质组成,分别设计了如下实验方案。
方案甲:取20.00mL所配溶液于锥形瓶,用0.1000mol·L-1的酸性KMnO4溶液进行滴定。
方案乙:取20.00mL所配溶液进行如下实验。
![]()
(3)方案甲中盛装标准溶液的仪器名称为__;涉及反应的离子方程式为__;达到滴定终点的现象是___。
(4)方案乙测得样品的纯度为__%(用含m、w的式子表示)。
(5)若实验操作都正确,但方案甲的测定结果总是小于方案乙,其可能原因为__。设计实验,验证你的假设__。
查看答案和解析>>
科目: 来源: 题型:
【题目】硼化镁是迄今发现的临界温度最高的简单的金属化合物超导材料。回答下列问题:
(1)基态硼的电子排布图为__,基态镁原子的电子运动状态有__种。
(2)BF3的键角(填“大于”、“小于”或“等于”)__NF3的键角,理由是__。
(3)碱土金属的碳酸盐热分解反应模式为:MCO3(s)=MO(s)+CO2(g)。从结构的角度解释:MgCO3的热分解温度小于CaCO3的热分解温度的原因是__。
(4)已知硼化镁属六方晶系(如图1所示)a=b≠c,α=β=90°,γ=120°。又知硼化镁是一种插层型离子化合物,镁层和硼层交替排列;镁原子层呈三角形结构,硼原子层具有规则的六角蜂房结构,与石墨相似。硼化镁晶体沿z轴方向的投影如图2所示,黑球代表硼原子,白球代表镁原子。硼化镁的化学式为__;B的配位数是__。

(5)已知硼化镁的晶格常数为:a=b=0.3086nm,c=0.3524nm,则硼化镁晶体的密度表达式为__g/cm3(用NA表示阿伏加德罗常数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com