
科目: 来源: 题型:
【题目】“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出)。

下列有关该方法的叙述中正确的是
①能耗小是该方法的一大优点
②整个过程中,有两种物质可以循环利用
③“反应分离”环节中,分离物质的基本操作是过滤、蒸发、结晶
④该方法可减少碳排放,“捕捉”到的CO2还可用来制备甲醇等产品
A.①③B.②④C.③④D.①④
查看答案和解析>>
科目: 来源: 题型:
【题目】碘及其化合物在科研、生活等方面有广泛用途。如图所示为从海带中制取碘的工艺流程。
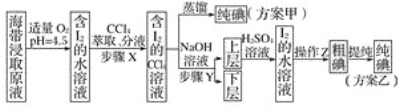
已知:3I2+6NaOH===5NaI+NaIO3+3H2O。
请回答下列问题:
(1)分液漏斗使用前需要检漏,检漏方法为__________。
(2)步骤X中,萃取后分液漏斗内观察到的现象是_____________。
(3)下列有关步骤Y的说法中正确的是_____(填字母)。
A.应控制NaOH溶液的浓度和体积
B.将碘单质转化成碘离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以用乙醇代替
(4)向“上层”中加入H2SO4溶液,发生反应的化学方程式为____,操作Z的名称为________。
(5)方案甲中采用蒸馏不合理,理由是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A. 生成物全部化学键形成所释放的能量大于破坏反应物全部化学键所吸收的能量时, 反应为吸热反应
B. 向Na2CO3溶液中加少量BaCl2固体,CO32-的水解程度变小
C. 在FeCl3+3KSCN![]() 3KCl+Fe(SCN)3体系中加入KI固体,平衡不移动
3KCl+Fe(SCN)3体系中加入KI固体,平衡不移动
D. 对一个可逆反应来说,吸热反应一方的速率受温度变化的影响总是大于放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】海水中有取之不尽的化学资源,从海水中可提取多种化工原料。如图是某化工厂对海水资源综合利用的示意图:
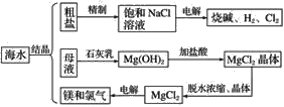
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、NaOH溶液和Na2CO3溶液,过滤,最后向滤液中加入盐酸至滤液呈中性。请写出加入盐酸后发生反应的离子方程式:____________________________。
(2)从海水中提取食盐后的母液中有K+、Na+、Mg2+等阳离子。从离子反应的角度思考,在母液里加入石灰乳起____________作用?
(3)海水里的镁元素处于游离态还是化合态_________?从海水中提取氯化镁的反应是不是氧化还原反应_________?为什么_________________?
(4)电解无水氯化镁所得的镁蒸气可以在下列哪种气体氛围中冷却?________。
A.H2
B.CO2
C.空气
D.O2
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示是以海水为原料,获得某产物的工艺流程图。已知在吸收塔中,溶液的pH显著减小。试回答下列问题:

(1)图中两次氯化的作用是否相同________(选填“是”或“否”)。
(2)吸收塔中反应的化学方程式为_______________________________,第2次氯化的离子方程式为_________________________________________________。
(3)资料证实,在酸性介质中,第1次氯化过程中可用氧气或空气替代。但在实际工业生产中为什么不用更廉价的空气替代氯气________________________。
(4)本工艺的处理方法可简单概括为“空气吹出、X气体吸收、氯化”。某同学认为在工业生产过程中对第1次氯化液直接蒸馏也可得到产物,不必进行上述过程,请对该同学的说法作出正确的评价___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铝热反应不仅用于焊接钢轨,而且还常用于冶炼熔点较高的金属如钒、铬、锰等。
请配平下列用铝热反应冶炼金属钒和钴的化学方程式,指出哪些物质是还原剂、哪些物质是氧化剂,并计算生成1 mol各种金属分别需要纯铝的质量。
V2O5+Al——Al2O3+V Co3O4+Al——Al2O3+Co
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)CH2Cl2的空间构型为______;聚丙烯的链节为______。
(2)比较Li+和H-半径大小r(Li+)____r(H-)(填“>”或“<”),并说明理由____。
查看答案和解析>>
科目: 来源: 题型:
【题目】丙烯(C3H6)是重要的有机化工原料。丙烷直接脱氢制丙烯发生的反应有:
反应Ⅰ:C3H8(g)C3H6(g)+H2(g) △H1
反应Ⅱ:2C3H8(g)3C2H4(g)+2H2(g) △H2
已知:①反应Ⅰ活化能Ea(Ⅰ)小于反应Ⅱ活化能Ea(Ⅱ);
②3种物质的燃烧热如下表:
C3H8(g) | C3H6(g) | H2(g) |
—2217.8kJ·mol-1 | —2058kJ·mol-1 | —285.8kJ·mol-1 |
(1)△H1=_______kJ·mol-1
(2)恒温恒容条件下,向密闭容器中充入1molC3H8(g),下列情况能说明丙烷脱氢制丙烯反应达到平衡状态的是______________。
A.该反应的H保持不变B.混合气体的平均摩尔质量保持不变
C.![]() 保持不变D.C3H8分解速率与C3H6消耗速率相等
保持不变D.C3H8分解速率与C3H6消耗速率相等
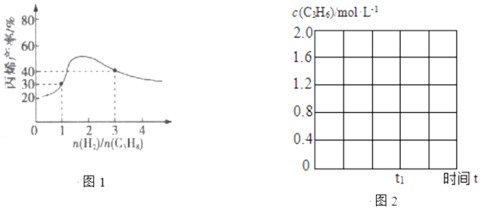
(3)一定温度下,向恒容密闭容器中充入总物质的量为4mol的丙烷和氢气混合气体(氢气的作用是活化催化剂)。反应相同时间,丙烯产率与进料气的关系如图1所示。图中曲线升高的原因是______________。
(4)①反应温度600℃,将10molC3H8(g)充入2L的刚性容器中,丙烷平衡转化率与丙烯的选择性均为40%,则反应Ⅰ的平衡常数K=______________。(保留2位小数)(丙烯的选择性=![]() ×100%)
×100%)
②600℃,丙烷脱氢反应在t1时达平衡,请在图2中画出该条件下c(C3H6)随时间t的变化图。______________
(5)含一氯丙烷(C3H7Cl)的废水可通过加入适量乙酸钠,设计成微生物电池除去,其原理如图3所示。写出N电极的电极反应式______________。

查看答案和解析>>
科目: 来源: 题型:
【题目】某固体混合物可能由SiO2、Fe2O3、Fe、Na2SO3、Na2CO3、BaCl2中的若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
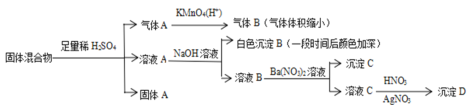
A.气体A是SO2和CO2的混合气体
B.固体A一定含有SiO2,可能含有BaSO4
C.该固体混合物中Fe2O3和Fe至少有其中一种
D.该固体混合物一定含有Na2CO3、Na2SO3、BaCl2
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下用0.1mol·L-1NaOH溶液滴定10.00mL二元弱酸H2A溶液,滴定曲线如图所示,d点恰好中和。假设混合时溶液体积变化忽略不计,下列说法不正确的是
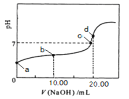
A.a点pH>1
B.c点时c(Na+)=c(H2A)+2c(A2-)+c(HA-)
C.b点时:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
D.滴定过程中c(Na+)+c(A2-)+c(HA-)+c(H2A)=0.1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com