
科目: 来源: 题型:
【题目】(1)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题。
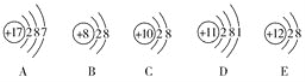
①与离子相对应的元素符号是______________,与原子相对应的离子的结构示意图是______________。
②电子层结构相同的是__________(填写代号,下同),性质最稳定的是__________,最容易失去电子的是__________,最容易得到电子的是__________。
③可直接相互结合形成的化合物的化学式是____________。可经过得失电子后再相互结合形成的化合物的化学式是______________。
④在核电荷数1~10的元素内,列举两个与B电子层结构相同的离子,写出离子的符号______________。
(2)已知元素X和Y的核电荷数均小于18,最外层电子数分别为n和(m-5),次外层有(n+2)个和m个电子,据此推断元素X和Y,其名称为X__________,Y__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
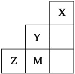
A.电负性:Z>M>Y
B.离子半径:M->Z2->Y-
C.ZM2分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子最外层电子轨道表示式为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.0.1 L 0.5 mol·L-1 CH3COOH溶液中含有的H+数为0.05NA
B.1 mol Na2O2与足量CO2和H2O充分反应,转移的电子数无法计算
C.m g CO与N2的混合气体中所含分子数目为![]() NA
NA
D.18 g 2H216O中含有的质子数与中子数均为10NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学兴趣小组为研究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)加入药品前,检查I中气体发生装置气密性的操作是__。
(2)装置Ⅰ中发生反应的化学方程式为__。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在__和___(填装置序号)之间添加洗气装置,该装置的作用是___。
(4)装置V中NaOH溶液的作用是__,相关反应的化学方程式为___。
(5)反应完毕,为探究装置Ⅳ中溶质的成分,需要的试剂主要有__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
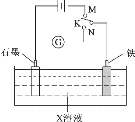
A.K与N连接时,X为硫酸,一段时间后溶液的pH减小
B.K与N连接时,X为氯化钠,石墨电极的电势更高
C.K与M连接时,X为硫酸,一段时间后溶液的pH增大
D.K与M连接时,X为氯化钠,石墨电极反应:4OH--4e-=2H2O+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】熔融碳酸盐燃料电池简称MCFC ,具有高发电效率,工作原理示意图如图。下列有关说法正确的是
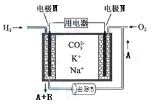
A. 电极M为负极,K+、Na+移向M
B. 电池工作时,熔融盐中CO32-物质的量增大
C. A 为CO2,正极的电极反应为:O 2+4e -+2CO2 = 2CO32 -
D. 若用MCFC给铅蓄电池充电,电极N接Pb极
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组制备氯气并对产生氯气的条件进行探究。

(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的___________(填“氧化性”或“还原性”)。
(2)A中产生的气体不纯,含有的杂质可能是___________。
(3)B用于收集Cl2,请完善装置B并用箭头标明进出气体方向_____________。
(4)C用于吸收多余的Cl2,C中发生反应的离子方程式是____________________________________________________________。
(5)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行如下探究。

①已知MnO2呈弱碱性。 Ⅰ中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是___________________________________________________。
②Ⅱ中发生了分解反应,反应的化学方程式是__________________________________。
③Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验Ⅳ进行探究:

将实验Ⅲ、Ⅳ作对比,得出的结论是____________________________;
将ⅰ、ⅱ作对比,得出的结论是___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙实验小组设计如下实验装置分别制备SnCl4和漂白粉。
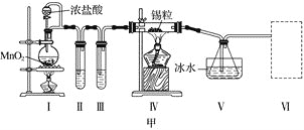
(1)已知:a.金属锡熔点231 ℃,化学活泼性与铁相似;
b.干燥的氯气与熔融金属锡反应生成SnCl4,SnCl4的沸点114 ℃;
c.SnCl2、SnCl4均易水解,易溶于有机溶剂,且Sn2+易被氧化。根据图甲装置回答:
①试管Ⅱ中的试剂是____________________,Ⅲ中的试剂是________________________。
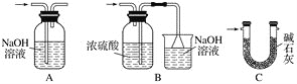
②Ⅵ处装置最好选用________(填字母)。
③Ⅰ处装置中反应的离子方程式是____________________________________________。
④实验结束后,欲回收利用装置Ⅰ中未反应完的MnO2,需要的玻璃仪器有______________。
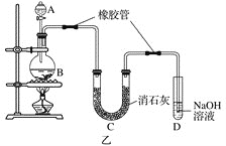
(2)已知:①Cl2与潮湿的消石灰反应是放热反应;②温度较高时Cl2与潮湿Ca(OH)2的反应为6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。
根据图乙装置回答:此实验所得Ca(ClO)2产率较低的理由是
①________________________________________________________________________;
②________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】香兰素具有浓郁的奶香,味微甜,广泛用于食品、巧克力、冰淇淋、饮料以及日用化妆品中起增香和定香作用。下面是一种以甲苯为原料合成香兰素的路线。
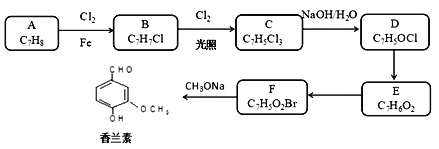
已知:
①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
②R-NO2![]() R-NH2。
R-NH2。
③R-NH2+R'COOR"![]() R-NHR"。
R-NHR"。
回答下列问题:
(1)下列说法不正确的是________。
A. 化合物A能发生还原反应 B. 化合物E能与碳酸氢钠反应产生气体
C. 化合物F具有弱酸性 D. 香兰素分子中最多12个原子共平面
(2)由F生成香兰素的化学反应方程式为________。
(3)E的结构简式为__________。
(4)写出以甲苯和乙酸乙酯为原料制备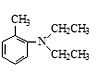 的合成路线____(用流程图表示,无机试剂任选)。
的合成路线____(用流程图表示,无机试剂任选)。
(5)写出比E分子多3个碳原子的同系物的所有同分异构体结构简式,且符合以下要求: _______。
①能使FeCl3溶液显紫色,又能发生银镜反应。②核磁共振氢谱中存在5种氢原子。
查看答案和解析>>
科目: 来源: 题型:
【题目】向20 mL某浓度的AlCl3溶液中滴加2 mol·L-1的NaOH溶液时,得到Al(OH)3沉淀的质量(g)与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
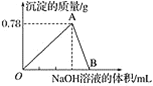
(1)图中A点表示的沉淀是__________(写化学式),其物质的量为____________。
(2)反应至A点时消耗NaOH溶液的体积为______________。
(3)图中B点溶液中的溶质有________________。
(4)AlCl3溶液的浓度为______________。
(5)O点到B点反应的总离子方程式可表示为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com