
科目: 来源: 题型:
【题目】室温下,某一元弱酸HA的电离常数K=1.6×10-6。向20.00mL浓度约为0.1mol·L-1 HA溶液中逐滴加入0.1000mol·L-1的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
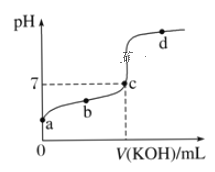
(1)a、b、c、d四点中水的电离程度最大的是_______点,滴定过程中宜选用__________作指示剂,滴定终点在__________(填“c点以上”或“c点以下”)。
(2)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_____(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(3)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。(保留4位有效数字)
实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
1 | 21.01 | 20.00 |
2 | 20.99 | 20.00 |
3 | 21.60 | 20.00 |
(4)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,向该溶液中通入过量的
,向该溶液中通入过量的![]() ,下列判断正确的是( )
,下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的有![]() 、
、![]() ;②有胶状物质生成;③有气体产生;④溶液颜色发生变化;⑤共发生了2个氧化还原反应.
;②有胶状物质生成;③有气体产生;④溶液颜色发生变化;⑤共发生了2个氧化还原反应.
A.①③⑤B.①②③C.②③④D.②④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至______。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为_________,由水电离出的c(OH-)=________mol·L-1。
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验过程中产生的现象与对应的图形相符的是( )
A.  NaHSO3 粉末加入HNO3溶液中B.
NaHSO3 粉末加入HNO3溶液中B. 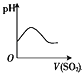 SO2气体通入新制氯水中
SO2气体通入新制氯水中
C. 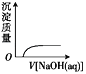 NaOH溶液滴入 Ba(HCO3)2溶液中D.
NaOH溶液滴入 Ba(HCO3)2溶液中D.  CO2气体通入澄清石灰水中
CO2气体通入澄清石灰水中
查看答案和解析>>
科目: 来源: 题型:
【题目】稀土资源素有“工业维生素”“新材料之母”之称,我国稀土储量世界第一。已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快反应(注:铈常见的化合价为![]() 和
和![]() ,氧化性:
,氧化性:![]() )。下列说法正确的是( )
)。下列说法正确的是( )
A.铈溶于氢碘酸的化学方程式可表示为:![]()
B.![]() 溶液与硫酸铁溶液混合,其离子方程式为:
溶液与硫酸铁溶液混合,其离子方程式为:![]()
C.铈元素如果要排在金属活动性顺序表中,其位置应靠近![]() 元素
元素
D.金属![]() 保存时可以用水封来隔绝空气,防止被氧化
保存时可以用水封来隔绝空气,防止被氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为__(写离子符号);若所得溶液c(HCO3):c(CO32)=2:1,溶液pH=__。(室温下,H2CO3的K1=4×107;K2=5×1011)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=__。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是__(填“A”或“B”)。
(3)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①下列叙述能说明此反应达到平衡状态的是___。
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H-H键断裂
②产物甲醇可以用作燃料电池,碱性条件下的甲醇(CH3OH)燃料电池负极反应式:__。
查看答案和解析>>
科目: 来源: 题型:
【题目】高锰酸钾、高铬酸是一种典型的强氧化剂。完成下列填空:
(1)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2 已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中的还原剂是_____________。
②该反应中,发生还原反应的过程是____________→__________。
③写出该反应的化学方程式_______________________。
(2)在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①MnO4-+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
②MnO4-+CuS+H+→Cu2++SO2↑+Mn2++H2O(未配平)
下列关于反应①的说法中正确的是______________(填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,反应转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
(3)在稀硫酸中,![]() 和H2O2也能发生氧化还原反应。
和H2O2也能发生氧化还原反应。
已知:2KMnO4+7H2O2+3H2SO4===K2SO4+2MnSO4+6O2↑+10H2O,则被2 mol KMnO4氧化的H2O2是____________mol。
(4)高锰酸钾溶液与硫化亚铁固体有如下反应:
10FeS+6KMnO4+24H2SO4===3K2SO4+6MnSO4+5Fe2(SO4)3+10S+24H2O
若上述反应前后固体的质量减少了2.8 g,则硫元素与KMnO4之间发生电子转移的数目为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(化学——选修3:物质的结构与性质)
钛有“生物金属”和“未来金属”之称,钛及其化合物的应用正越来越受到人们的关注。
(1)基态钛原子外围电子的轨道表达式为___________。与钛同周期的元素中,基态原子的未成对电子数与钛相同的有___种。
(2)金属钛的熔点、硬度均比铝大,可能的原因是____。
(3)TiCl4是氯化法制取钛的中间产物。TiCl4和SiCl4在常温下都是液体,分子结构相同。采用蒸馏的方法分离TiCl4和SiCl4的混合物,先获得的馏分是__________ (填化学式)。

(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯等的聚合,其结构如图所示。
①组成该物质的元素中,电负性最大的是__________ (填元素名称)。
②M中碳原子的杂化形式有___________种。
③M中不含__________ (填字母代号)。
a.π键 b.σ键 c.配位键
d.氢键 e.离子键

(5)①金属钛晶体中原子采用面心立方最密堆积,则晶胞中钛原子的配位数为_____。
②设钛原子的直径为d cm,用NA表示阿伏加德罗常数的值,钛原子的摩尔质量为M g·mol-1,则晶体钛的密度为________g·cm-3。
③金属钛晶胞中有若干个正四面体空隙,如图中a、b、c、d四个钛原子形成一个正四面体,其内部为正四面体空隙,可以填充其他原子。若晶胞中所有的正四面体空隙中都填充氢原子,那么形成的氢化钛的化学式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】海底蕴藏着丰富的锰结核矿,其主要成分是MnO2。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其工艺流程如图所示:
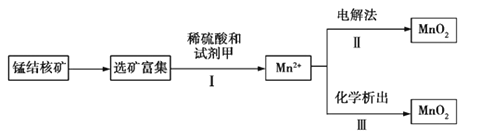
已知:化学析出时用NaClO3作析出试剂,每生成0.05 mol MnO2时消耗0.02 mol NaClO3。
根据以上工艺流程及信息,判断下列说法不正确的是
A.步骤Ⅰ中的试剂甲必须具有较强的还原性
B.步骤Ⅲ发生反应的离子方程式为2ClO3—+5Mn2++4H2O=5MnO2+Cl2+8H+
C.若用电解法,则MnO2将在阳极产生,电极反应式为Mn2+-2e-+2H2O=MnO2+4H+
D.测定步骤Ⅰ所得溶液中Mn2+的含量可采用先将Mn2+转化为Mn,然后再用0.1 mol·L-1 HCl标准溶液滴定的方法
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构示意图如图所示。下列说法不正确的是
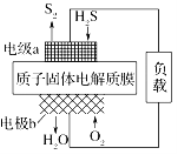
A. 电极a为电池的负极
B. 电极b上发生的电极反应为O2+4H++4e-===2H2O
C. 电路中每流过4 mol电子,在正极消耗44.8 L H2S
D. 每0.5molH2S参与反应,有1 mol H+经质子膜进入正极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com