
科目: 来源: 题型:
【题目】将溶液或气体X慢慢的加入或通入到一定量的Y溶液中,Y溶液产生沉淀的量与X的物质的量的关系可以用如图表示的是 :

A.X为NaOH溶液,Y为AlCl3溶液
B.X为CO2,Y为Ca(OH)2溶液
C.X为NH3,Y为Al2(SO4)3溶液
D.X为HCl,Y为Na[Al(OH)4]溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物醇A与羧酸B发生酯化反应生成分子式为C9H18O2的酯,0.5molA完全燃烧产生的气体被足量的澄清石灰水吸收生成200g沉淀,则下列说法正确的是( )
A.A的分子式为C4H8OB.B的分子式为C5H10O2
C.酯C9H18O2在稀硫酸溶液中不水解D.有机物A、B都能与NaHCO3溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E、F6种短周期元素,G为过渡元素;已知相邻的A、B、C、D 4种元素原子核外共有56个电子,在周期表中的位置如图所示。1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E单质粉末与G的氧化物常用于野外焊接钢轨;F是短周期最活泼的金属元素。请回答下列问题:
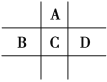
(1)元素D、G的名称分别为:__。
(2)D的单质与C的气态氢化物反应方程式为___。
(3)C、E、A的简单离子半径:__>__>__,B、C、D的最高价氧化物对应的水化物的酸性强弱顺序为___(用化学式表示)。
(4)向D与E形成的化合物的水溶液中滴加过量烧碱溶液的离子方程式为__。
(5)用电子式表示F与C形成化合物的过程___。
(6)G的单质与高温水蒸气反应的方程式___。
(7)部分元素在周期表中的分布如图所示(虚线为金属元素与非金属元素的分界线),下列说法不正确的是___。
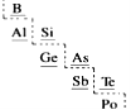
A.B只能得电子,不能失电子 B.原子半径Ge>Si
C.As可作半导体材料 D.Po处于第六周期第VIA族
查看答案和解析>>
科目: 来源: 题型:
【题目】黄色超氧化钾(KO2)可作为宇宙飞船舱的氧源。某学习小组设计以下实验探究KO2的性质,请回答相关问题:
I.探究KO2与水的反应:取少量KO2固体于试管中,滴加少量水快速产生气泡,将带火星的木条靠近试管口木条复燃,滴加酚酞试液则先变红后褪色。
向褪色后溶液中滴加FeCl3溶液推测产生的现象为___。
II.探究KO2与SO2的反应
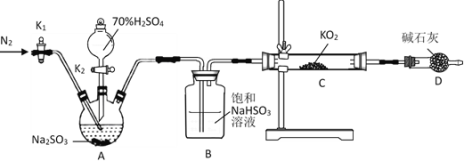
(1)正确的操作依次是__。
①打开K1通入N2 ,排尽装置内原气体后关闭 ②拆卸装置至实验完成
③检查装置气密性,然后装入药品 ④打开分液漏斗活塞K2
(2)检查上述装置气密性的方法是___。
(3)A装置发生的化学方程式为___。
(4)用上述装置验证“KO2与SO2反应生成O2”还存在不足,你的改进措施是__。
(5)改进后再实验,待KO2完全反应后,将装置C中固体加水溶解,配成50.00mL溶液,等分为M、N两份。
①向M溶液中加入足量的盐酸酸化的BaCl2溶液,充分反应后,将沉淀过滤、__、__,称重为2.33g。
②将N溶液移入__(填仪器名称)中,用0.40mol/L酸性KMnO4溶液滴定,终点时消耗酸性KMnO4溶液20.00mL。
③依据上述现象和数据,请写出该实验总反应的化学方程式__。
查看答案和解析>>
科目: 来源: 题型:
【题目】经研究发现白蚁信息素有:![]() (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),![]() (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
A.2,4-二甲基1庚烯的分子式为C9H18
B.2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同系物
C.以上三种信息素均能使溴的四氯化碳溶液褪色
D.1 mol家蚕的性信息素与1 mol Br2加成,产物只有一种
查看答案和解析>>
科目: 来源: 题型:
【题目】烟气脱硫脱硝是环境治理的热点问题。
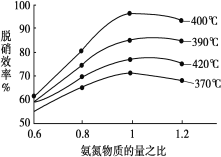
(1)氧化还原法脱硝:4NO(g)+4NH3(g)+O2(g)=4N2(g)+6H2O(g)ΔH=-1627.2kJ/mol。检验脱硝效果的重要指标是脱硝效率(脱硝过程中单位时间内NOx浓度变化占烟气初始浓度的百分比)。影响SCR系统脱硝效率的因素有很多,根据如图判断提高脱硝效率的最佳条件是__;氨氮比一定时,随温度的升高脱硝效率增大,其可能的原因是___。
(2)H2Y2-与Fe2+形成的络合物FeY2-可用于吸收烟气中的NO。原理:FeY2-(aq)+NO(g)![]() FeY2-(NO)(aq)ΔH<0
FeY2-(NO)(aq)ΔH<0
①将含NO的烟气以一定的流速通入起始温度为50℃的FeY2-溶液中。NO吸收率随通入烟气的时间变化如图。时间越长,NO吸收率越低的原因是___。
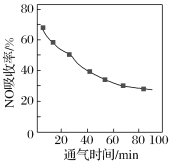
②生成的FeY2-(NO)(aq)可通过加入铁粉还原再生,其原理为FeY2-(NO)(aq)+Fe+H2O→FeY2-(aq)+Fe(OH)2+NH3(未配平)。若吸收液再生消耗14 g铁粉,则所吸收的烟气中含有NO的物质的量为__mol。
(3)以连二硫酸盐(S2O42-)为媒介,使用间接电化学法也可处理NO,装置如图所示:阴极的电极反应式为___。
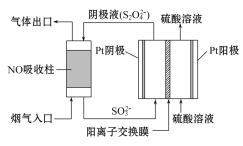
(4)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO42-。
①KMnO4脱硫(SO2)的离子方程式为____。
②加入CaCO3的作用是___。
(5)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,溶液pH对脱硫脱硝的影响如图所示:图中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释二者去除率不同的可能原因是__。
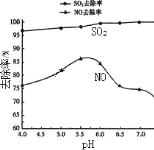
查看答案和解析>>
科目: 来源: 题型:
【题目】利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是
5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是

A. b点时,CO的转化率为20%
B. 容器内的压强保持恒定,表明反应达到平衡状态
C. b点和d点的化学平衡常数:Kb>Kd
D. 0到0.5min反应速率v(CO)=0.3mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应X(g)+Y(g)![]() R(g)+Q(g)的平衡常数与温度的关系如表所示。830 ℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005 mol/(L·s)。下列说法正确的是
R(g)+Q(g)的平衡常数与温度的关系如表所示。830 ℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005 mol/(L·s)。下列说法正确的是
温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A. 4 s时容器内c(Y)=0.76 mol/L
B. 830 ℃达平衡时,X的转化率为80%
C. 反应达平衡后,升高温度,平衡正向移动
D. 1 200 ℃时反应R(g)+Q(g) ![]() X(g)+Y(g)的平衡常数K=0.4
X(g)+Y(g)的平衡常数K=0.4
查看答案和解析>>
科目: 来源: 题型:
【题目】温度分别为T1和T2时,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g),一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g),一段时间后达到平衡,反应过程中测定的数据如下表:
温度/K | t/min | t1 | t2 | t3 | t4 |
T1 | n(Y)/mol | 0.14 | 0.12 | 0.10 | 0.10 |
T2 | n(Y)/mol | 0.13 | 0.09 | 0.08 |
下列说法正确的是( )
A. 该反应的正反应为放热反应
B. T2温度下此反应的平衡常数K=4
C. 温度为T1时,0~t1时间段的平均速率υ(Z)=2.0×10-3mol·L-1·min-1
D. 在T1下平衡后,保持其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
科目: 来源: 题型:
【题目】相对分子质量为Mr的气态化合物V L(标准状况)溶于m g水中,得到溶液的溶质质量分数为w%,物质的量浓度为c mol·L-1,密度为ρ g·cm-3,则下列说法正确的是
A.溶液密度ρ可表示为![]()
B.物质的量浓度c可表示为![]()
C.溶液的质量分数w%可表示为![]()
D.相对分子质量Mr可表示为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com