
科目: 来源: 题型:
【题目】过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
![]()
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:_____________。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(以mg·L1表示),写出计算过程_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】经检测,某工业废水显酸性,且废水中含有大量Na+、Cu2+、Cl-、SO42-、NO3-,
(1)下列离子中,不可能大量存在于该废水中的是___(填序号)。
A.K+ B.Fe3+ C.Ag+ D.HCO3-
(2)若向上述废水中加入大量的过氧化钠固体,观察到的现象为___;相关的离子方程式为___。
(3)若工业废水中只含有H+和Na+、Cu2+、Cl-、SO42-、NO3-,经分析测得,H+、Cu2+、Cl-、SO42-、NO3-的物质的量浓度分别为:0.1mol·L-1、0.05mol·L-1、0.2mol·L-1、0.1mol·L-1、0.1mol·L-1,则Na+的物质的量浓度为___。
(4)设计实验方案除去原废水中的Cu2+和SO42-(用流程图表示)(提示:加入的试剂要过量)___。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究Cl2、SO2同时通入水中所发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
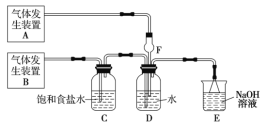
(1)该化学兴趣小组的同学采用Na2SO3与质量分数为70%的硫酸为原料制取SO2,采用MnO2与浓盐酸为原料制取Cl2。在此实验中,仪器![]() 的作用是______;气体发生装置B应选择下列装置中的____________(填序号)。
的作用是______;气体发生装置B应选择下列装置中的____________(填序号)。
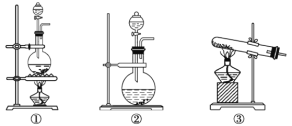
(2)为验证通入D装置中的气体是Cl2过量还是SO2过量,该化学兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有______(填序号)的试管中,再加入______(填序号),产生的现象是______。
若SO2过量,取适量D中溶液滴加至盛有______(填序号)的试管中,产生的现象是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知镁在空气中燃烧主要生成氧化镁,同时还会与氮气反应生成微量的氮化镁(Mg3N2)在周期表中,镁与锂;铍与铝处于对角线上,处于对角线上的主族元素性质相 似,这称为对角线规则。据此请回答:
(1)锂在空气中燃烧主要产物的电子式是_____________同时生成微量的________。(写化学式)
(2)铍的最高价氧化物对应的水化物的化学式是_________________,它属两性化合物,证明这一结论的有关离子方程式为____________________,_____________________。
(3)若已知反应Be2C+4H2O===2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式为____________________________。
(4)用电子式表示BeCl2的形成过程:________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用氧化还原反应原理配平
(1)__NH3+___O2![]() ____NO +____H2O
____NO +____H2O
(2)____FeSO4+____KNO3+____H2SO4=____K2SO4+____Fe2(SO4)3+____NO↑+____H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组用如图所示装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。请回答下列问题:
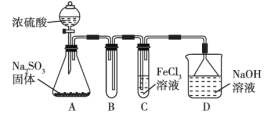
(1)通入足量SO2时C中观察到的现象为______。
(2)根据以上现象,该小组同学认为SO2与FeCl3发生了氧化还原反应。
请设计实验方案检验有Fe2+生成:____________。
(3)为了验证SO2具有还原性,实验中可以代替FeCl3溶液的试剂有______(填序号)。
A.浓硫酸 B.酸性KMnO4溶液
C.碘水 D.NaCl溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:pAg=-lgc(Ag+),pX=-lg c(Xn-)。298K时,几种物质的Ksp如下表:
化学式 | AgCl | AgSCN | Ag2CrO4 |
颜色 | 白 | 浅黄 | 红 |
Ksp | 1.8×1010 | 1.0×1012 | 2.0×1012 |
AgCl、AgSCN、Ag2CrO4的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
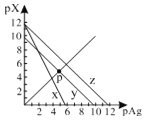
A.图中x代表AgCl曲线,z代表AgSCN曲线
B.298K时,在Cl-和CrO42-的物质的量浓度均为0.1mol/L的溶液中,滴入少量0.1mol/L的AgNO3溶液,首先产生的是红色沉淀
C.298K时若增大p点的阴离子浓度,则y上的点沿曲线向上移动
D.298K时Ag2CrO4(s)+2SCN-(aq) ![]() 2AgSCN(s)+CrO42- (aq)的平衡常数K=2.0×1012
2AgSCN(s)+CrO42- (aq)的平衡常数K=2.0×1012
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。(已知:Na2SO3+ H2SO4(浓)=Na2SO4+SO2↑+H2O)
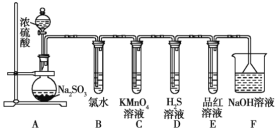
请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠仪器的名称分别是______、______。
(2)反应后,装置B中产生的现象是______,发生反应的离子方程式为______;装置D中的现象是______,发生反应的化学方程式为______。
(3)装置E的目的是探究SO2与品红溶液作用的可逆性,写出实验操作及现象:____________。
(4)F装置的作用是______,倒扣漏斗的作用是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下分别向20.00 mL 0.1000 mol·L-1的氨水、醋酸铵溶液中滴加0.1000mol·L-1的盐酸,溶液pH与加入盐酸体积的变化关系如图所示。下列说法正确的是

A. M点溶液中c (OH-)>c(NH4+)>c(NH3·H2O)>c(H+)
B. N点溶液中c(NH4+)>c(NH3·H2O)>c(Cl-)>c(OH-)
C. P点溶液中c(NH4+)>2c(CH3COO-)+c(NH3·H2O)
D. Q点溶液中2c(Cl-)>c(CH3COOH)+c(NH4+)
查看答案和解析>>
科目: 来源: 题型:
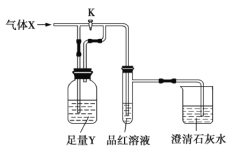
【题目】如图是一套检验气体性质的实验装置。请回答下列问题。
A | B | C | D | |
X | 氯气 | 二氧化硫 | 二氧化碳 | 氯化氢 |
Y | Na2SO3溶液 | 饱和NaHCO3溶液 | Na2SO3溶液 | 饱和NaHSO3溶液 |
(1)向装置中缓缓通入少量气体X,若关闭活塞K,则品红溶液褪色。据此判断气体![]() 和洗气瓶内的溶液Y可能的组合是_________(填表中序号,下同)。
和洗气瓶内的溶液Y可能的组合是_________(填表中序号,下同)。
(2)若打开活塞K,品红溶液褪色,同时澄清石灰水变浑浊,则气体X和洗气瓶内液体Y可能的组合是______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com