
科目: 来源: 题型:
【题目】油脂是人类日常生活中必不可少的营养物质,油脂的主要成分是高级脂肪酸甘油酯。常见的高级脂肪酸有硬脂酸、软脂酸、油酸和亚油酸四种,现将这四种酸与甘油混合加热,生成混甘油酯的种类有(不考虑立体异构)(已知:结构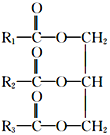 中,R1、R2、R3相同的为单甘油酯,R1、R2、R3不完全相同的为混甘油酯)
中,R1、R2、R3相同的为单甘油酯,R1、R2、R3不完全相同的为混甘油酯)
A. 28种 B. 32种 C. 36种 D. 40种
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜矿是工业冶炼铜的原料,主要成分为 CuFeS2。试回答下列问题:
(1)基态硫原子核外电子有_____种不同运动状态,能量最高的电子所占据的原子轨道形状为_________。
(2)基态Cu原子的价层电子排布式为_________;Cu、Zn的第二电离能大小I2(Cu) _________I2(Zn)(填“>”“<”或“=”)。
(3)SO2分子中S原子的轨道杂化类型为_________,分子空间构型为_________;与SO2互为等电子体的分子有_________(写一种)。
(4)请从结构角度解释H2SO3的酸性比H2SO4酸性弱的原因_________。
(5)Cu(CH3CN)4比四氨合铜离子稳定,其配离子中心原子配位数为_________,配位体中σ键与π键个数之比为_________。
(6)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

若该晶体储氢时,H2分子在晶胞的体心和棱的中心位置,距离最近的两个H2分子之间距离为anm。则该晶体的密度为_________g/cm3(列出计算表达式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室通常用无水乙醇和浓硫酸加热到170℃制取乙烯,反应方程式为:CH3CH2OH![]() CH2=CH2↑+H2O。若温度过高或加热时间过长,制得的乙烯往往混有CO2、SO2、H2O(g)。
CH2=CH2↑+H2O。若温度过高或加热时间过长,制得的乙烯往往混有CO2、SO2、H2O(g)。
(1)试用下图所示的装置设计一个实验,验证制得的气体中含有杂质气体:二氧化碳,二氧化硫和水蒸气,按气流的方向,各装置的连接顺序是 。

(2)实验时若观察到:①中A瓶中溶液褪色,B瓶中溶液颜色逐渐变浅,C瓶中溶液不褪色,则B瓶的作用是 ,C瓶的作用是 。
(3)若气体通过装置③中所盛溶液时,产生白色沉淀,它可以用来验证的气体是____。
(4)装置②中所加的试剂名称是____ _______。
(5)乙烯在一定条件下能制得聚乙烯,写出相应的化学反应方程式: 。
(6)某同学做此实验时发现装置④存在的不妥之处是: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为_____,X的相对原子质量为_____。
(2)相同状况下,一定体积的气态氢化物H2X的质量是等体积NH3的2倍.则X的相对原子质量为_____。
(3)0.05mol 的硫酸钠中含有_____个氧原子;与_____g NaCl中所含有的Na+数目相同.
(4)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mLA受热完全分解生成15mLO2和10mL F2,则A的化学式为_____。
(5)0.5L 0.5mol/L FeCl3溶液中的Cl﹣的物质的量浓度为_____。
(6)质量分数为98%,密度为1.84g.cm﹣3的某浓硫酸,溶质的物质的量浓度为_____。
(7)a个X原子的总质量为b g,则X的相对原子质量可表示为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物 A 广泛用于涂料、油墨、胶黏剂、医药及农药中间体领域。已知:有机物 A 的仪器分析如下:
①有机物 A 的质谱 ②有机物 A 的红外光谱
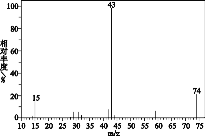
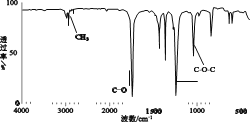
③ 有机物 A 的核磁共振氢谱图上有 2 个吸收峰,峰面积之比是 1︰1。回答下列问题:
(1)A 的相对分子质量是______;
(2)A 含有官能团的名称是_______;
(3)A 的结构简式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】物质的分类如图所示:

由图判断下列说法中不正确的是( )
A.甲图所示的分类方法属于树状分类法
B.乙图所示的分类方法属于交叉分类法
C.碱性氧化物一定是金属氧化物
D.非金属氧化物一 定是酸性氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】石油裂解气用途广泛,可用于合成各种橡胶和医药中间体。利用石油裂解气合成CR橡胶和医药中间体K的线路如下:

已知:Ⅰ.氯代烃D的相对分子质量是113,氯的质量分数约为62.8%,核磁共振氢谱峰面积之比为2:1.
Ⅱ.  。
。
(1)A中官能团的结构式为__________________,D的系统名称是________________.
(2)反应②的条件是_____________,依次写出①和③的反应类型___________、_________.
(3)写出F→G过程中第一步反应的化学方程式____________________________.
(4)K的结构简式为____________________.
(5)写出比G多2个碳原子的同系物的所有同分异构体的结构简式_________________.
(6)已知双键上的氢原子很难发生取代反应。以A为起始原料,选用必要的无机试剂合成B_______。合成路线流程图示如下:
![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色混合物水溶液,可能含有以下离子中的若干种:K+、NH4+、Mg2+、Cu2+、Cl-、CO32-、SO42-,现各取 100mL 溶液三份进行如下实验:①向第一份加入 AgNO3 溶液,有白色沉淀产生;②向第二份加入足量 NaOH 溶液后加热,收集到气体 0.896L(标准状况)③向第三份加入足量 BaCl2 溶液,得到沉淀 6.63 克,经足量盐酸洗涤后,剩余 4.66 克。 试回答下列问题:
(1)肯定存在的离子有__________,肯定不存在的离子有__________;
(2)可能存在的离子是__________,判断该离子存在与否的方法是__________;
(3)肯定存在的阳离子在原溶液中的物质的量浓度__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)

实验过程:
Ⅰ.打开弹簧夹,打开活塞 a,滴加浓盐酸
Ⅱ.当 B 和 C 中的溶液都变为黄色时,夹紧弹簧夹
Ⅲ.当 B 中溶液由黄色变为棕红色时,关闭活塞 a
Ⅳ.…
(1)A 中反应的化学方程式为:____KMnO4+_____HCl(浓)═____ KCl+____MnCl2+____Cl2↑+____H2O,则氧化性 KMnO4________Cl2(填“>”“<”或“=”).
(2)验证氯气的氧化性强于碘的实验现象是__________
(3)过程Ⅲ的实验目的是__________
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是__________。
(5)浸有 NaOH溶液的棉花团的作用是__________。此处发生 的化学方程式是__________。
(6)氰(CN)2、硫氰(SCN)2的化学性质和卤素很相似,化学上称为“类卤素”,它们阴离子的还原性强弱为:Cl- < Br- < CN- < SCN- < I-。试写出:
a.(CN)2 与 KOH 反应的化学方程式__________;
b.在 NaBr 和 KSCN 的混合溶液中加入(CN)2 的离子方程式__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液最好的方法是_______(写出具体实验操作,结论)。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________________________。
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是_____;
②溶液组成的测定:取50.0mL待测溶液,加入足量的AgNO3溶液,得到21.525g白色沉淀。则溶液中c(Cl-)=______mol/L。
③验证该溶液中是否含有Fe2+,正确的实验方法是_____________。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液先滴入氯水再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
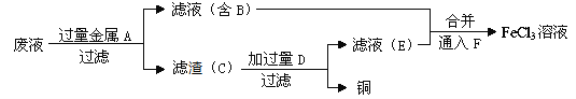
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
①滤渣C的化学式为_________________。
②加过量D发生反应的离子方程为_____________________________________。
③通入F发生反应的离子方程式为 ____________________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com