
科目: 来源: 题型:
【题目】实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是

A. 向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B. 实验中装置b中的液体逐渐变为浅红色
C. 装置c中的碳酸钠溶液的作用是吸收溴化氢
D. 反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
查看答案和解析>>
科目: 来源: 题型:
【题目】祖母绿是四大名贵宝石之一,主要成分为Be3Al2Si6O18,含有微量的Cr、Ni、Fe元素而呈现各种颜色。回答下列问题:
(1)基态Ni2+的电子排布式为_______________;宝石中Si的杂化方式是____。
(2)成键元素电负性差值越大,化学键离子性百分数越高,在卤素与Al组成的化合物中,离子性百分数最高的化合物是______(填化学式)。
(3)六羰基铬[Cr(CO)6]用于制高纯度铬粉,它的沸点为220℃。Cr(CO)6的晶体类型是______,加热Cr(CO)6可得到高纯度铬粉和CO,反应破坏的作用力类型为_________。
(4)多数配离子显示颜色与d轨道的分裂能有关。分裂能是指配离子的中心原子(离子)的一个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量(用Δ表示),它与中心离子的结构、电荷、配体有关。试判断分裂能Δ[Fe(H2O)63+] _____ Δ[Fe(H2O)62+](填“>”“<”或“=”),理由是__________。
(5)氧化镍晶胞如图所示,A的原子坐标参数为:(0,0,![]() ),则底面面心B的原子坐标参数为______。
),则底面面心B的原子坐标参数为______。
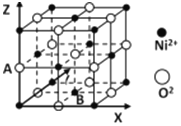
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋资源开发前景十分广阔。海水晒盐能够得到粗盐和卤水,卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线。则下列说法不正确的是

A.t1℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgCl2
B.t1℃时,分别在100g水中溶解了等质量的MgCl2、KCl,两溶液都可达到饱和
C.t2℃时,KCl和MgSO4两种物质的溶解度相同
D.将卤水加热到t2℃ 以上,析出的晶体主要为MgSO4
查看答案和解析>>
科目: 来源: 题型:
【题目】已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表:
元素 | 结构或性质信息 |
X | 原子的L层上s电子数等于p电子数 |
Y | 原子核外的L层有3个未成对电子 |
Z | 地壳中含量最多的元素 |
Q | 单质常温常压下是气体,原子的M层上有1个未成对的p电子 |
R | 核电荷数是Y与Q的核电荷数之和 |
E | N能层上只有一个电子,K、L、M层均排满电子 |
请根据信息回答有关问题:
(1)写出元素Y的原子核外价电子排布图:___________。X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为______。
(2)X、Y、Z三种元素的第一电离能由高到低的排列为(写元素符号)_____。
(3)X、Z元素分别与氢元素形成的最简单化合物中,沸点较高的为(写化学式)______,原因是________。
(4)XZ与Y2属于等电子体,写出化合物XZ的结构式:_____。
(5)R的一种配合物的化学式为RCl36H2O。已知0.01mol RCl36H2O在水溶液中用过量硝酸银溶液处理,产生0.02mol AgCl沉淀。此配合物最可能是____。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2H2O
C.[R(H2O)4Cl2]Cl2H2O D.[R(H2O)3Cl3]3H2O
(6)向含少量ESO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,反应的离子方程式为:__,继续滴加氨水至过量,沉淀溶解,得到深蓝色溶液,写出反应的离子方程式为:__。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,容积为2 L的密闭容器中,将2 mol M气体和3 mol N气体混合发生下列反应2M(g)+ 3N(g)![]() xQ(g)+ 3R(g),该反应达到平衡时生成2.4 mol R,并测得Q浓度为0.4 mol/L,下列叙述正确的是
xQ(g)+ 3R(g),该反应达到平衡时生成2.4 mol R,并测得Q浓度为0.4 mol/L,下列叙述正确的是
A.x值为2
B.混合气体的密度增大
C.平衡时N的浓度为 0.6 mol/L
D.N的转化率为80%
查看答案和解析>>
科目: 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O。将6g该有机物的完全燃烧产物先通过浓硫酸,浓硫酸增重3.6g,再通过碱石灰,碱石灰增重8.8g。则该有机物的分子式为( )
A.C4H10B.C2H6OC.C3H8OD.C2H4O2
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F的核电荷数依次增大,且均为核电荷数小于18的非稀有气体元素。A的单质是自然界中密度最小的气体,A和C可形成A2C和A2C2两种常见的液态化合物,B、C原子的最外层电子数之和等于11,D+与C的简单离子的最外层电子排布相同,C、E原子的最外层电子数相同。请回答下列问题:
(1)写出元素符号:B______,D______。
(2)A元素具有两个中子的核素的表示符号为______,E的简单离子的结构示意图是______。
(3) A2C2的分子式为______。
(4)将少量![]() 的单质通入足量NaOH溶液中,发生反应的离子方程式是______。
的单质通入足量NaOH溶液中,发生反应的离子方程式是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)E的价电子排布式是_____,A、B、C、D的第一电离能由小到大的顺序_____。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是__________;
(3)D的低价氧化物分子的空间构型是_______。
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为_______________;(每个球均表示1个原子,白球为A,黑球为E) 若相邻A原子和E原子间的距离为a nm,阿伏加德罗常数为NA,则该晶体的密度为_____________g/cm3(用含a、NA的符号表示)。
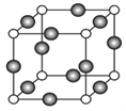
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C三种元素的原子中,质于数:A<B<C,且都小于18。A元素原子的最外层电子数是次外层电子数的2倍;B元素原子的M层电子数是L层电子数的一半;C元素原子的次外层电子数比最外层电子数多1。试回答下列问题。
(1)写出三种元素的名称和符号:A______,B______,C______。
(2)画出三种元素的原子结构示意图:A______,B______,C______。
查看答案和解析>>
科目: 来源: 题型:
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是
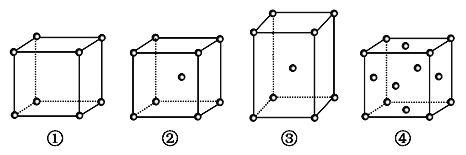
A.晶胞中原子的配位数分别为①6,②8,③8,④12
B.空间利用率的大小关系为①<②<③<④
C.①为简单立方堆积,②为镁型,③为钾型,④为铜型
D.每个晶胞含有的原子数分别为①1个,②2个,③2个,④4个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com