
科目: 来源: 题型:
【题目】乳酸是天然的酸味调节剂,乳酸的结构简式为![]() ,下列关于乳酸的说法正确的是( )
,下列关于乳酸的说法正确的是( )
A.含有醛基官能团
B.1mol乳酸可以和2molNaOH 溶液恰好完全反应
C.1mol乳酸和碳酸氢钠溶液充分反应生成2molCO2
D.乳酸和乙酸都显酸性,但它们在浓硫酸作用下经加热可以发生化学反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于苯乙烯(![]() )的下列叙述①能使酸性KMnO4溶液褪色、②可发生加聚反应、③可溶于水、④可溶于苯中、⑤能与浓硝酸发生取代反应、⑥所有的原子可能共平面,其中正确的是( )
)的下列叙述①能使酸性KMnO4溶液褪色、②可发生加聚反应、③可溶于水、④可溶于苯中、⑤能与浓硝酸发生取代反应、⑥所有的原子可能共平面,其中正确的是( )
A.仅①②④⑤B.仅①②⑤⑥C.仅①②④⑤⑥D.全部正确
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物F是一种重要的有机合成中间体,它的合成路线如图:
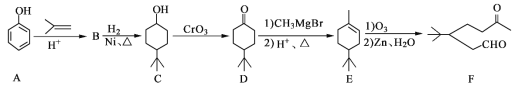
(1)化合物F中含氧官能团的名称是______和______,由A生成B的化学反应类型是______;
(2)写出化合物B的结构简式:______;
(3)写出化合物C与乙酸反应生成酯的化学方程式:______;
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化合物的结构简式:______(任写一种);
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作说法正确的是
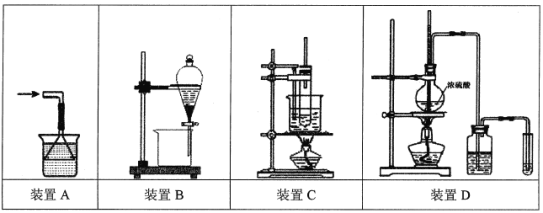
A.处理极易溶于水的气体尾气如NH3时,可选用装置A
B.萃取分离溴水中的Br2,可选用装置B,在萃取剂选择上可使用酒精、苯或CCl4
C.苯的硝化反应实验可选用装置C,反应前在试管中将1.5 mL浓HNO3和2 mL浓硫酸混合均匀,再快速倒入苯,防止其挥发
D.验证乙醇消去反应生成乙烯的实验可选用装置D,洗气瓶内需盛放NaOH溶液,反应开始时,加热烧瓶使混合液迅速上升到170℃
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2。
(1)C分子的质谱图如图所示,从图中可知其相对分子质量是__,则C的分子式是__。
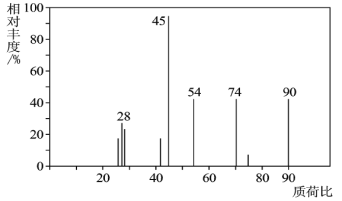
(2)C能与NaHCO3溶液发生反应,C一定含有的官能团是__。
(3)C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则C的结构简式是__。
(4)0.1molC与1.0mol/L的氢氧化钠溶液反应,需溶液的体积是__mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.铜和过量的浓HNO3反应:3Cu +8H+ +2NO![]() = 3Cu2++ 2NO↑+4H2O
= 3Cu2++ 2NO↑+4H2O
B.CaCO3和盐酸反应:2H++CaCO3 =Ca2+ +CO2 ↑+H2O
C.向NH4HCO3溶液中加过量Ca(OH)2溶液并加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
D.将Ba(OH)2滴加到稀硫酸中:Ba2+ + SO![]() = BaSO4 ↓
= BaSO4 ↓
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是
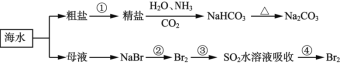
A.制取NaHCO3的反应是利用其溶解度小于NaCl
B.侯氏制碱应先通NH3再通CO2
C.在第②、③、④步骤中,溴元素均被氧化
D.③④的目的是进行溴的富集
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题:
(1)键线式![]() 的系统命名为 __________________;
的系统命名为 __________________;
(2)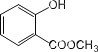 中含有的官能团为_______________;
中含有的官能团为_______________;
(3)2-甲基-1-丁烯的结构简式____________________;
(4)相对分子质量为 72 且一氯代物只有一种的烷烃的结构简式________________;
(5)分子式为 C2H6O 的有机物,有两种同分异构体,乙醇(CH3CH2OH)、甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是________________;
A.红外光谱 B.核磁共振氢谱 C.质谱法 D.与钠反应
查看答案和解析>>
科目: 来源: 题型:
【题目】镍及其化合物在生产生活中有着极其重要的作用。现以低品位镍红土矿(主要成分为镍的氧化物、Fe2O3·H2O和SiO2等)为原料制备兰尼镍的工艺流程如图所示:
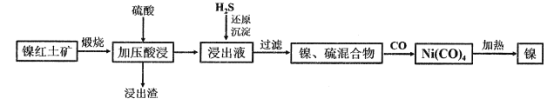
已知加压酸浸过程中的相关影响因素如下:
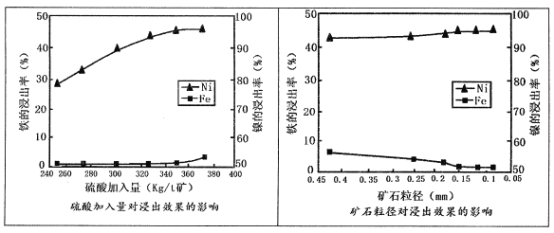
请回答:
(1)请根据图示,选择加压酸浸过程中硫酸的加入量和矿石粒径的最适宜条件为_______
A.260Kg/t矿;0.45mm B.320 Kg/t矿:0.25mm
C.350Kg/t矿;0.15mm D.380 Kg/t矿;0.05mm
(2)①已知镍红土矿煅烧后生成Ni2O3,而加压酸浸后浸出液中含有Ni2+,写出加压酸浸过程中镍元素所涉及的化学反应方程式____________。
②甲同学取该浸出液,控制pH为2~3,经过-系列操作,制取少量NiSO4·7H2O晶体。其控制pH为2~3的目的为____________________________________________________。
③乙同学取该浸出液,经多次处理,得到一定浓度的NiSO4溶液,往其中加入适量的NaClO和NaOH混合液,制得碱性镍电池电极材料NiOOH,该反应的离子方程式为____________。
(3)向浸出液中通入H2S气体,该反应的离子方程式为__________。
(4)下列说法正确的是________________
A.在煅烧过程中,空气宜选择从下往上的通入方式,使镍红土矿燃烧更充分
B.加压酸浸中,为加快反应速率,可选用浓硫酸
C.加压酸浸中,在最适宜条件下,浸出渣中的主要成份为SiO2和Fe2O3·H2O
D.CO为无色无味的有毒气体,故从镍硫混合物到镍的过程中,需注意通风并及时检测操作过程中是否有CO泄露
查看答案和解析>>
科目: 来源: 题型:
【题目】欲配制250mL0.1molL-1的稀盐酸,实验室的浓盐酸密度为1.25gcm-3,质量分数为36.5%。
请回答下列问题:
(1)配制稀盐酸时下表中不需要使用的仪器有___(填序号),还缺少的仪器为___、___(写仪器名称)。
序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
仪器 |
|
|
|
|
|
|
(2)需要量取浓盐酸的体积为___mL。
(3)配制该溶液的操作顺序是:D→___→___→___→___→B(用字母符号表示,每个字母符号只用一次)。
A.用30mL蒸馏水洗涤烧杯和玻璃棒各2~3次,将洗涤液全部注入容量瓶中并轻轻摇动
B.将容量瓶盖紧,振满,摇匀
C.将已恢复至室温的盐酸沿玻璃棒注入所选用的容量瓶中
D.用量筒准确量取所需体积的浓盐酸,将其沿玻璃棒注入烧杯中,再向烧杯中加入少量蒸馏水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
E.改用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶的刻度线相切
F.继续往容量瓶中小心地滴加蒸馏水,直到液面接近刻度线1~2cm处
(4)在定容时,液面高于刻度线,则所配溶液的浓度将___(选填“偏高”或“偏低”),该如何处理?___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com