
科目: 来源: 题型:
【题目】利用铝热炼镁还原渣[Al、Ca(AlO2)2、Al2O3、MgO及少量不能被碱液溶出的尖晶石型铝的化合物等]制取Al(OH)3的工艺流程如下:
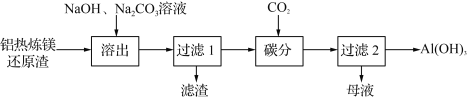
(1) “滤渣”成分包括:水合铝酸钙、尖晶石型铝的化合物、不含铝的化合物______________(写两种物质的化学式)。
(2) “溶出”时,在适当条件下,铝及其大部分含铝化合物以NaAlO2溶出。
①金属Al与NaOH溶液反应的化学方程式为________________________________。
②其他条件相同时,Na2CO3、NaOH溶液的浓度对铝的溶出率的影响如图所示:
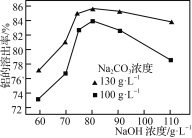
NaOH溶液浓度一定时,130 g·L-1的Na2CO3溶液对铝的溶出率比100 g·L-1的大,这是因为______________(从平衡移动角度分析);Na2CO3溶液浓度一定时,当NaOH溶液浓度大于80 g·L-1,铝的溶出率随NaOH溶液浓度增大而减小,可能原因是______________。
(3) “碳分”时,溶液与过量CO2反应的离子方程式为________________________。
(4) “过滤2”的母液经再生处理可返回“溶出”工序循环使用,再生的方法是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)在101kPa下,1g氢气完全燃烧生成液态水放出142.9kJ的热量。
①该反应的反应物总能量_____生成物总能量(填“大于”、“小于”或“等于”)。
②该反应的热化学方程式为_______________________。
(2)若lmol氢气完全燃烧生成lmol气态水放出241kJ的热量。
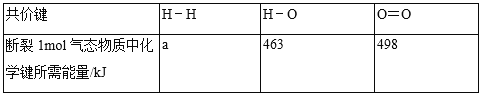
经计算表中a为_____
(3)炭粉与水蒸气反应生成CO(g)和标准状况下22.4LH2(g)吸收131.5kJ的热量,写出热化学方程式:_____________。
(4)当同一反应,生成物状态不同时,A(g)+B(g)=C(g) ΔH1<0;A(g)+B(g)=C(l) ΔH2<0,则ΔH1____ΔH2。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算铜元素相对原子质量。提供的实验仪器及试剂如下(根据需要可重复选用,加入的氯化铵与氢氧化钙的量足以产生使氧化铜完全还原的氨气):
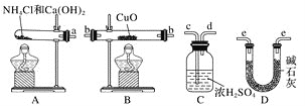
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为__。
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→__。
(3)在本实验中,若测得m(CuO)=ag,m(H2O)=bg,则Ar(Cu)=__。
(4)在本实验中,使测定结果Ar(Cu)偏大的是__(填序号)。
①氧化铜未完全起反应 ②氧化铜不干燥 ③氧化铜中混有不反应的杂质 ④碱石灰不干燥 ⑤氯化铵与氢氧化钙混合物不干燥
(5)在本实验中,还可通过测定__和__,或__和__达到实验目的。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A. 已知2SO2(g)+O2(g)![]() 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B. 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C. 已知H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ/mol,代表任何酸碱反应的中和热都是ΔH=-57.3 kJ/mol
D. 已知2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学一有机化学基础](13分)
对二甲苯(英文名称p-xylene,缩写为PX)是化学工业的重要原料。
(1)写出PX的结构简式 。
(2)PX 可发生的反应有 、 (填反应类型)。
(3)增塑剂(DEHP)存在如下图所示的转化关系,其中A 是PX的一种同分异构体。

① B 的苯环上存在2 种不同化学环境的氢原子,则B 的结构简式是 。
② D 分子所含官能团是 (填名称)。
③ C 分子有1个碳原子连接乙基和正丁基,DEHP的结构简式是
(4)F 是B 的一种同分异构体,具有如下特征:
a.是苯的邻位二取代物;b.遇FeCl3溶液显示特征颜色;c.能与碳酸氢钠溶液反应。
写出F 与NaHCO3溶液反应的化学方程式
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 的
的![]() 溶液加水稀释100倍后,pH______
溶液加水稀释100倍后,pH______![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ,原因是______
,原因是______![]() 用离子方程式和必要的文字说明
用离子方程式和必要的文字说明![]() ;pH相等的NaOH溶液与
;pH相等的NaOH溶液与![]() 溶液,分别加热到相同的温度后
溶液,分别加热到相同的温度后![]() 溶液的pH______NaOH溶液的
溶液的pH______NaOH溶液的![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ;
;
![]() 相等时,
相等时,![]() 三种溶液中
三种溶液中![]() 由大到小的顺序为______;
由大到小的顺序为______;
![]() 等体积、等浓度的氢氧化钠与醋酸混合后溶液呈 ______ 性,溶液中
等体积、等浓度的氢氧化钠与醋酸混合后溶液呈 ______ 性,溶液中![]() ______
______ ![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ;
;![]() 的氢氧化钠与
的氢氧化钠与![]() 的醋酸等体积混合后溶液呈______性,溶液中
的醋酸等体积混合后溶液呈______性,溶液中![]() ______
______ ![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() ;
;
![]() ,用
,用![]() 溶液滴定
溶液滴定![]() 某一元酸HA溶液所得滴定曲线如图。
某一元酸HA溶液所得滴定曲线如图。
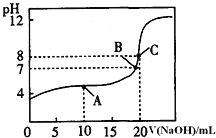
![]() 为减小实验误差,由图可知滴定时指示剂应选用______
为减小实验误差,由图可知滴定时指示剂应选用______![]() 填“石蕊”、“酚酞”、“甲基橙”
填“石蕊”、“酚酞”、“甲基橙”![]() ;
;
![]() 、B、C三点所示溶液导电能力最强的是 ______ 点对应的溶液;
、B、C三点所示溶液导电能力最强的是 ______ 点对应的溶液;
![]() ,A点的离子浓度大小关系是 ______ .
,A点的离子浓度大小关系是 ______ .
查看答案和解析>>
科目: 来源: 题型:
【题目】芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E的转化关系如图所示:
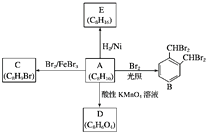
回答下列问题:
(1)A的化学名称是________;E属于________(填“饱和烃”或“不饱和烃”)。
(2)A→B的反应类型是__________,在该反应的副产物中,与B互为同分异构体的副产物的结构简式为________________。
(3)A→C的化学方程式为________________________________________________。
(4)A与酸性KMnO4溶液反应可得到D,写出D的结构简式:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用稀硝酸与铜反应制备NO气体,如果采用图Ⅰ装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不是十分理想,因为观察到的现象不能有力证明反应产物是NO。有人设计了图Ⅱ装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果。
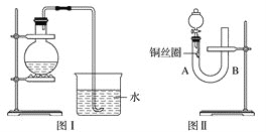
(1)用图Ⅰ装置做实验时,用排水法收集到的气体的颜色为_____色;实验过程中由于______,不易观察到____________生成,从而不能有力证明反应产物是NO。
(2)用图Ⅱ装置做实验时,将有关操作补充完全:
①将分液漏斗的活塞打开,从U形管的B侧管口注入稀硝酸,一直注到____________为止。
②关闭活塞,用酒精灯在U形管的A侧加热,当______时,立即撤去酒精灯。
(3)根据图Ⅱ装置的实验完成下列问题:
①反应在什么情况下可以自动停止?________________________。
可在何处观察到无色的NO气体?____________________________________________。
②如果将分液漏斗的活塞慢慢打开,可立即观察到哪些明显现象?_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子能在指定溶液中,能大量共存的是![]()
![]() 无色溶液中:
无色溶液中:![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]()
![]() 的溶液中:
的溶液中:![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]()
![]() 水电离的
水电离的![]() 浓度
浓度![]() 的溶液中:
的溶液中:![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]()
![]() 加入Mg能放出
加入Mg能放出![]() 的溶液中:
的溶液中:![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]()
![]() 使石蕊变红的溶液中:
使石蕊变红的溶液中:![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]()
![]() 中性溶液中:
中性溶液中:![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() .
.
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验现象所对应的离子方程式不正确的是( )
选项 | 实验 | 现象 | 离子方程式 |
A |
| 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I—+O2=2I2+2H2O |
B |
| 溶液由浅绿色变为红色 |
|
C |
| 溶液由黄绿色变为无色 |
|
D |
| 有白色沉淀生成,溶液由红色变无色 |
|
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com