
科目: 来源: 题型:
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。
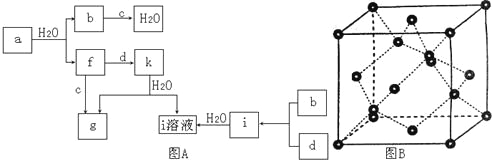
回答下列问题:
(1)图B对应的物质名称是_________,其晶胞中的原子数为______,晶体类型为_______。
(2)d中元素的原子核外电子排布式为_______。
(3)图A中由二种元素组成的物质中,沸点最高的是______,原因是______,该物质的分子构型为_________,中心原子的杂化轨道类型为_________。
(4)图A中的双原子分子中,极性最大的分子是_________。
(5)k的分子式为_________,中心原子的杂化轨道类型为_________,属于_________分子(填“极性”或“非极性”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】取3mL 5mol·L-1 H2O2溶液,加入少量MnO2粉末,2min时c(H2O2)降为1mol·L-1。下列说法不正确的是
A.2min内,v(H2O2) =2molL-lmin-1
B.MnO2是催化剂,能加快H2O2的分解速率
C.升高温度或增大H2O2的浓度,均能加快H2O2的分解速率
D.若将5 molL-l H2O2溶液的体积增至6mL,则H2O2的分解速率增至原来的2倍
查看答案和解析>>
科目: 来源: 题型:
【题目】某绿色溶液A含有H+、Na+、Mg2+、Fe2+、Cu2+、SO42-、Clˉ、CO32-和HCO3-离子中的若干种。取该溶液进行如下实验(已知Ag2SO4微溶于水,可溶于酸):①向溶液中滴加少量Ba(OH)2溶液,过滤,得到不溶于酸的白色沉淀和绿色滤液B;②取滤液B,先用HNO3酸化,再滴加0.001 mol·Lˉ1AgNO3溶液,有白色沉淀生成。下列说法不正确的是
A.溶液A中不存在Mg2+、CO32-和HCO3-,不能确定Na+的存在
B.溶液A中存在Fe2+与Cu2+中的一种或两种
C.第②步生成的白色沉淀中只有AgCl,没有Ag2CO3
D.溶液A中一定存在H+、SO42-和Clˉ
查看答案和解析>>
科目: 来源: 题型:
【题目】化学实验装置的科学设计是实验是否取得预期效果的关键。请回答下列有关实验装置的相关问题:

I.图一中A为教材制备乙酸乙酯的实验装置,甲同学认为图一中B装置比A要好,则冷却水应从______口进入;乙同学认为图一中C装置效果更好,理由是_______。
Ⅱ.“摩尔盐”[(NH4)2Fe(SO4)26H2O]是分析化学中的重要试剂。已知:摩尔盐隔绝空气加热至500℃时可完全分解。某学习小组欲探究其分解产物。
(1)[提出猜想]小组同学认为分解产物可能有以下几种情况:
A.Fe2O3、SO2、NH3、H2O B.FeO、SO3、NH3、H2O
C.FeO、SO2、NH3、H2O D.Fe2O3、SO3、SO2、NH3、H2O
根据所学知识,可确定_________不成立(填序号)
(2)[药品验纯]甲同学提出可以用湿润的红色石蕊试纸、稀盐酸和_________溶液检验出“摩尔盐”中的三种离子;取一定量的“摩尔盐”配成溶液,取少量溶液置于试管中,向其中滴加_______(填试剂名称和实验现象),则“摩尔盐”未因氧化而变质。
(3)[实验探究]为检验分解产物,甲同学设计了如下实验装置。
①取一定量“摩尔盐”置于加热管A中,加热至分解完全后打开K,再通入N2,目的是________。
②实验中观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀.C中发生反应的离子方程式为________。
③实验验证取A中残留物少许加入稀硫酸溶解,再滴入KMnO4稀溶液,不褪色证明产物不含______。
(4)[实验结论与反思]通过实验现象和认真反思,上述猜想中一定正确的是______。(填序号)
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
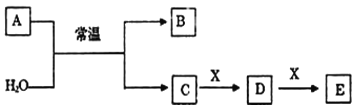
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:___。
(2)若A为淡黄色粉末,X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种稀溶液,可选择的试剂为___(填代号)。
A.盐酸 B.BaCl2溶液 C.Ca(OH)2溶液
(3)若A为非金属氧化物,B为气体,遇空气会变红棕色,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2CuCl+2CO+2H2O=Cu2Cl22CO2H2O。回答下列问题:
(1)Cu在元素周期表中属于______(选填“s”、“p”、“d”或“ds”)区元素。
(2)C、N、O三种原子中的第一电离能最大的是____________。NO3- 离子的空间构型是______。
(3)CO与N2互称等电子体。下表为CO和N2的有关信息。
键的类型 | A-B(单键) | A=B(双键) | A≡B(叁键) | |
键能(kJ/mol) | CO | 351 | 803 | 1071 |
N2 | 159 | 418 | 946 | |
根据表中数据,说明CO比N2活泼的原因是________________________。
(4)Cu2Cl22CO2H2O是一种配合物,其结构如图所示:
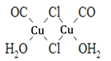
①该配合物中氯原子的杂化方式为_________________________。
②该配合物中,CO作配体时配位原子是C而不是O的原因是______________________。
③1molCu2Cl22CO2H2O含有的______________个σ键。
查看答案和解析>>
科目: 来源: 题型:
【题目】用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx)转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其转化过程如图所示。下列说法不正确的是
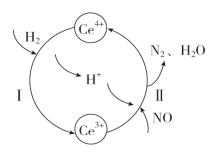
A.反应Ⅰ的离子反应方程式为2Ce4++H2===2Ce3++2H+
B.反应前溶液中c(Ce4+)一定等于反应后溶液中的c(Ce4+)
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为1∶2
D.反应过程中混合溶液内Ce3+和Ce4+的总数一定保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】铜与浓硝酸反应的方程式为:![]()
(1)在该反应中,被还原的元素是_______,氧化产物是_______。
(2)在方程式标出电子转移的方向和数目_______。
(3)若有32g铜参与反应,被还原的硝酸有_______mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与社会生活密切相关,下列说法正确的是( )
A.军舰船底镶嵌锌块作正极,以防船体被腐蚀
B.汽车尾气中NO和CO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢
C.金属冶炼过程是金属离子得电子变成金属单质的氧化过程
D.PM2.5颗粒![]() 微粒直径约为2.5×106m)分散在空气中形成气溶胶
微粒直径约为2.5×106m)分散在空气中形成气溶胶
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是![]()
A.合成纤维、淀粉、蛋白质和地沟油都是高分子化合物
B.“火树银花”中的焰火实质上是金属元素的焰色反应
C.去皮苹果放在空气久置变黄与纸张变黄原理相似
D.煤经过气化、液化和干馏等物理变化过程,可以转化为清洁能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com