
科目: 来源: 题型:
【题目】图中曲线分别表示相同温度下,压强为P1、P2条件下发生可逆反应:mX(g)+nY(g)![]() 2Z(g)+W(s)的过程。下列说法不正确的是( )
2Z(g)+W(s)的过程。下列说法不正确的是( )
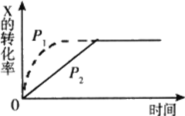
A.P1>P2B.m+n=2
C.m+n=3D.P1、P2下平衡常数相同
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各实验操作中错误的是![]()
![]() 实验室制乙烯时,温度计水银球应插入混合液中
实验室制乙烯时,温度计水银球应插入混合液中
![]() 配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止
配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止
![]() 配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止
配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止
![]() 用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱
用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱
![]() 做过银镜反应的试管用浓硝酸清洗
做过银镜反应的试管用浓硝酸清洗
![]() 卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类
卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类
![]() 若苯酚不慎沾到皮肤上,应立即用酒精洗涤
若苯酚不慎沾到皮肤上,应立即用酒精洗涤
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应:![]() 在恒容容器中进行,达到平衡状态的标志是( )
在恒容容器中进行,达到平衡状态的标志是( )
①单位时间内生成![]() 的同时生成
的同时生成![]()
②单位时间内生成![]() 的同时生成
的同时生成![]()
③用![]() 、
、![]() 、
、![]() 的物质的量浓度变化表示的反应速率之比为2∶2∶1的状态
的物质的量浓度变化表示的反应速率之比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A.①④⑥B.②③⑤C.①③④D.①②③④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)亚铁氰化钾是食盐中常用的抗结剂,其化学式为K4[Fe(CN)6]。
①CN-的电子式是__________;1 mol该配离子中含σ键数目为________。
②该配合物中存在的作用力类型有_________(填字母)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(2)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其晶胞,晶胞边长为a nm。则硼原子与磷原子最近的距离为__________。 用M g·mol-1表示磷化硼的摩尔质量,NA表示阿伏加德罗常数的值,则磷化硼晶体的密度为__________g·cm-3。
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中3原子1的坐标为(1/2,1/2,0),则原子3的坐标分别为________________。
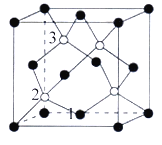
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g) 达到平衡。下列说法正确的是
CH3OH(g) 达到平衡。下列说法正确的是
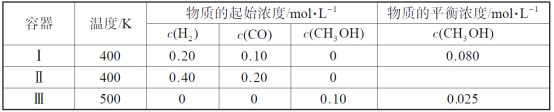
A.该反应的正反应吸热
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C.达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
科目: 来源: 题型:
【题目】若R元素原子的质量数为A,Rm-的核外电子数为x,则w g Rm-所含中子的物质的量为( )
A.(A-x+m) molB.(A-x-m) mol
C.![]() (A-x+m) molD.
(A-x+m) molD.![]() (A-x-m) mol
(A-x-m) mol
查看答案和解析>>
科目: 来源: 题型:
【题目】反应aA(g)+bB(g)![]() cC(g) (ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g) (ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
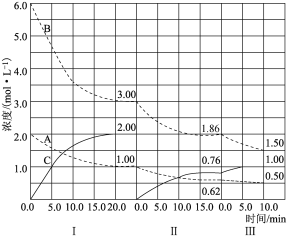
(1)第Ⅰ阶段达平衡时的平衡常数K=___。
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从小到大排列次序为___;
(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最大的是___;
(4)由第Ⅰ阶段平衡到第Ⅱ阶段平衡,平衡移动的方向是___,采取的措施是___;
(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低:T2__T3(填“>”“<”“=”),判断的理由是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】电化学的应用十分广泛,是现代生产、生活、国防,乃至整个人类生活不可缺的物质条件。请根据所给材料回答下列问题:
(1)请结合组成原电池的条件,将氧化还原反应:2Fe3++Cu=2Fe2++Cu2+设计成一个原电池。

①电解液:___,
②正极材料:___;
③负极反应式:___。
(2)用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池。电池充放电时的总反应为:NiO(OH)+MH![]() Ni(OH)2+M
Ni(OH)2+M
①电池放电时,负极的电极反应式为___。
②当该电池充电时,与外电源正极连接的电极上发生的反应是___。
A.H2O的还原 B.NiO(OH)的还原 C.H2的氧化 D.Ni(OH)2的氧化
(3)按如图电解饱和食盐水溶液,写出该电解池中发生反应的总反应式:___;将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是:___。

查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示,利用海水可提取很多重要的化工原料。
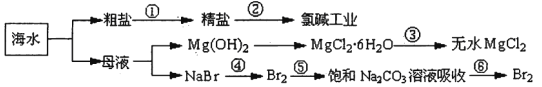
下列有关说法正确的是.( )。
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.第②步中工业上可采用石墨为阴极,铁为阳极,采用阳离子交换膜的电解装置
C.第③步中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2
D.在第④步中溴元素被氧化,第⑤、⑥步中既有溴元素被氧化也有溴元素被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com