
科目: 来源: 题型:
【题目】下列说法正确的是![]()
![]()
A.海水淡化的常用方法有蒸馏法、电渗析法和过滤法
B.pH相等的三种溶液:![]() 溶液
溶液![]() 溶液
溶液![]() 溶液,其浓度大小顺序为
溶液,其浓度大小顺序为![]()
C.在![]() 和
和![]() 的混合溶液中加入
的混合溶液中加入![]() 产生黑色沉淀,证明
产生黑色沉淀,证明![]()
D.侯式制碱法的化学方程式为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】向浓度相等、体积均为100 mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,逐滴加入0.1 mol/L的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示。

(1)A曲线表明,原溶液通入CO2 ________mL(标准状况)。
(2)B曲线表明,原溶液通入CO2后,所得溶液中溶质的物质的量之比为__________。
(3)原NaOH溶液的物质的量浓度为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物F是一种食品保鲜剂,可按如下途径合成:

已知:RCHO+CH3CHO![]() RCH(OH)CH2CHO。
RCH(OH)CH2CHO。
试回答:
(1)A的结构简式是_________,E→F的反应类型是_________。
(2)B→C反应的化学方程式为_____________。
(3)C→D所用试剂和反应条件分别是_________。E中官能团的名称是________________。
(4)检验F中碳碳双键的方法是_________________________。
(5)连在双键碳上的羟基不稳定,会转化为羰基,则D的同分异构体中,只有一个环的芳香族化合物有______种(除D外)。其中苯环上只有一个取代基,核磁共振氢谱有4个峰,峰面积比为3∶2∶2∶1的同分异构体的结构简式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于水溶液中的离子平衡,下列说法正确的是
A.往![]() 稀溶液中加入NaOH固体,溶液中
稀溶液中加入NaOH固体,溶液中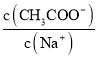 变大
变大
B.等物质的量浓度的![]() 、
、![]() 、
、![]() 三种溶液中,
三种溶液中,![]() 的大小顺序为:
的大小顺序为:![]()
C.常温下![]() 的
的![]() 溶液和
溶液和![]() 的NaOH溶液等体积混合,溶液中离子浓度大小顺序为:
的NaOH溶液等体积混合,溶液中离子浓度大小顺序为:![]()
D.![]() 的
的![]() 溶液中:
溶液中:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】把0.6mol X气体和0.4mol Y气体混合于2L容器中,发生反应:3X(g)+Y(g)== nZ(g)+2W(g),5min末已生成0.2mol W,若测知以Z浓度变化来表示的平均速率为0.03mol·L﹣1·min﹣1,计算:
(1)n的值为____;
(2)前5min内用X表示的反应速率_____;
(3)5min末Y的浓度_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将![]() 缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人
缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加人![]() 溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )
溶液,整个过程中pH的变化如图所示,下列有关叙述正确的是( )

A.曲线③④段有离子反应:![]()
B.可依据②处数据计算所溶解的![]()
C.③处表示氯气与氢氧化钠溶液恰好反应完全
D.①处![]() 约为
约为![]() 处
处![]() 的两倍
的两倍
查看答案和解析>>
科目: 来源: 题型:
【题目】三氯氧磷(POCl3)是重要的基础化工原料,广泛用于制药、染化、塑胶助剂等行业。某兴趣小组模拟PCl3直接氧化法制备POCl3,实验装置设计如下:
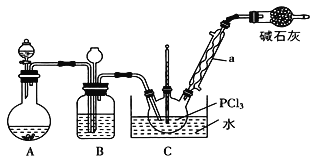
有关物质的部分性质如下表:
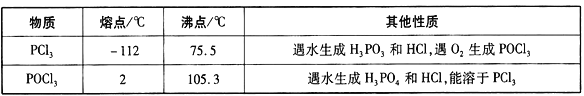
回答下列问题:
(1)仪器a的名称是_____________。装置A中发生反应的化学方程式为_______。
(2)装置C中制备POCl3的化学方程式为________________________________。
(3)C装置控制反应在60~65℃进行,其主要目的是_______________________。
(4)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
I.取xg产品于锥形瓶中,加入足量NaOH溶液,待完全反应后加稀硝酸至溶液显酸性;
II.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀;
III.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
IV.加入指示剂,用c mol·L-1 NH4SCN溶液滴定过量Ag+至终点,记下所用体积为VmL。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是(填序号)________,滴定终点的现象为_____________。
a.酚酞 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②Cl元素的质量分数为(列出算式)________________。
③若取消步骤III,会使步骤IV中增加一个化学反应,该反应的离子方程式为________;该反应使测定结果________(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分:(不得用a~h字母回答)元素周期表有7个横行,每一个横行称为“周期”,周期序数=电子层数;元素周期表共有18列,每一列称为 “族”,下表中的7列为主族元素,分别用罗马数字Ⅰ、Ⅱ、……表明族序数,族序数=最外层电子数。
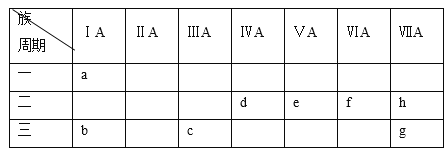
根据a~h各元素的性质,选择相应的化学符号、化学式或化学方程式填空:
(1)单质氧化性最强的是__________,酸性最强的含氧酸是_____________。
(2)写出e的碱性气态氢化物的电子式_____,将它和化合物df 2通入饱和食盐水发生反应的化学方程式是_____。
(3)最高价氧化物对应的水化物中,碱性最强的是___________。
(4)在b、c、g、h中,常见离子半径最大的是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关系图中,A 是一种正盐,B 是气态氢化物,C 是单质,F 是强酸。当 X 无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当 X 是强碱时,过量的 B 跟 Cl2 反应除生成 C 外,另一产物是盐酸盐。
下列说法中不正确的是( )
![]()
A.当 X 是强酸时,A、B、C、D、E、F中均含同一种元素,F 可能是 H2SO4
B.当 X 是强碱时,A、B、C、D、E、F中均含同一种元素,F 是 HNO3
C.用 O2 代替 Cl2, 也能与 B 反应生成 C 物质
D.当 X 是强酸时,C 在常温下是一种易溶于酒精的固体
查看答案和解析>>
科目: 来源: 题型:
【题目】Fe2(SO4)3溶液可除去煤中以黄铁矿(FeS2)形式存在的硫元素,反应如下:
______FeS2 + ______Fe2(SO4)3 +______H2O →______FeSO4 + ______H2SO4
(1)试配平反应的化学方程式,并用单线桥标出电子转移方向及数目_____;还原剂是_______,还原产物是_________,被还原的元素是__________。
(2)Fe2(SO4)3溶液呈_____性,用离子方程式解释其原因________。
(3)检验上述反应中Fe2(SO4)3是否消耗完的实验方案:_________________________。
(4)该方法的优点之一是Fe2(SO4)3易再生。向反应后的溶液中通入__________,就能达到使Fe2(SO4)3再生的目的,方便且价廉。
(5)实验室.配制一定量FeSO4溶液时,需加入少量_____和_______其目的是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com