
科目: 来源: 题型:
【题目】氮化钙(Ca3N2)是一种重要的化学试剂,通常条件下为棕色易水解的固体。某小组在实验室制备氮化钙并测定其纯度,设计如下实脸(夹持装置略去):
I.氮化钙的制备。
(1)加热条件下,钙和氮气制备氮化钙的反应方程式为_________。

(2)按气流由左到右的方向,上述装置合理的连接顺字为__________(填仪器接口字母)。
(3)按连接好的装置进行实验。
①实验步骤如下,检查装置气密性,加入药品:_______(请按正确顺序填入下列步骤的字母标号)。
a.点燃装置C处酒精灯,反应一段时间
b.打开分液漏斗活塞
c.点燃装置A处酒精灯
d.熄灭装置A处酒精灯
e.熄灭装置C处酒精灯
f.关闭分液漏斗活塞
②装置B的作用为_________。
③装置C的硬质玻璃管中的现象为_________。
(4)设计实验证明Ca3N2中混有钙单质:_______________。
II.测定氮化钙纯度。
i.称取4.0g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1 .00mol/L盐酸中,充分反应后,将所得溶液稀释到200 . 00 mL;
ii.取20 . 00mL稀释后的溶液,用0 . 2mol/LNaOH标准溶液滴定过量的盐酸,到终点时消耗标准溶液25 . 00 mL。
(5)所取固体中氮化钙的质量分数为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表列出了①~⑨九种元素在周期表中的位置:
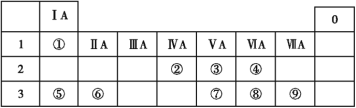
请按要求回答下列问题。
(1)元素③的名称是__,元素⑨的元素符号是____,元素④形成的单质具有____(填“氧化性”或“还原性”)。
(2)元素⑦⑧⑨的气态氢化物的稳定性由弱到强的顺序:____(用化学式表示)。
(3)写出一条能说明元素⑤的金属性比元素⑥强的事实:_____。
(4)写出元素⑤形成的单质与水反应的离子方程式:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】通常情况下,氯化钠、氯化铯、二氧化碳和二氧化硅的晶体结构分别如下图所示
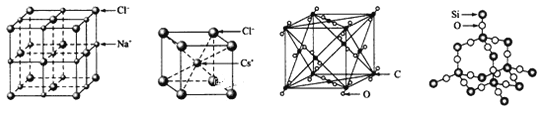
(1) 在NaCl的晶胞中,与Na+最近且等距的Na+有_____个,在NaCl的晶胞中有Na+_____个,Cl-____个
(2)在CsCl的晶胞中,Cs+与Cl-通过_________结合在一起。
(3) 1mol二氧化硅中有______mol硅氧键。
(4)设二氧化碳的晶胞密度为a g/cm3,写出二氧化碳的晶胞参数的表达式为____n m (用含NA的代数式表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】一种新型高效净水剂PAFC--聚合氯化铁铝![]()
![]() ,
,![]() ,
,![]() 广泛用于生活用水的净化和废水的净化
广泛用于生活用水的净化和废水的净化
![]() 为测定PAFC中Al的含量,采用如图所示流程进行.
为测定PAFC中Al的含量,采用如图所示流程进行.
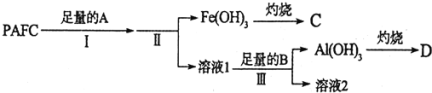
回答下列问题:
![]() 有关PAFC的说法正确的是 ______
有关PAFC的说法正确的是 ______
A PAFC中铁显![]() 价
价
B PAFC用于净化饮用水时,可以除去水中所有的有害物质
C PAFC用于净水时,比用相同量的氯化铝和氯化铁对水的pH改变小
D PAFC在强酸性或强碱性溶液中都能稳定存在
![]() 步骤I中的试剂A是 ______
步骤I中的试剂A是 ______ ![]() 填“氨水”或“氢氧化钠溶液”
填“氨水”或“氢氧化钠溶液”![]()
![]() 步骤III的离子方程式为 ______ .
步骤III的离子方程式为 ______ .
![]() 实验室进行“灼烧”时所需的陶瓷仪器有 ______ .
实验室进行“灼烧”时所需的陶瓷仪器有 ______ .
![]() 溶液2中存在的电荷守恒式为 ______ ;向溶液2中滴加少量NaOH镕液,则
溶液2中存在的电荷守恒式为 ______ ;向溶液2中滴加少量NaOH镕液,则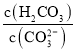 ______填“变大”、“变小”或“不变”
______填“变大”、“变小”或“不变”![]() .
.
![]() 已知C和某一金属在高温下发生反应可用于焊接钢轨,某同学在实验室中进行此反应,反应结束后将所得固体溶于足量的稀硫酸,滴加KSCN溶液无明显现象,由此该同学确定该固体混合物中无
已知C和某一金属在高温下发生反应可用于焊接钢轨,某同学在实验室中进行此反应,反应结束后将所得固体溶于足量的稀硫酸,滴加KSCN溶液无明显现象,由此该同学确定该固体混合物中无![]() ,他的判断是否正确?说明理由.
,他的判断是否正确?说明理由.![]() 可用文字或离子方程式解释理由
可用文字或离子方程式解释理由![]() .______ .
.______ .
![]() 有资料介绍:溶液中铝元素以氢氧化物
有资料介绍:溶液中铝元素以氢氧化物![]() 用
用![]() 表示
表示![]() 形式存在的pH范围是
形式存在的pH范围是![]() 现有A、B两种均含铝元素形成的某种离子溶液,其pH分别为1、13,两溶液等体积混合时反应的离子方程式为 ______ .
现有A、B两种均含铝元素形成的某种离子溶液,其pH分别为1、13,两溶液等体积混合时反应的离子方程式为 ______ .
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.12.4 g白磷(P4)中所含的P-P键数目为0.6 NA
B.40 g SiC晶体中含有SiC分子的数目为NA个
C.1 mol麦芽糖完全水解后产生的葡萄糖分子数目为NA
D.标准状况下,2 mol Na2O2与44.8 L SO2完全反应,转移的电子数目为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.电离平衡常数可以表示弱电解质的相对强弱
B.电离平衡常数受溶液浓度的影响
C.H2CO3的电离常数表达式:K=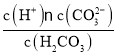
D.电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大
查看答案和解析>>
科目: 来源: 题型:
【题目】I.被誉为改变未来世界的十大新科技之一的燃料电池。 右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.

试回答下列问题:
(1)燃料电池的优点是________;电解质溶液中的OH-移向______极(填“负”或“正”).
(2)写出氢氧燃料电池工作时正极反应式:_______________________。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________.
(4)利用该装置可以处理氮的氧化物和NH3 尾气,总反应为:6NO2 +8NH3=7N2+12H2O,负极反应式为__________。
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为________________;
(2)通过导线的电子数为__________(用NA表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.写出下列有机物的系统命名或结构简式:
(1)![]() ____________。
____________。
(2)CH3CH(CH3)C(CH3)2CH2CH3____________。
(3) 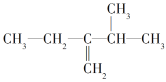 ________。
________。
Ⅱ.食品安全关系着国民生计,影响食品安全的因素很多。
(1)聚偏二氯乙烯(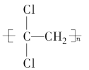 )具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
)具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
(2)劣质植物油中的亚油酸[CH3(CH2)4—CH=CH—CH2—CH=CH—(CH2)7COOH]含量很低。下列关于亚油酸的说法中,正确的是________。
A.分子式为C18H34O2 B.一定条件下能与甘油(丙三醇)发生酯化反应
C.能和NaOH溶液反应 D.能使酸性KMnO4溶液褪色
(3)假酒中甲醇(CH3OH)含量超标,请写出Na和甲醇反应的化学方程式:_______。
(4)劣质奶粉中蛋白质含量很低。蛋白质水解的最终产物是________________。
(5)在淀粉中加入吊白块制得的粉丝有毒。淀粉最终的水解产物是葡萄糖。请设计实验证明淀粉已经全部水解,写出操作、现象和结论:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异
B.可用蘸有浓氨水的玻璃棒检验输送氯气的管道是否漏气
C.白炽灯工作时,电能全部转化为光能
D.日本福岛核电站核泄漏事故提醒我们不要开发新能源,要大力挖掘化石能源
查看答案和解析>>
科目: 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O)简称三盐,白色或微黄色粉末,稍带甜味、有毒。200℃以上开始失去结晶水,不溶于水及有机溶剂。可用作聚氯乙烯的热稳定剂。以100.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。
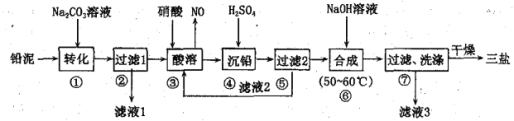
已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13。请回答下列问题
(1)步骤①转化的目的是将PbSO4转化为PbCO3,反应的离子方程式为___________________。
(2)滤液3中的主要溶质为_____________(填化学式)。
(3)步骤③酸溶时,铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为____________________。
(4)滤液2中可循环利用的溶质为___________(填化学式)。若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol·L-1,则此时c(SO42-)为___________mol·L-1
(5)步骤⑥合成三盐的化学方程式为____________________________。若得到纯净干燥的三盐49.50 t,假设铅泥中的铅元素有80.00%转化为三盐,则铅泥中铅元素的质量分数为_____。[已知:三盐(3PbO·PbSO4·H2O)的相对分子质量为990,注意保留正确的有效数字]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com