
科目: 来源: 题型:
【题目】298K时,碳酸、醋酸和亚硫酸的电离平衡常数见下表:
名称 | 碳酸 | 醋酸 | 亚硫酸 |
电离常数(298K) | K1=4.4×10–7 K2=4.7×10–11 | K=1.8×10–5 | K1=1.3×10–2 K2=6.2×10–8 |
(1)298K时,碳酸、醋酸和亚硫酸,从强到弱的顺序_______________________.(用化学式表示)
(2)用离子方程式表示Na2SO3溶液显碱性的原因_______________________。
(3)25℃时,相同浓度的CH3COONa溶液的碱性________Na2CO3溶液的碱性(填“>”“<”或“=”)。
(4)向醋酸溶液中加少量NaOH溶液,醋酸的电离平衡常数________(填“增大”、“减小”、“不变”).
(5)已知常温下:某NaHSO3溶液的pH=5,则该NaHSO3溶液中c(H2SO3) ________ c(SO32-)(填“>”“<”或“=”).
(6)25℃时,PH=4的亚硫酸溶液与PH=10的NaOH溶液等体积混合后,溶液显_________性.
A.酸性 B.碱性 C.中性 D.无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)M与Q是同素异形体,由M=Q;△H = -19KJ/mol可知,M比Q________(填稳定、不稳定)。
(2)已知:![]()
![]()
请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式_________________。
(3)在与外界隔离的体系中,自发过程将导致体系的熵__________,(填“增大”、“减小”、“不变”);对于同一种物质,________时熵值最大(填“固态”、“液态”、“气态”)。
(4)某工厂实验室用CO和H2制备CH3OH,其原理为:![]() 该温度下的化学平衡常数表达式__________________;若在298K、398K时化学平衡常数分别为K1、K2,则K1 ___ K2(填“>”、“<”、“=”)。
该温度下的化学平衡常数表达式__________________;若在298K、398K时化学平衡常数分别为K1、K2,则K1 ___ K2(填“>”、“<”、“=”)。
(5)500℃条件下,对于反应![]() ,K=2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正) ______ v(逆)(填“>”“<”或“=”)。
,K=2.33 ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正) ______ v(逆)(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于各图像的解释或结论不正确的是( )
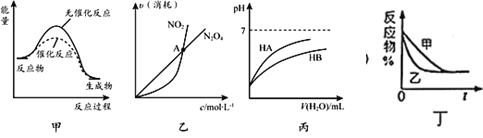
A.由甲可知:使用催化剂不影响反应热
B.由乙可知:对于恒温恒容条件下的反应![]() ,A点为平衡状态
,A点为平衡状态
C.由丙可知:等浓度的HA溶液和HB溶液,其pH前者小于后者
D.图丁表示压强对可逆反应![]() 的影响(横坐标代表时间),乙的压强比甲的压强大
的影响(横坐标代表时间),乙的压强比甲的压强大
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g) ![]() 2SO3(g)达到平衡后改变下述条件,SO3(g)平衡浓度不改变的是
2SO3(g)达到平衡后改变下述条件,SO3(g)平衡浓度不改变的是
A. 保持温度和容器体积不变,充入1mol SO3(g)
B. 保持温度和容器内压强不变,充入1molO2(g)
C. 保持温度和容器内压强不变,充入1mol SO3(g)
D. 保持温度和容器内压强不变,充入1mol Ar(g)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,隔板I固定不动,活塞II可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)![]() xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )
xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )

A. 若x=3,达到平衡后A的体积分数关系为:![]()
B. 若x<3,C的平衡浓度关系为:c(M)<c(N)
C. 若x>3,达到平衡后B的转化率关系为:![]()
D. x不论为何值,平衡时M、N中的平均相对分子质量都相等
查看答案和解析>>
科目: 来源: 题型:
【题目】温度为T时,向2VL的密闭容器中充入一定量的A和B,发生反应:![]() ;
;![]() ,容器中A、B、D的物质的量浓度随时间的变化如图所示。下列说法正确的是
,容器中A、B、D的物质的量浓度随时间的变化如图所示。下列说法正确的是
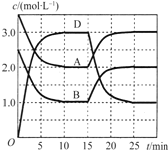
A.反应在前10min的平均反应速率![]()
B.反应至15min时,改变的条件是降低温度
C.若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动
D.该反应的平衡常数表达式
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度的恒容绝热闭容器中进行如下可逆反应![]() 下列叙述中,能说明反应已达到化学平衡状态的是
下列叙述中,能说明反应已达到化学平衡状态的是
①A、B、C的分子数之比为1:2:3
②单位时间内生成 amolA,同时生成3amolC
③![]() 的物质的量浓度不再变化
的物质的量浓度不再变化
④![]() :
:![]() :
:![]() :2:3
:2:3
⑤混合气体的密度不再变化
⑥容器内的压强不再变化
A.②③⑥B.③④⑥C.②③D.①②⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】温度相同,浓度均为0.1 mol·L-1的:①(NH4)2CO3,②(NH4)2Fe(SO4)2,③氨水,④NH4NO3,⑤ NH4HSO4溶液,它们中的c(NH![]() )由大到小的排列顺序是( )
)由大到小的排列顺序是( )
A. ②⑤④①③ B. ③⑤②④①
C. ②①⑤④③ D. ⑤②①④③
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是____。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备实验:
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。请评价该操作是否正确____。
②乙同学直接加热饱和FeCl3溶液,请评价是否正确____。
③丙同学向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确__。
(3)写出制备Fe(OH)3胶体的化学方程式:_____。证明有Fe(OH)3胶体生成的实验操作是________。利用的胶体性质是___。
(4)Fe(OH)3胶体稳定存在的主要原因是___。
A.胶粒直径小于1 nm B.胶粒带正电荷
C.胶粒作布朗运动 D.胶粒能透过滤纸
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,将2mol![]() 和
和![]() 充入10L恒容密闭容器中,发生反应
充入10L恒容密闭容器中,发生反应![]() ,5min时达到平衡,测得反应放热
,5min时达到平衡,测得反应放热![]() 下列说法错误的是
下列说法错误的是![]()
A.![]() 内,用
内,用![]() 表示的平均反应速率
表示的平均反应速率![]()
![]()
B.反应物浓度的比值不变时,该反应达到平衡状态
C.若增大![]() 的浓度,
的浓度,![]() 的转化率增大
的转化率增大
D.条件不变,若起始时充入4mol![]() 和
和![]() ,平衡时放出的热量大于
,平衡时放出的热量大于![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com