
科目: 来源: 题型:
【题目】蚀刻铜制线路板的蚀刻液种类很多:酸性蚀刻液,如![]() 蚀刻溶液、H2O2-盐酸及CuCl2-盐酸
蚀刻溶液、H2O2-盐酸及CuCl2-盐酸![]() 碱性蚀刻液,如
碱性蚀刻液,如![]() 溶液等。回答下列问题:
溶液等。回答下列问题:
(1)写出下列蚀刻液蚀刻铜的离子方程式。
①FeCl3溶液:_______。
②H2O2-盐酸:_______。
③![]() 溶液:_______
溶液:_______![]() 生成
生成![]() 。
。
(2)利用废![]() 蚀刻液
蚀刻液![]() 含
含![]() 、
、![]() 及
及![]() 制备碱性蚀刻液
制备碱性蚀刻液![]() 溶液和
溶液和![]() 的主要步骤包括:用
的主要步骤包括:用![]() 氧化废蚀刻液,通入氨气
氧化废蚀刻液,通入氨气![]() ,固液分离,用盐酸溶解沉淀和
,固液分离,用盐酸溶解沉淀和![]() 的制备。下列实验装置不能达到实验目的的是_______
的制备。下列实验装置不能达到实验目的的是_______![]() 填字母
填字母![]() 。
。
A. 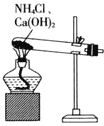 制备
制备![]()
B. 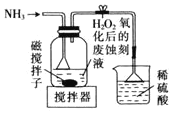 制备
制备![]() 并沉铁
并沉铁
C. 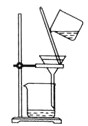 分离
分离![]() 溶液和
溶液和![]() 沉淀
沉淀
D. 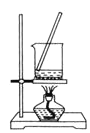 将
将![]() 溶液蒸干制备
溶液蒸干制备![]()
(3)常用水合肼![]() 还原法回收CuCl2-盐酸蚀刻液得到单质铜,先用氢氧化钠溶液中和其中酸并将溶液调至强碱性,然后加入水合肼得纳米铜,该氧化还原反应中氧化剂与还原剂的物质的量之比为_______。
还原法回收CuCl2-盐酸蚀刻液得到单质铜,先用氢氧化钠溶液中和其中酸并将溶液调至强碱性,然后加入水合肼得纳米铜,该氧化还原反应中氧化剂与还原剂的物质的量之比为_______。
(4)文献报道一种回收蚀刻废液中铜并制取胆矾![]() 的主要工艺流程如下:
的主要工艺流程如下:
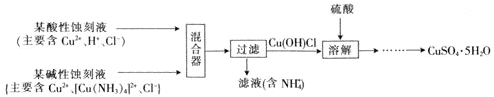
已知:![]() 易与酸反应。
易与酸反应。
![]() 在混合器中,
在混合器中,![]() 的离子方程式为_______。
的离子方程式为_______。
![]() 溶于硫酸的离子方程式为_______。
溶于硫酸的离子方程式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有以下有机物:
①CH3CHO②CH3CH2OH③CH3COOH④CH3COOC2H5
(1)能与Na反应的是______________;
(2)能与NaOH溶液反应的有______________;
(3)既能发生消去反应,又能发生酯化反应的有______________;
(4)能发生银镜反应的有______________;并写出化学方程式:______________
(5)能与NaHCO3溶液反应有气泡产生的是_______________;并写出化学方程式:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式中正确的是( )
A. 用铜电极电解硫酸铜溶液:2Cu2++2H2O![]() 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
B. 0.01 mol·L-1NH4Al(SO4)2溶液与0.02 mol·L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-==2BaSO4↓+Al(OH)3↓+NH3·H2O
C. 偏铝酸钠溶液中通入过量的二氧化碳:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D. NaClO溶液和FeCl2溶液混合:2ClO-+Fe2++2H2O==Fe(OH)2↓+2HClO
查看答案和解析>>
科目: 来源: 题型:
【题目】pH=1的某溶液X中还含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种(忽略水的电离及离子的水解), 取该溶液进行如下实验:

下列有关推断不正确的是
A. 沉淀H为Al(OH)3、BaCO3的混合物
B. 根据上述连续实验不能确定溶液X中是否含有Fe2+、Cl-
C. 溶液X中一定含有NH4+、Al3+、Fe2+、SO42-、H+
D. 若溶液X 为100mL ,产生的气体A为44.5mL(标况),则X中c(Fe2+)=0.06mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)298K时,将20mL3xmol·L-1Na3AsO3、20mL3xmol·L-1I2和20mLNaOH溶液混合,发生反应:AsO![]() (aq)+I2(aq)+2OH-(aq)
(aq)+I2(aq)+2OH-(aq)![]() AsO
AsO![]() (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO![]() )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
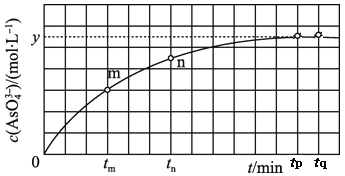
①下列可判断反应达到平衡的是__(填标号)。
a.溶液的pH不再变化
b.v(I-)=2v(AsO![]() )
)
c.![]() 不再变化
不再变化
d.c(I-)=ymol·L-1
e.![]() =
=![]() 不再变化
不再变化
②tn时,v正__v逆(填“大于”“小于”或“等于”)。
③tm时v逆__tn时v逆(填“大于”“小于”或“等于”),理由是__。
④比较产物AsO![]() 在tm~tnmin和tp~tqmin时平均反应速率的大小,前者__;(填大或小或相等)
在tm~tnmin和tp~tqmin时平均反应速率的大小,前者__;(填大或小或相等)
(2)合成氨工厂常通过测定反应前后混合气体的密度来确定氨的转化率。某工厂测得合成塔中N2、H2混合气体的密度为0.5536g/L(标准状况),从合成塔中出来的混合气体在相同条件下密度为0.693g/L(标准状况)。该合成氨厂N2的转化率___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液X含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的几种,已知该溶液中各离子物质的量浓度均为
中的几种,已知该溶液中各离子物质的量浓度均为![]() 不考虑水的电离及离子的水解
不考虑水的电离及离子的水解![]() 。为确定该溶液中含有的离子,现进行了如下的操作:
。为确定该溶液中含有的离子,现进行了如下的操作:
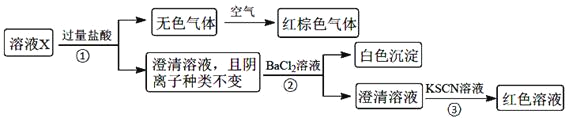
下列说法正确的是![]()
A.无色气体可能是NO和![]() 的混合物
的混合物
B.由步骤![]() 可知,原溶液肯定存在
可知,原溶液肯定存在![]()
C.溶液X中所含离子种类共有4种
D.另取100mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】保护环境已成为当前和未来的一项全球性重大课题.为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提出利用太阳能促使燃料循环使用的构想,如图所示:

过程I可用如下反应表示:
①2CO2![]() 2CO+O2
2CO+O2
②2H2O![]() 2H2+O2
2H2+O2
③2N2+6H2O![]() 4NH3+3O2
4NH3+3O2
④2CO2+4H2O![]() 2CH3OH+3O2
2CH3OH+3O2
⑤2CO+H2O![]() +3O2
+3O2
请回答下列问题:
(1)过程I的能量转化形式为: 能转化为 能.
(2)请完成第⑤个反应的化学方程式
(3)上述转化过程中,△H1和△H2的关系是
(4)断裂1mol化学键所需的能量见表:
共价键 | H﹣N | H﹣O | N≡N | O=O |
断裂1mol化学键所需能量/kJmol﹣1 | 393 | 460 | 941 | 499 |
常温下,N2和H2O反应生成NH3的热化学方程式为
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液X中仅可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是
中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是 ![]()
![]()
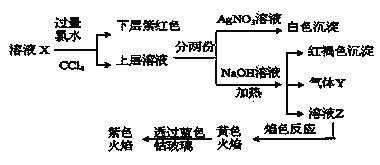
A.该溶液X中可能有![]() 、
、![]()
B.该溶液可能由是硫酸亚铁、碘化钾和氯化铵溶于水后得到的
C.如果气体Y能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有![]()
D.取样溶液Z,滴加氯化钡溶液出现沉淀,可推出X中一定存在![]() 、
、![]() 中的某一种
中的某一种
查看答案和解析>>
科目: 来源: 题型:
【题目】利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下:

(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为 ;“水解”采用90℃而不在室温下进行的原因是 。
(2)“酸溶”时,Al2O3发生反应的离子方程式为 。
(3)“氧化”时,发生反应的离子方程式为________________________________。
(4)“废渣”成分为______________(填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是______________________。
(6)煅烧硫酸铝铵晶体,发生的主要反应为4[NH4Al(SO4)2·12H2O] ![]() 2Al2O3 + 2NH3↑
2Al2O3 + 2NH3↑ + N2↑ + 5SO3↑ + 3SO2↑ + 53H2O,将产生的气体通过如右图所示的装置。则集气瓶中收集到的气体是 (填化学式)。
+ N2↑ + 5SO3↑ + 3SO2↑ + 53H2O,将产生的气体通过如右图所示的装置。则集气瓶中收集到的气体是 (填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】固体粉末可能由SiO2、Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,某学习小组对该固体进行了如下实验。下列判断正确的是( )

A. 气体甲一定能使湿润的红色石蕊试纸变蓝
B. 白色沉淀甲可能是纯净物也可能是混合物
C. 无色溶液乙和无色溶液丙混合一定有无色气体生成,可能有白色沉淀生成
D. 该粉末中一定存在AlCl3、(NH4)2SO4、MgCl2,一定不存在FeCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com