
科目: 来源: 题型:
【题目】有M、V、W、X、Y、Z六种元素,它们的核电荷数依次增大,且都小于20。其中只有X、Z是金属元素;M元素的一种核素原子核内无中子,Z元素原子的最外层只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。V的单质在空气中含量最高。回答下列问题:
(1)M的一种核素中质子数为中子数的![]() ,则该核素的名称为__。
,则该核素的名称为__。
(2)Z的元素符号为__。
(3)X元素的单质与Z的最高价氧化物对应的水化物反应的离子反应方程式为__。
(4)Y的单质在加热条件下与铁反应的化学方程式为__。
(5)非金属性W__Y(填大于或小于)
(6)用一个方程式证明W和Y的非金属性强弱__。
(7)实验室中,V的最高价氧化物对应的水化物可用Y的最高价氧化物对应的水化物制得,写出相应的化学反应方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素。设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
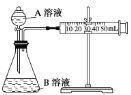
(1)通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小。实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见下表:
序号 | A溶液 | B溶液 |
① | 2mL0.1mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液 |
② | 2mL0.2mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液 |
③ | 2mL0.2mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液和少量MnSO4 |
该实验探究的是___对化学反应速率的影响。在反应停止之前,相同时间内针管中所得CO2的体积由大到小的顺序是___(用实验序号填空)。
(2)某组同学利用如图完成该实验。请分析导管a的两点作用:①___;②___。

查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是元素周期表的一部分,根据①~⑩在周期表中的位置按题目要求回答:
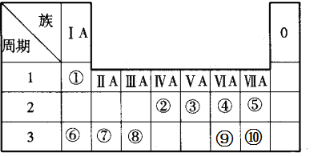
(1)在元素①~⑩中,非金属性最强的元素是__(填元素名称)。
(2)在元素⑥~⑩中,离子半径最小的元素的离子结构示意图为__。
(3)元素⑥⑦⑧的最高价氧化物对应的水化物,按碱性从强到弱的顺序排列是__(用化学式表示)。
(4)用电子式表示元素①和③形成的化合物甲的形成过程__。
(5)为验证ⅦA族部分元素非金属性的递变规律,设计了如图所示装置进行实验,请回答:

①实验室制取单质⑩的化学反应方程式__。
②A中发生反应的离子方程式是__。
③棉花中浸有的NaOH溶液的作用是(用离子方程式表示)__。
④为验证溴与碘非金属性强弱:通入一定量⑩的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到__。
⑤通过此实验,某同学得到结论:“溴比碘非金属性强”,这一说法是否正确,请说明理由___。
⑥化合物乙、丙均由①④⑥⑨四种元素组成,请写出乙与丙发生反应的离子反应方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W四种物质在一定条件下具有如图所示的转化关系,下列判断不正确的是![]()
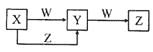
A.若图中反应均为氧化还原反应,当W为金属单质时,则Z可能是![]()
B.若图中反应均为氧化还原反应,当W为![]() 时,则X可能是
时,则X可能是![]()
C.若图中反应均为非氧化还原反应,当W为非金属氧化物时,则X可能是NaOH
D.若图中反应均为非氧化还原反应,Y为![]() ,则W可能为一元强酸或一元强碱
,则W可能为一元强酸或一元强碱
查看答案和解析>>
科目: 来源: 题型:
【题目】研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是
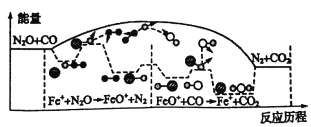
A. 反应总过程△H<0
B. Fe+使反应的活化能减小
C. 总反应若在2L的密闭容器中进行,温度越高反应速率一定越快
D. Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为放热及应
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.下表是某食品包装袋上的说明,从表中的配料中分别选出一种物质在相应的横线上。
品名 | ××× |
配料 | 鲜鸡蛋、精面粉、白砂糖、精炼植物油、奶油、奶粉、食盐、柠檬汁等 |
保质期 | 240天 |
生产日期 | 标于包装袋袋封口上 |
(1)富含蛋白质的物质是___________________________;
(2)富含糖类的物质是____________________________;
(3)富含油脂的物质是____________________________;
(4)富含维生素的物是___________________________。
Ⅱ.钢铁在潮湿的空气里很快就被腐蚀,原因是在钢铁的表面形成了一层电解质溶液的薄膜,跟钢铁里的铁和少量的碳构成无数微小的原电池,请写出两极发生的主要的电极式为:负极________________;正极_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据能量变化示意图,下列说法正确的是

A. 1molC和1molH2O反应生成1molCO和1molH2一定吸收131.3kJ的热量
B. 反应的热化学方程式可表示为C(s)+H2O(g)=CO(g)+H2(g) ΔH=(a-b)KJ/mol
C. 该反应过程反应物断键吸收的能量要小于生成物成键放出的能量
D. 加入适当的催化剂,可以加快正、逆反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组以苯甲酸(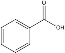 )为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
)为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
密度/g·cm-3 | 0.792 | 1.2659 | 1.0888 |
相对分子质量 | 32 | 122 | 136 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约为0.79g·cm-3),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是______________;写出苯甲酸与甲醇反应的化学方程式:______________。
(2)甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用__________装置(填“甲”或“乙”)

(3)反应物CH3OH应过量,理由是______________。
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称a______________,b______________。
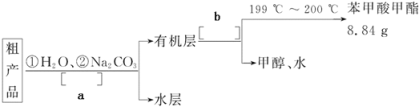
(5)通过计算,苯甲酸甲酯的产率为______________
查看答案和解析>>
科目: 来源: 题型:
【题目】标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图所示。下列分析正确的是

A. a点对应溶液的导电性比d点强
B. 氢硫酸的酸性比亚硫酸的酸性强
C. 向d点对应的溶液中加入Ba(NO3)2溶液,产生BaSO4白色沉淀
D. H2S饱和溶液的物质的量浓度为0.05 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组探究某金属M的性质进行了如下实验,实验过程及现象如图所示。结合实验现象判断,该同学得出的下列结论中正确的是![]()
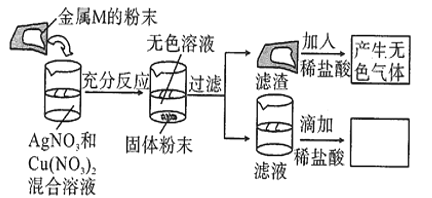
A.加入的金属M可能是铁
B.向滤液中滴加盐酸的实验现象是产生白色沉淀
C.向充分反应后未过滤的混合物中加入稀盐酸,产生的无色气体一定是![]()
D.滤渣中一定含有金属M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com