
科目: 来源: 题型:
【题目】兴趣小组设计实验,测定![]() 与
与![]() 混合物中
混合物中![]() 的质量分数.
的质量分数.
甲方案:
实验步骤为:
![]() 称量空坩埚的质量为
称量空坩埚的质量为![]() ;
;![]() 称量装有试样的坩埚质量为
称量装有试样的坩埚质量为![]() ;
;
![]() 加热;
加热;
![]() 冷却;
冷却;
![]() 称量坩埚和残余物的质量为
称量坩埚和残余物的质量为![]() ;
;
![]() 重复
重复![]() 至
至![]() 操作,直至恒重,质量为
操作,直至恒重,质量为![]() 。
。
(1)坩埚中发生反应的化学方程式___________________________。
(2)计算![]() 质量分数为 _____________________________
质量分数为 _____________________________![]() 表达式
表达式![]() 。
。
乙方案:
准确称取![]() 样品,放锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用
样品,放锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用![]() 的标准盐酸滴定至溶液由粉红色刚好变为无色,达到滴定终点时产物为
的标准盐酸滴定至溶液由粉红色刚好变为无色,达到滴定终点时产物为![]() ,即
,即![]() 。重复上述操作两次。
。重复上述操作两次。
![]() 配制上述盐酸标准溶液100ml,若用
配制上述盐酸标准溶液100ml,若用![]() 进行配制,需用量筒量取该HCl溶液________ml;定容时俯视刻度线,将导致配制的溶液浓度________。
进行配制,需用量筒量取该HCl溶液________ml;定容时俯视刻度线,将导致配制的溶液浓度________。![]() 填“偏高”、“偏低”或“没有影响”
填“偏高”、“偏低”或“没有影响”![]()
(4)根据下表数据,样品中![]() _________。
_________。![]() 保留三位有效数字
保留三位有效数字![]()
滴定次数 | 样品的质量 | 稀盐酸的体积 | |
滴定前刻度 | 滴定后刻度 | ||
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
丙方案:称取![]() 样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
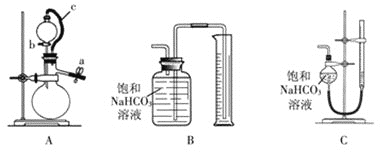
(5)某同学按以下方法检查装置A的气密性:在分液漏斗中加入适量水,如图连接好装置,关闭止水夹a,用止水夹夹住橡皮管c,打开活塞b。若分液漏斗中的水无法持续滴下,试判断装置A是否漏气?________![]() 填“漏气”、“不漏气”或“无法确定”
填“漏气”、“不漏气”或“无法确定”![]() 。实验时,装置A中c的作用_____________________,________________。
。实验时,装置A中c的作用_____________________,________________。
(6)为了提高测定的准确性,应选用装置A和_____![]() 填写字母标号
填写字母标号![]() 进行实验。
进行实验。
查看答案和解析>>
科目: 来源: 题型:
【题目】Cu及化合物在生产、国防中有重要的应用。
I.纳米级Cu2O既是航母舰艇底部的防腐蚀涂料,也是优良的催化剂。
(1)已知:Cu2O(s)+![]() O2(g)=2CuO(s) ΔH=-196kJ·mol-1
O2(g)=2CuO(s) ΔH=-196kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-220.8kJ·mol-1
则工业上用碳粉与CuO粉末混合在一定条件下反应制取Cu2O(s),同时生成CO气体的热化学方程式为___。
(2)用纳米级Cu2O作催化剂可实现甲醇脱氢制取甲醛:CH3OH(g)![]() HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。
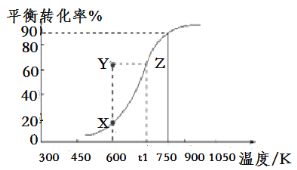
①该反应的ΔH___0(填“>”或“<”);600K时,Y点甲醇的v(正)___v(逆)(填“>”或“<”)。
②在t1K时,向固定体积为1L的密闭容器中充入2molCH3OH(g),温度保持不变,9分钟时达到平衡,则0~9min内用CH3OH(g)表示的反应速率v(CH3OH)___,温度为t1时,该反应的平衡常数K的表达式为___。
II.Cu既是常见的催化剂,又是常见的电极材料。
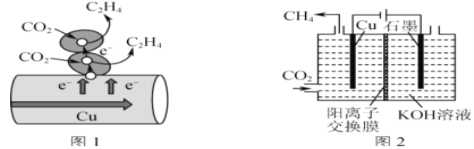
(3)图1表示的是利用CO2的“直接电子传递机理”。在催化剂铜的表面进行转化。当直接传递的电子物质的量为2mol时,则参加反应的CO2的物质的量为___。
(4)图2表示以KOH溶液作电解质溶液进行电解的示意图,CO2在Cu电极上可以转化为CH4,该电极反应的方程式为___。
III.含铜离子的废水会造成污染,通常将其转化为硫化铜沉淀而除去。
(5)已知:Ksp(CuS)=1×10-36,要使铜离子的浓度符合排放标准(不超过6.25×10-6mol/L),溶液中的硫离子的物质的量浓度至少为___mol/L(保留至小数点后一位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)根据氯化铁溶液回答下列问题:
①向FeCl3溶液中加入少量NaHCO3。产生的现象为___。用离子方程式表示其原因___。
②不断加热FeCl3溶液蒸干其水分并灼烧,得到的固体是___。
③在配制FeCl3溶液时,为防止溶液变浑浊,应加入___。
(2)利用反应Cu+H2O2+H2SO4=CuSO4+2H2O设计一个原电池,回答下列问题:
①负极材料为___;正极反应式为___。
②反应过程中SO![]() 向____极移动。
向____极移动。
③当电路中转移0.1mol电子时,电解液质量(不含电极)增加了___克。
(3)已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
①物质的量浓度均为0.1molL-1的四种溶液:pH由小到大排列的顺序是__(用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
②常温下,0.1molL-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是___(填字母)
A.c(H+) B.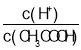 C.c(H+)c(OH-) D.
C.c(H+)c(OH-) D.![]() E.
E.![]()
③写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:____。
④25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=____(填准确数值)。
⑤标准状况下,将1.12LCO2通入100mL1molL-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+____。
查看答案和解析>>
科目: 来源: 题型:
【题目】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )
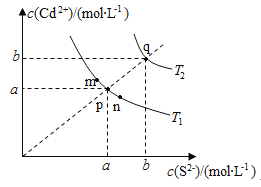
A.图中a和b分别为T1、T2温度下CdS在水中的溶解度
B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.无色溶液中:Al3+、NH4+、Cl-、S2-
B.使酚酞显红色的溶液中:Na+、ClO-、CO32-、NO3-
C.0.1mol·L-1FeCl3溶液中:Mg2+、NH4+、SCN-、SO42-
D.由水电离出的c(H+)=1×10-13mol·L-1的溶液中:Fe2+、Cu2+、SO42-、NO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,Ksp(ZnS)=l.6×10-24,Ksp(FeS)=6.4×10-18,其中FeS为黑色晶体,ZnS是一种白色颜料的组成成分。下列说法正确的是
A.向物质的量浓度相等的FeSO4和ZnSO4混合液中滴加Na2S溶液,先产生黑色沉淀
B.常温下,反应FeS(s)+Zn2+(aq)ZnS(s)+Fe2+(aq)的平衡常数K=4.0×l06
C.在ZnS的饱和溶液中,加入FeSO4溶液,一定不会产生FeS沉淀
D.向FeS悬浊液中通入少许HC1,c(Fe2+)与Ksp(FeS)均增大
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用 0.1 mol·L-1 KOH 溶液滴定 10 mL 0.1 mol·L-1 HA(Ka =1.0×10-5)溶液的滴定曲线如图所示。下列说法正确的是( )
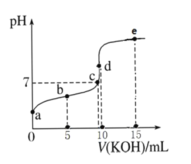
A.a 点溶液的 pH 约为 5
B.水的电离程度:c 点>d 点
C.b 点溶液中粒子浓度大小: c(A-)>c(K+)>c(HA)>c(H+)>c(OH-)
D.e 点溶液中:c(K+)=2c(A-)+2c(HA)
查看答案和解析>>
科目: 来源: 题型:
【题目】铁、钴、镍具有相似的性质,在化学上称为铁系元素。回答下列问题:
![]() 、
、![]() 常用作锂离子电池的正极材料。
常用作锂离子电池的正极材料。![]() 的空间构型为____________基态Co原子核外电子排布式为____________,第四电离能
的空间构型为____________基态Co原子核外电子排布式为____________,第四电离能![]() ______
______![]() 填“
填“![]() ”或
”或![]() ”
”![]() ,原因是________________。
,原因是________________。
![]() 铁系元素能与CO形成
铁系元素能与CO形成![]() 、
、![]() 等金属羰基配合物。
等金属羰基配合物。![]() 中与Fe形成配位键的是______
中与Fe形成配位键的是______![]() 填“碳”或“氧”
填“碳”或“氧”![]() 原子。与CO互为等电子体的是_________
原子。与CO互为等电子体的是_________![]() 任写一种即可
任写一种即可![]() 。在CO分子中,
。在CO分子中,![]() 键与
键与![]() 键数目之比为________。
键数目之比为________。
![]() 铁与
铁与![]() 、
、![]()
![]() 环戊二烯
环戊二烯![]() 在隔绝空气条件下共热可制得二茂铁
在隔绝空气条件下共热可制得二茂铁![]() 。在环戊二烯中,C原子的杂化轨道类型为______。二茂铁熔点为446K,不溶于水,易溶于乙醚、苯、乙醇等有机溶剂,373K即升华,则它的晶体类型是___________。
。在环戊二烯中,C原子的杂化轨道类型为______。二茂铁熔点为446K,不溶于水,易溶于乙醚、苯、乙醇等有机溶剂,373K即升华,则它的晶体类型是___________。
![]() 铁单质的堆积方式有两种,其中一种剖面图如图所示:
铁单质的堆积方式有两种,其中一种剖面图如图所示:
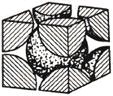
在此堆积方式里,铁原子的半径为![]() ,则其晶胞棱长为_______________cm。
,则其晶胞棱长为_______________cm。
查看答案和解析>>
科目: 来源: 题型:
【题目】CoC2O4是制备金属钴的原料。利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如图:
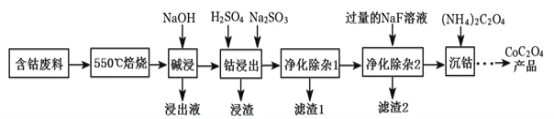
(1)“550℃煅烧”的目的是____。
(2)“浸出液”的主要成分是___。
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为___。
(4)“净化除杂1”过程中,如何检验该杂质__(用离子方程式表示),现象为__:需在40~50℃加入H2O2溶液,其原因是__,目的是__(用离子方程式表示);再升温至80~85℃,加入Na2CO3溶液,调pH至5,“滤渣I”的主要成分是__。
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×l0-5 mol/L,则滤液中c(Mg2+)为___mol/L。[已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com