
科目: 来源: 题型:
【题目】有机物的结构可用“键线式”表示,如:CH3CHCHCH3可简写为![]() 。有机物X的键线式为
。有机物X的键线式为![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A.X的化学式为C8H8
B.有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为![]()
C.X能使酸性高锰酸钾溶液褪色
D.X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有4种
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是Zn和Cu组成的原电池示意图,某小组做完该实验后,在读书卡片上记录如下,卡片上描述合理的是( )
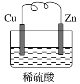
实验记录:
①导线中电流方向:Zn→Cu
②Cu极上有气泡产生,发生还原反应
③锌片变薄
实验结论:
④Zn为正极,Cu为负极
⑤正极反应式:Cu-2e-=Cu2+,发生氧化反应
⑥H+向Cu极移动,SO42-向Zn极移动
A.②③⑥B.④⑤⑥
C.③④⑤D.①②③
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:
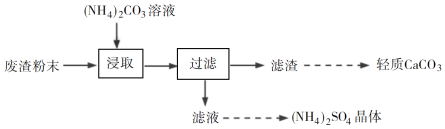
(1)室温下,反应CaSO4(s)+![]() (aq)
(aq)![]() CaCO3(s)+
CaCO3(s)+![]() (aq)达到平衡,则溶液中
(aq)达到平衡,则溶液中 =________[Ksp(CaSO4)=4.8×105,Ksp(CaCO3)=3×109]。
=________[Ksp(CaSO4)=4.8×105,Ksp(CaCO3)=3×109]。
(2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为________;浸取废渣时,向(NH4)2CO3溶液中加入适量浓氨水的目的是________。
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导致CaSO4的转化率下降,其原因是________;保持温度、反应时间、反应物和溶剂的量不变,实验中提高CaSO4转化率的操作有________。

(4)滤渣水洗后,经多步处理得到制备轻质CaCO3所需的CaCl2溶液。设计以水洗后的滤渣为原料,制取CaCl2溶液的实验方案:______[已知pH=5时Fe(OH)3和Al(OH)3沉淀完全;pH=8.5时Al(OH)3开始溶解。实验中必须使用的试剂:盐酸和Ca(OH)2]。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁、镍及其化合物在工业上有广泛的应用。从某矿渣 ![]() 成分为
成分为![]() 铁酸镍
铁酸镍![]() 、NiO、FeO、CaO、
、NiO、FeO、CaO、![]() 等
等![]() 中回收
中回收![]() 的工艺流程如下:
的工艺流程如下:
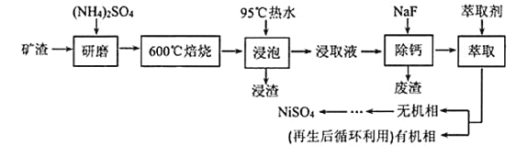
已知![]() 在
在![]() 分解生成
分解生成![]() 和
和![]() ,回答下列问题:
,回答下列问题:
![]() “浸渣”的成分有
“浸渣”的成分有![]() 、
、![]() 、
、![]() 外,还含有_________
外,还含有_________![]() 写化学式
写化学式![]() 。
。
![]() 矿渣中部分FeO焙烧时与
矿渣中部分FeO焙烧时与![]() 反应生成
反应生成![]() 的化学方程式为_____________。
的化学方程式为_____________。
![]() 溶剂萃取可用于对溶液中的金属离子进行富集与分离:
溶剂萃取可用于对溶液中的金属离子进行富集与分离:![]() 水相
水相![]() 有机相
有机相![]() 有机相
有机相![]() 水相
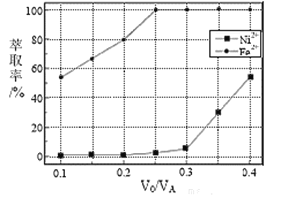
水相![]() 。萃取剂与溶液的体积比
。萃取剂与溶液的体积比![]() 对溶液中
对溶液中![]() 、
、![]() 的萃取率影响如下图所示,
的萃取率影响如下图所示,![]() 的最佳取值为________。在_______
的最佳取值为________。在_______![]() 填“强碱性”“强酸性”或“中性”
填“强碱性”“强酸性”或“中性”![]() 介质中“反萃取”能使有机相再生而循环利用。
介质中“反萃取”能使有机相再生而循环利用。
![]() 以Fe、Ni为电极制取
以Fe、Ni为电极制取![]() 的原理如下图所示。通电后,在铁电极附近生成紫红色的
的原理如下图所示。通电后,在铁电极附近生成紫红色的![]() ,若pH过高,铁电极区会产生红褐色物质。
,若pH过高,铁电极区会产生红褐色物质。
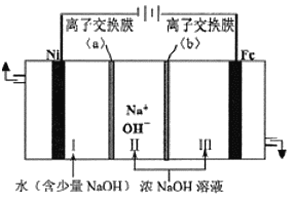
![]() 电解时阳极的电极反应式为_________,离子交换膜
电解时阳极的电极反应式为_________,离子交换膜![]() 为________
为________![]() 填“阴”或“阳
填“阴”或“阳![]() 离子交换膜。
离子交换膜。
![]() 向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为__________。
向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应2NO2![]() 2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时生成2nmolNO2
②单位时间内生成nmolO2的同时生成2nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
A.②③B.①④
C.①③④D.①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
(1)实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。

试回答:
①实验1、2研究的是__________________________对H2O2分解速率的影响。
②实验2、3的目的是_______________________________________________。
(2)实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

① 定性分析:如图甲可通过观察________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________________________。
②定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是__________________________________。
(3)实验三:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____________________的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_________。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 以
以![]() 和
和![]() 为原料合成尿素是利用
为原料合成尿素是利用![]() 的成功范例。在尿素合成塔中的主要反应可表示如下:
的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:![]()
![]()
反应Ⅱ:![]()
![]()
总反应:![]()
![]()
请回答下列问题:
![]() 反应Ⅰ的
反应Ⅰ的![]() ______________。
______________。
![]() 在____
在____![]() 填“高温”或“低温”
填“高温”或“低温”![]() 情况下有利于反应Ⅱ的自发进行。
情况下有利于反应Ⅱ的自发进行。
![]() 氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以
氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以![]() 、
、![]() 、
、![]() 、
、![]() 的形式存在。
的形式存在。

![]() “溶浸”中 ZnO发生反应的离子方程式为 _______。
“溶浸”中 ZnO发生反应的离子方程式为 _______。
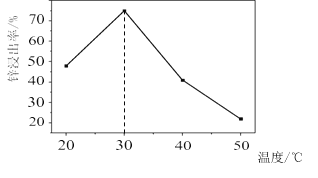
![]() 锌浸出率与温度的关系如图所示,分析
锌浸出率与温度的关系如图所示,分析 ![]() 时锌浸出率最高的原因为 __________。
时锌浸出率最高的原因为 __________。
![]() “滤渣 3”的主要成分为_______________。
“滤渣 3”的主要成分为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】北京冬奥会将于2022年举办,节俭办赛是主要理念。在场馆建设中用到一种耐腐、耐高温的表面涂料是以某双环烯酯为原料制得,该双环烯酯的结构如图所示(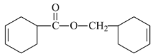 )。下列说法正确的是
)。下列说法正确的是
A.该双环烯酯的水解产物都能使溴水褪色
B.1 mol该双环烯酯能与3 mol H2发生加成反应
C.该双环烯酯分子中至少有12个原子共平面
D.该双环烯酯完全加氢后的产物的一氯代物有7种
查看答案和解析>>
科目: 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列有关说法不正确的是
A.尼龙属于有机高分子材料
B.稻草秸秆和甘蔗渣中富含纤维素,可以用它来制造纸张
C.将大桥钢制构件用导线与石墨相连可以起到防腐的作用
D.刘禹锡![]() 浪淘沙
浪淘沙![]() 诗句“千淘万漉虽辛苦,吹尽黄沙始到金”中“淘”“漉”相当于“过滤”
诗句“千淘万漉虽辛苦,吹尽黄沙始到金”中“淘”“漉”相当于“过滤”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com