
科目: 来源: 题型:
【题目】以下对化学反应描述的观点中正确的有几项:①放热反应在常温下均能自发进行;②电解过程中,化学能转化为电能而“储存”起来;③原电池工作时所发生的反应一定有氧化还原反应;④加热时,化学反应只向吸热反应方向进行;⑤盐类均能发生水解反应;⑥相同温度下,同一反应的化学平衡常数的大小与化学反应方程式的书写有关( )
A.1项B.2项C.3项D.4项
查看答案和解析>>
科目: 来源: 题型:
【题目】以淀粉为基本原料可制备许多物质,如:
![]()
下列有关说法正确的是( )。
A.淀粉与纤维素互为同分异构体
B.反应⑤是取代反应
C.反应①是氧化反应
D.在加热条件下,可用银氨溶液鉴别葡萄糖和乙醇
查看答案和解析>>
科目: 来源: 题型:
【题目】乳酸亚铁晶体![]() 是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与
是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与![]() 反应制得:
反应制得:![]() 。
。
I. 制备![]() :装置如下图所示:
:装置如下图所示:
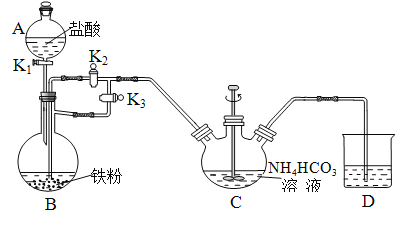
⑴B的名称是________________。
⑵①清洗仪器,检查装置的气密性。
②实验操作:在A中加入盐酸,B中加入铁粉、C中加入![]() 溶液。关闭活塞______(填
溶液。关闭活塞______(填![]() 或
或![]() ,下同)打开活塞______,滴入足量盐酸后,关闭活塞
,下同)打开活塞______,滴入足量盐酸后,关闭活塞![]() ,开动搅拌器,反应一段时间后关闭活塞______、打开活塞_______。
,开动搅拌器,反应一段时间后关闭活塞______、打开活塞_______。
C中发生的反应的离子方程式为_______________________________________。
Ⅱ.制备乳酸亚铁晶体:将制得的![]() 加入乳酸溶液中,加入少量铁粉,在
加入乳酸溶液中,加入少量铁粉,在![]() 下搅拌使之充分反应。然后再加入适量乳酸。
下搅拌使之充分反应。然后再加入适量乳酸。
⑶加入少量铁粉的作用是___________________________________。从所得溶液中获得乳酸亚铁晶体所需的实验操作是:隔绝空气低温蒸发,冷却结晶,______、______、干燥。
Ⅲ.乳酸亚铁晶体纯度的测量:
⑷若用![]() 滴定法测定样品中
滴定法测定样品中![]() 的量进而计算纯度时,发现结果总是大于
的量进而计算纯度时,发现结果总是大于![]() ,其原因可能是_________________________。
,其原因可能是_________________________。
⑸经查阅文献后,改用![]() 标准溶液滴定进行测定。反应中
标准溶液滴定进行测定。反应中![]() 离子的还原产物为
离子的还原产物为![]() 。测定时,先称取
。测定时,先称取![]() 样品溶解后进行必要处理,配制成250mL溶液,每次取
样品溶解后进行必要处理,配制成250mL溶液,每次取![]() ,用
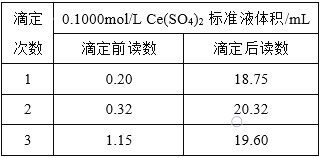
,用![]() 标准溶液滴定至终点,记录数据如右表。则产品中乳酸亚铁晶体的纯度为:____________
标准溶液滴定至终点,记录数据如右表。则产品中乳酸亚铁晶体的纯度为:____________![]() 以质量分数表示,乳酸亚铁式量为
以质量分数表示,乳酸亚铁式量为![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
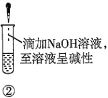
【题目】下列关于蔗糖属于非还原性糖,而其水解产物具有还原性的实验方案的说法正确的是( )。
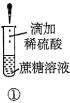
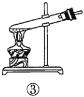
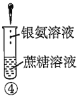
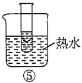
A.验证蔗糖属于非还原性糖的操作顺序:④③
B.验证蔗糖風于非还原性糖的操作顺序:④②③
C.验证蔗糖水解产物具有还原性的操作顺序:①④⑤
D.验证蔗糖水解产物具有还原性的操作顺序:①②④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】反应2NO2(g)![]() N2 O4(g);△H= -57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
N2 O4(g);△H= -57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A浅,C深
C.由状态A到状态B,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)水的电离平衡曲线如图所示,若A点表示25 ℃时水的电离达平衡时的离子浓度,B点表示100 ℃时水的电离达平衡时的离子浓度。则100 ℃时pH=12的NaOH溶液100mL,要使它的pH为11。(体积变化忽略不计)
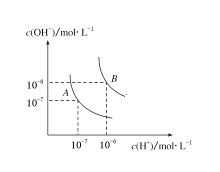
①如果加入蒸馏水,应加_________mL;
②如果加入pH=10的NaOH溶液,应加_________mL;
(2)25 ℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是________(填“促进”、 “抑制”或“不影响”)。
已知如表数据。
化学式 | 电离平衡常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
(3)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为_________。(填化学式)
(4)25 ℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,则c(Na+)________c(CH3COO-)(填“>”、“<”或“=”)。
(5)向NaCN溶液中通入少量CO2,反应的化学方程式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置。下列叙述正确的是( )

A.a和b用导线连接时,铁电极上发生还原反应
B.a和b用导线连接时,电子经硫酸铜溶液从铁电极流向铜电极
C.无论a和b是否连接,铜电极质量都增加
D.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室中用氯气与粗铜![]() 杂质只有Fe)反应,制备CuCl2·2H2O晶体的流程如下
杂质只有Fe)反应,制备CuCl2·2H2O晶体的流程如下

已知:氯化铜从水溶液中结晶时,所得晶体CuCl2·2H2O与温度关系如下
温度 | 小于15℃ | 15—25.7℃ | 26—42℃ | 42—100℃ | 100℃以上 |
晶体 | CuCl2·4H2O | CuCl2·3H2O | CuCl2·2H2O | CuCl2·H2O | CuCl2 |
下列说法不正确的是
A.制备氯气的反应:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
B.由溶液乙制备纯净CuCl2·2H2O晶体的系列操作步骤为:加少量盐酸、蒸发浓缩、冷却到室温结晶、过滤、洗涤、干燥。
C.固体乙是氢氧化铁
D.此流程中溶解固体甲的酸只能是盐酸
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)“民以食为天,食以安为先”。近年来屡屡发生的 劣质奶粉、苏丹红、多宝鱼等食品安全事件严重威胁消费者的健康和生命安全。下列有关蛋白质的说法正确的是____________(填序号)。
A.蛋内质是重要的营养物质,也是提供人体所需能最的主要物质
B.蛋白质在淀粉酶的作用下,可水解成葡萄糖等
C.蛋白质水解的最终产物是氨基酸
(2)奶粉中蛋内质含量的国家标准是:每100 g婴幼儿奶粉中含蛋白质1225 g。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨, 由氨的量计算出氮的量,再由氮的量求出蛋白质的含量(蛋白质含氮量按16%计算)。某市质检局取100 g市场中的某个品牌的奶粉样品进行检验。该样品进行反应后生成的![]() 和 7.5 g 19. 6%的稀硫酸恰好完全反应,通过计算可判断出这种奶粉__________(填“属于”或“不属于”)合格奶粉。
和 7.5 g 19. 6%的稀硫酸恰好完全反应,通过计算可判断出这种奶粉__________(填“属于”或“不属于”)合格奶粉。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com