
科目: 来源: 题型:
【题目】某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) ![]() 2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随时间的变化如图乙所示,下列说法中正确的是( )
2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随时间的变化如图乙所示,下列说法中正确的是( )

A.30~40 min间该反应使用了催化剂
B.化学方程式中的x=1,正反应为吸热反应
C.30 min时降低温度,40 min时升高温度
D.8 min前A的平均反应速率为0.08 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据要求填写下列空白:
(1)常温下均为0.02mol/L硫酸和氢氧化钠,等体积混合后溶液的pH=________
(2)常温下,pH都为11的Na2CO3和NaOH溶液中,由水电离出的c(OH-)之比为_____________
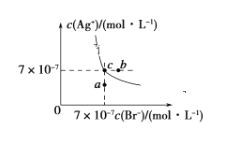
(3)在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。已知AgCl的Ksp=4×10-10,则 AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)的平衡常数K=_______________。
AgBr(s)+Cl-(aq)的平衡常数K=_______________。
(4)已知二元酸H2A在水中存在以下电离:H2A=H++HA-,HA-![]() H++A2-,回答下列问题:
H++A2-,回答下列问题:
①NaHA溶液呈________(填“酸”、“碱”、“中”或“无法确定”)性,理由是____________。
②某温度下,向10 mL、0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至中性,此时溶液中以下关系一定正确的是________(填写字母)。
a.溶液pH=7 b.水的离子积Kw=c2(OH-) c.V=10 d.c(K+)<c(Na+)
查看答案和解析>>
科目: 来源: 题型:
【题目】中学化学常见物质存在转化关系:A+B→C+D+H2O,其中C属于盐类,下列推断不正确的是
A.若A为黄绿色气体,则D可能有漂白性
B.若A为红色金属单质,则D一定是红棕色气体
C.若A为纯碱,则D一定能使澄清石灰水变浑浊
D.若A为氯化铵,则D一定是具有刺激性气味的气体
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据要求填写下列空白:
(1)NaHCO3溶液呈碱性的原因是 ______________(用方程式和必要文字表示),写出该溶液存在的物料守恒的关系式 ________________。
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要产物是________________________。
(3)若想除去CuCl2 溶液中混有FeCl3杂质,则往往加入试剂 ______________。
①NaOH ②NH3·H2O ③CuO ④CuCO3
(4)在酸碱滴定中,我们用0.1000mol/L HCl来滴定未知浓度的NaOH溶液,①在滴定过程中,操作或说法错误的是_______________。
a.滴定终点为:当滴完最后一滴恰好变色,且在半分钟内不恢复原色
b.进行中和滴定操作时,左手震荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化
c.酸式滴定管中的盐酸装液前未经润洗,导致所测定的c(NaOH)偏低。
d.酸式滴定管在滴定前有气泡,滴定后气泡消失,导致所测定的c(NaOH)偏高
②某学生根据三次实验分别记录有关数据如下:
滴定次数 | 待测氢氧化钠 溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=________________
查看答案和解析>>
科目: 来源: 题型:
【题目】A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是( )

A. X与A反应的化学方程式是:Al2O3 + 2Fe ![]() Fe2O3 + 2Al
Fe2O3 + 2Al
B. 检验D溶液中的金属阳离子的反应:Fe3++3SCN—= Fe(SCN)3↓
C. 单质Y在一定条件下能与水发生置换反应
D. 由于化合物B和C均既能与酸反应,又能与碱反应,所以均是两性化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)煤的利用可以是直接燃烧,也可以是先气化再燃烧 ,下面用等量的C分别按两途径进行反应
a. C(s)+O2(g) = CO2(g) △H =E1
b. C(s) +H2O(g)=CO(g)+H2 (g) △H =E2
H2(g)+![]() O2(g)=H2O(g ) △H =E3
O2(g)=H2O(g ) △H =E3
CO(s)+![]() O2(g)=CO2(g) △H =E4
O2(g)=CO2(g) △H =E4
甲同学认为:煤的气化效率高,所以b途径产生的热量高。乙同学认为,a、b途径产生的热量在理论上应该相同,你认为_____同学说法正确,理由是______________。
(2)在一元强碱MOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性。甲同学认为溶液中c(A-)=c(M+),而乙同学认为c(A-)是否等于 c(M+),要看一元酸HA是强酸还是弱酸。你认为_____同学说法正确,理由是______________
查看答案和解析>>
科目: 来源: 题型:
【题目】反应N2O4(g)![]() 2NO2(g) ΔH=57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g) ΔH=57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
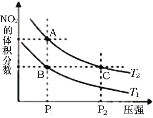
A.由状态B到状态A,可以用加热的方法
B.A、C两点气体的颜色:A深,C浅
C.A、C两点的反应速率:A>C
D.A、C两点气体的平均相对分子质量:A>C
查看答案和解析>>
科目: 来源: 题型:
【题目】已知海水中的溴含量约为 65 mg·L-1,从海水中提取溴的工业流程如下:
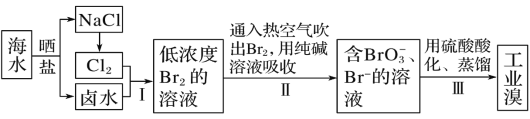
(1)写出步骤Ⅰ的离子方程式________________。
(2)步骤Ⅱ通入热空气吹出 Br2,利用了溴的_________________(填序号)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在横线上填入正确的化学计量数:______Br2+______CO32-=______BrO3-+______Br-+______CO2↑
(4)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为_______________。
(5)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有________________(填字母)。
A.乙醇 B.四氯化碳 C.醋酸 D.苯
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A. m=2
B. 两次平衡的平衡常数相同
C. X与Y的平衡转化率之比为1:1
D. 第二次平衡时,Z的浓度为0.4 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铁矿主要成分是二硫化亚铁。某化学实验小组取1.0g黄铁矿样品在空气中充分灼烧时发生反应4FeS2+11O2![]() 2Fe2O3+8SO2(假设杂质不参加反应),生成的SO2气体恰好被50mLFe2(SO4)3溶液完全吸收,在所得溶液中加入足量BaCl2溶液充分反应后,过滤、洗涤、干燥得13.98g固体。回答下列问题:
2Fe2O3+8SO2(假设杂质不参加反应),生成的SO2气体恰好被50mLFe2(SO4)3溶液完全吸收,在所得溶液中加入足量BaCl2溶液充分反应后,过滤、洗涤、干燥得13.98g固体。回答下列问题:
(1)FeS2在空气中灼烧时,化合价升高的元素是__________,SO2与Fe2(SO4)3反应的化学方程式是_________________。
(2)原Fe2(SO4)3溶液的物质的量浓度为_______,黄铁矿中FeS2的质量分数为______。
(3)工业上煅烧10 t上述黄铁矿,产生的SO2经催化氧化制硫酸,理论上可制得98%的浓硫酸多少吨______?(列式计算)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com