
科目: 来源: 题型:
【题目】(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g)![]() Fe3O4+4H2。该反应中H2O作__________(填“氧化剂”或“还原剂”);
Fe3O4+4H2。该反应中H2O作__________(填“氧化剂”或“还原剂”);
(2)检验某溶液中是否含有SO42-,先加盐酸,再加______(填“BaCl2”或“NaCl;
(3)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是__________(填“生石灰”或“盐酸”)。
(4)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式:2Na2O2 + 2______ = 2Na2 CO3 +O2 ↑;
(5)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有________(填“钠”或“钾”)元素;
查看答案和解析>>
科目: 来源: 题型:
【题目】氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应![]() 。已知该反应的反应速率随
。已知该反应的反应速率随![]() 的增大而增大。如图所示为用
的增大而增大。如图所示为用![]() 在单位时间内物质的量浓度变化表示的该反应的
在单位时间内物质的量浓度变化表示的该反应的![]() 图。下列说法不正确的是
图。下列说法不正确的是
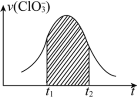
A.反应开始时速率增大可能是![]() 增大所致
增大所致
B.纵坐标为![]() 的
的![]() 曲线与图中曲线完全重合
曲线与图中曲线完全重合
C.图中阴影部分的面积表示![]() 时间内
时间内![]() 的物质的量的减少量
的物质的量的减少量
D.后期反应速率下降的主要原因是反应物浓度减小
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,是原电池的装置图。请回答:
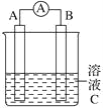
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反应式为____;
(2)若C为CuCl2溶液,Zn是负极,Cu极发生____反应,电极反应为____。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
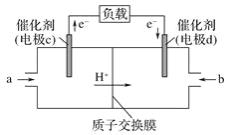
电池总反应为2CH3OH+3O2=2CO2+4H2O,c电极为____极,电极反应方程式为____。若线路中转移2mol电子,则消耗的O2在标准状况下的体积为____ L。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.![]() 能发生的反应类型:加成反应、取代反应、消去反应、水解反应
能发生的反应类型:加成反应、取代反应、消去反应、水解反应
B.已知![]() (X)
(X)![]()
![]() (Y),X与Y互为同分异构体,可用FeCl3溶液鉴别
(Y),X与Y互为同分异构体,可用FeCl3溶液鉴别
C.3—甲基—3—乙基戊烷的一氯代物有6种
D.相同条件下乙酸乙酯在水中的溶解度比其在乙醇中的溶解度大
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,将2molSO2和1molO2置于10L密闭容器中发生反应:2SO2(g)+O2(g) ![]() 2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A. 由图甲推断,B点SO2的平衡浓度为0.3 mol·L-1
B. 由图甲推断,A点对应温度下该反应的平衡常数为800(L·mol-1)
C. 达平衡后,若增大容器容积,则反应速率变化图像可以用图乙表示
D. 压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个绝热定容的密闭容器中,1molA与2molB发生反应A(g)+2B(g) ![]() xC(g)+2D(g) △H=bkJ·mol1(b<0),下列说法不正确的是
xC(g)+2D(g) △H=bkJ·mol1(b<0),下列说法不正确的是
A.平衡时,A和B的转化率相等
B.若 x=1,容器中压强不变时不能判断反应达到平衡
C.当B和D的物质的量之比1:1不变时,表明该反应已达到平衡
D.达到平衡过程中,正反应速率可能是先增大再减小
查看答案和解析>>
科目: 来源: 题型:
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)![]() xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol·L1·min1,下列说法正确的是
xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol·L1·min1,下列说法正确的是
A. 反应速率v(B)=0.25 mol·L-1·min-1
B. 该反应方程式中x=1
C. 2min时,A的物质的量为1.5mol
D. 2min时,A的转化率为60%
查看答案和解析>>
科目: 来源: 题型:
【题目】用惰性电极电解足量下列溶液一段时间后,再加入一定量括号内的纯净物,能使溶液恢复到原来的成分和浓度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨电极为惰性电极,溶液中阳离子在阴极放电,阴离子在阳极放电。A、电解AgNO3溶液,Ag+在阴极放电生成Ag,OH-在阳极放电生成O2,且n(Ag)∶n(O2)=2∶1,则应加入Ag2O恢复浓度,故A错误;B、电解NaOH溶液,H+在阴极放电生成H2,OH-在阳极放电生成O2,且n(H2)∶n(O2)=2∶1,则应加入一定量的H2O恢复原样,故B错误;C、电解KCl溶液,H+在阴极放电生成H2,Cl-在阳极放电生成Cl2,且n(H2)∶n(Cl2)=1∶1,则应加入一定量HCl恢复原样,故C错误;D、电解CuSO4溶液,Cu2+在阴极放电生成Cu,OH-在阳极放电生成O2,且n(Cu)∶n(O2)=2∶1,则应加入一定量CuO恢复原样,故D正确。故选D。
点睛:分析电解反应的原理,在两极析出什么物质(固体或气体),相当于什么物质脱离反应体系,根据元素守恒和原子比例,加入对应的物质,即可使溶液完全复原。
【题型】单选题
【结束】
28
【题目】工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是
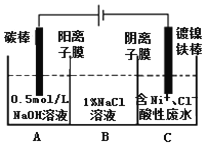
已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH--4e-=O2↑+2H2O
B. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C. 为了提高Ni的产率,电解过程中需要控制废水pH
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目: 来源: 题型:
【题目】按下图装置进行实验,并回答下列问题:

(1)判断装置的名称:A池为___________ ;B池为______________;
(2)锌极为________极,电极反应式为___________________________________;铜极为________极,电极反应式为___________________________________;石墨棒C1为______极,电极反应式为__________________________________;石墨棒C2附近发生的实验现象为______________________________________;
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化_________(变大、不变或变小)了________g,CuSO4溶液的质量_________(增加、不变或减少)_________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】在温度不变的条件下,在恒容的容器中进行下列反应:N2O4(g)![]() 2NO2(g),若N2O4的浓度由0.1mol·L-1降到0.07mol·L-1需要15s,那么N2O4的浓度由0.07mol·L-1降到0.05mol·L-1所需的反应时间( )
2NO2(g),若N2O4的浓度由0.1mol·L-1降到0.07mol·L-1需要15s,那么N2O4的浓度由0.07mol·L-1降到0.05mol·L-1所需的反应时间( )
A.等于5sB.等于10sC.小于10sD.大于10s
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com