
科目: 来源: 题型:
【题目】CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示,下列结论不正确的是( )
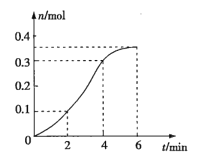
A.反应在![]() 内的平均反应速率最大
内的平均反应速率最大
B.反应速率先增大后减小
C.![]() 内温度对反应速率的影响较大
内温度对反应速率的影响较大
D.反应在![]() 内生成CO2的平均反应速率为
内生成CO2的平均反应速率为![]() 内的2倍
内的2倍
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,分别用0.1mol/L溶液进行下列实验,结论不正确的是![]()
![]()
A.向![]() 溶液中通
溶液中通![]() 至
至![]() :c(Na+)=c(HCO3-)+ 2c(CO32-)
:c(Na+)=c(HCO3-)+ 2c(CO32-)
B.向![]() 溶液中加入等浓度等体积的盐酸:c(Na+)=c(Cl-)
溶液中加入等浓度等体积的盐酸:c(Na+)=c(Cl-)
C.向![]() 溶液中加入等浓度等体积的
溶液中加入等浓度等体积的![]() 溶液:pH=13
溶液:pH=13
D.向氨水中加入少量![]() 固体:
固体:![]() 增大
增大
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中的硫的回收:SO2(g)+2CO(g)![]() 2CO2(g)+S(l) ΔH<0。一定温度下,在容积为2L的恒容密闭容器中,1molSO2和nmolCO发生反应,2min后达到平衡,生成2amolCO2。下列说法中正确的是( )
2CO2(g)+S(l) ΔH<0。一定温度下,在容积为2L的恒容密闭容器中,1molSO2和nmolCO发生反应,2min后达到平衡,生成2amolCO2。下列说法中正确的是( )
A.反应前2min的平均速率υ(SO2)=0.1amol/(L·min)
B.当混合气体的物质的量不再改变时,反应达到平衡状态
C.平衡后保持其他条件不变,从容器中分离出部分硫,平衡向正反应方向移动
D.平衡后保持其他条件不变,升高温度和加入催化剂,SO2的转化率均增大
查看答案和解析>>
科目: 来源: 题型:
【题目】足量Zn粉与![]() 的稀硫酸充分反应。为了减慢此反应的速率而不改变H2的产量,可以使用如下方法中的( )
的稀硫酸充分反应。为了减慢此反应的速率而不改变H2的产量,可以使用如下方法中的( )
①加Na2SO4溶液
②改用![]() 的稀盐酸
的稀盐酸
③改用![]() 的稀硝酸
的稀硝酸
④减压
⑤冰水浴
⑥加![]() 溶液
溶液
A.①⑤B.③⑤⑥C.①②⑤⑥D.全部
查看答案和解析>>
科目: 来源: 题型:
【题目】光刻技术需利用深紫外激光,我国是唯一掌握通过非线性光学晶体变频来获得深紫外激光技术的国家。目前唯一实用化的晶体是氟硼铍酸钾(KBeBF,含K、B、Be、O、F元素)。
回答下列问题:
(1)一群均处于激发态1s22s13s1的铍原子,若都回到基态,最多可发出___种波长不同的光。
A.1 B.2 C.3 D.4
(2)Be和B都容易与配体形成配位键,如[BeF4]-、[B(OH)4]-等,从原子结构分析其原因是__。
(3)氟硼酸钾是制备KBeBF的原料之一,高温下分解为KF和BF3。KF的沸点比BF3的高,原因是___。
(4)BF3易水解得到H3BO3(硼酸)和氢氟酸。氢氟酸浓溶液中因F-与HF结合形成HF![]() 使酸性大大增强。HF
使酸性大大增强。HF![]() 的结构式为___;H3BO3和BF
的结构式为___;H3BO3和BF![]() 中,B原子的杂化类型分别为___、__。
中,B原子的杂化类型分别为___、__。
(5)KBeBF晶体为层片状结构,图1为其中一层的局部示意图。平面六元环以B—O键和Be—O键交织相连,形成平面网状结构,每个Be都连接一个F,且F分别指向平面的上方或下方,K+分布在层间。KBeBF晶体的化学式为____。

(6)BeO晶体也是制备KBeBF的原料,图2为其晶胞结构示意图。
①沿着晶胞体对角线方向的投影,下列图中能正确描述投影结果的是___。

②BeO晶胞中,O的堆积方式为____;设O与Be的最近距离为acm,NA表示阿伏加德罗常数的值,则BeO晶体的密度为____g·cm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示![]() 某些条件和部分产物已略去
某些条件和部分产物已略去![]() 下列说法错误的是
下列说法错误的是![]()
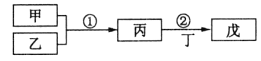
A.若戊为一种强碱且焰色反应为黄色,则反应![]() 可能都属于氧化还原反应
可能都属于氧化还原反应
B.常温下,若丙为无色气体,戊为红棕色气体,则甲、乙是铜和稀硝酸
C.若甲为硫磺燃烧产物,丁为水,则戊可用于干燥甲
D.若甲为浓盐酸,乙为![]() ,则戊可能使品红褪色
,则戊可能使品红褪色
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2SO3、NaHSO3、Na2S2O5可用于食品工业的漂白剂、防腐剂、抗氧化剂。已知:1molL﹣1Na2SO3溶液的pH≈9;1molL﹣1NaHSO3溶液的pH≈5。
(1)NaHSO3溶液的pH≈5的原因是_______(用化学用语并结合文字说明回答)。
(2)甲同学结合微粒观,应用所学知识,设计了如图所示实验,发现闭合开关后灵敏电流计指针发生偏转。

则:
①a电极为_______(填“正极”或“负极”);电极反应式为:______________。
②取少量Na2SO3溶液电极附近的混合液,加入_______,产生白色沉淀,证明产生了![]() 。
。
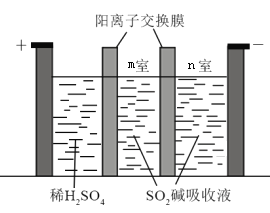
(3)制备Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3,则阳极的电极反应式为_____________。电解后,_____________室的NaHSO3浓度增加。
(4)乙同学测定市面上某干红葡萄酒中Na2S2O5残留量,取50.00 mL葡萄酒样品于锥形瓶中,用装有0.010 mol·L1碘标准液的_________(填“酸式”或“碱式”)滴定管滴定至终点,消耗标准液10.00 mL。该样品中Na2S2O5的残留量为____________g·L1(以SO2计)。(已知:![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】在2L恒容密闭容器中充入2molX和1molY发生反应:2X(g)+Y(g)![]() 3Z(g) ΔH<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列说法正确的( )
3Z(g) ΔH<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列说法正确的( )
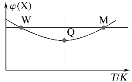
A.平衡时再充入Z,达到新平衡时Z的体积分数比原平衡时大
B.W点X的正反应速率等于M点X的正反应速率
C.Q点时,Y的转化率最小
D.升高温度,平衡常数减小
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关系式错误的是![]()
A.![]() 的水溶液:
的水溶液:![]()
B.等浓度的HCN溶液与NaOH溶液等体积混合,所得溶液![]() ,则溶液中离子浓度:
,则溶液中离子浓度:![]()
C.![]() 某一元酸HA溶液和
某一元酸HA溶液和![]() 溶液等体积混合的溶液中:
溶液等体积混合的溶液中:![]()
D.两种弱酸HX和HY混合后,溶液中的![]() 为
为![]() 为电离平衡常数
为电离平衡常数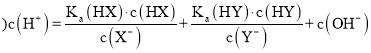
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.黄铁矿,主要成分是FeS,它只是生产硫酸的工业原料
B.利用铁的活泼性可以从铜盐中置换出铜单质,是青铜器时代湿法炼铜的原理
C.从海水中提取镁时需要先往海水中加入石灰乳
D.玻璃、玛瑙、石英、陶瓷、水泥都是传统的硅酸盐工业产品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com