
科目: 来源: 题型:
【题目】工业上使用Au 基体催化CO2 合成甲酸的反应过程如图所示。下列说法不正确的是
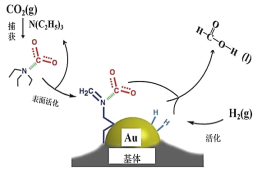
A.二氧化碳的电子式为![]()
B.在捕获过程,二氧化碳分子中的共价键完全断裂
C.N(C2H5)3 能够协助二氧化碳到达催化剂表面
D.CO2 催化加氢合成甲酸的总反应式为H2(g)+CO2(g)=HCOOH(l)
查看答案和解析>>
科目: 来源: 题型:
【题目】T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
 A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为3X(g)+Y(g) ![]() 2Z(g)
2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目: 来源: 题型:
【题目】下列与新冠肺炎防疫和检测有关的过程中,没有发生化学反应的是( )
A | B | C | D |
|
|
|
|
以丙烯为原料制备熔喷聚丙烯,作为医用外科口罩的材料 | 电解饱和食盐水制备消毒液,对公共场所进行消毒 | 使用明矾作为絮凝剂,对采集水样进行前处理 | 使用液氨作为制冷剂, 对疫苗进行低温保存 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】丙烯(C3H6)是重要的有机化工原料。丙烷脱氢制丙烯发生的主要反应及能量变化如图。
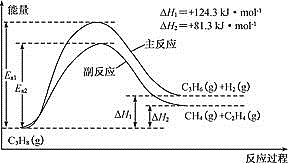
(1)丙烷脱氢制丙烯为强吸热过程。
①为提供反应所需热量,恒压时若向原料气中掺入水蒸气,则K(主反应)______(填“增大”、“减小”或“不变”)
②温度升高,副反应更容易发生的主要原因是:_____________________________。
(2)如图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分别为104Pa和105Pa)
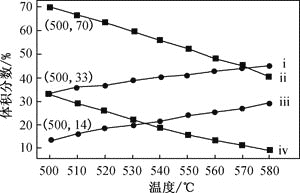
①104Pa时,图中表示丙烯的曲线是_________(填“i”、“ii”、“iii”或“iv”)
②104Pa、500℃时,主反应用平衡分压代替平黄浓度表示的化学平衡常数Kp=______(已知:气体分压=气体总压×体积分数)
(3)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图
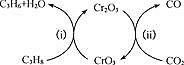
已知:CO和H2的燃烧热分别为H=-283.0kJ·mol-1、H=-285.8kJ·mol-1
①图中催化剂为___________。
②298K时,该工艺总反应的热化学方程式为____________。
③该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列现象或事实可用同一原理解释的是
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质
C.漂白粉、活性炭、![]() 都能使红墨水褪色
都能使红墨水褪色
D.![]() 和
和![]() 溶液使酸性高锰酸钾的紫色褪去
溶液使酸性高锰酸钾的紫色褪去
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:p[c(HX)/c(X-)]=-lg[c(HX)/c(X-)]。室温下,向0. 10 mol/LHX溶液中滴加0.10 mol/L NaOH溶液,溶液pH随p[c(HX)/c(X-)]变化关系如图。下列说法不正确的是
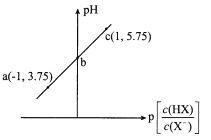
A. 溶液中水的电离程度:a<b<cB. 图中b点坐标为(0,4.75)
C. c点溶液中:c(Na+) =l0c(HX)D. 室温下HX的电离常数为10-4. 75
查看答案和解析>>
科目: 来源: 题型:
【题目】某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
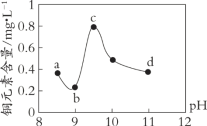
查阅资料,平衡I:Cu(OH)2 + 4NH3 ![]() [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;
平衡II:Cu(OH)2 + 2OH- ![]() [Cu(OH-)4]2-
[Cu(OH-)4]2-
项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+/ mg·L-1 | 72 | ≤0.5 |
NH4+/ mg·L-1 | 2632 | ≤15 |
下列说法不正确的是
A. 废水中Cu2+处理的最佳pH约为9
B. b~c段:随pH升高,Cu(OH)2的量增加,平衡I正向移动,铜元素含量上升
C. c~d段:随pH升高,c(OH-)增加,平衡I逆向移动,铜元素含量下降
D. d点以后,随c(OH-)增加,铜元素含量可能上升
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来AIST报告正在研制一种“高容量、低成本”锂-铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )

A. 放电时,Li+透过固体电解质向Cu极移动
B. 放电时,负极的电极反应式为Cu2O+H2O+2e-=2Cu+2OH-
C. 通空气时,铜被腐蚀,表面产生Cu2O
D. 整个反应过程中,铜相当于催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】某铜钴矿石主要含有 CoO(OH)、CoCO3、Cu2(OH)2CO3 和 SiO2,及一定量的 Fe2O3、MgO 和CaO等。由该矿石制Co2O3的部分工艺流程如图:
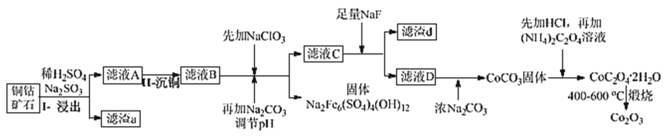
(1)在“浸出”过程中可以提高反应速率的方法有__。(写出两种即可)
(2)在“II-沉铜”过程中加入了FeS固体,得到更难溶的CuS,写出该步反应的离子方程式__。
(3)NaClO3 的主要作用是__。
(4)滤渣d 的主要成分是__。
(5)滤液D 中加入浓Na2CO3 后又加入HCl 溶解,其目的是__。
(6)写出CoC2O4·2H2O 在空气中煅烧得到 Co2O3 的化学方程式__。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定,下列实验中用高锰酸钾与浓盐酸反应制备得到氯气,然后再将氯气通入氢氧化钾溶液中与氢氧化铁固体充分反应而制得产品:
(1)制备K2FeO4(夹持装置略)
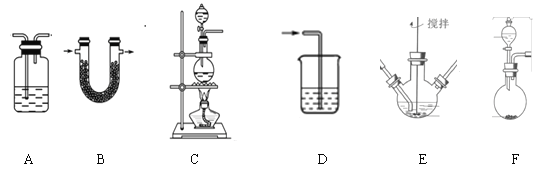
①请写出该过程中制备氯气的离子反应方程式________________(锰被还原为Mn2+)。
②请根据高铁酸钾制备的原理选择合适的装置,连接顺序为_________→ E →_________。(上述装置不一定全部用到,装置可以重复选用)
③装置E中反应时需进行搅拌,目的是_______________________
④E中得到紫色固体和溶液。E中生成高铁酸钾的反应为______________;反应充分进行后,E中溶液中主要的阴离子为__________________
(2)探究K2FeO4的性质
取E中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否是K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤E中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
②方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com