
科目: 来源: 题型:
【题目】下列图示与对应的叙述相符的是
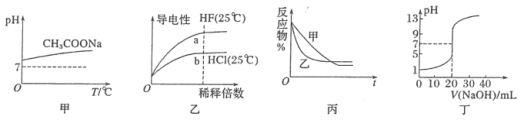
A.图甲表示升高温度醋酸钠的水解程度增大,溶液碱性增强
B.图乙表示氢氟酸为弱酸,且a点Kw的数值比b点Kw的数值大
C.图丙表示压强对可逆反应A(g)+B(g)![]() C(g)+D(s)的影响,乙的压强比甲的压强大
C(g)+D(s)的影响,乙的压强比甲的压强大
D.图丁表示0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1醋酸溶液的滴定曲线
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,将锌片和铜片按不同方式插入稀硫酸中,下列说法正确的是( )
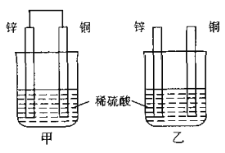
A. 甲中电子经导线从铜片流向锌片
B. 两烧杯中锌片上均发生还原反应
C. 两烧杯中铜片表面均无气泡产生
D. 一段时间后,两烧杯中溶液的c(H+)均减小
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于电解质溶液的说法正确的是
A.0.1 L 0.5 mol·L-1 CH3COOH溶液中含有的H+数为0.05NA
B.室温下,稀释0.1 mol·L-1 CH3COOH溶液,溶液的导电能力增强
C.向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中所有离子浓度均减小
D.CH3COOH溶液加水稀释后,溶液中![]() 的值减小
的值减小
查看答案和解析>>
科目: 来源: 题型:
【题目】常见有机物A~D有下图转化关系(部分反应条件和部分产物已略去)。已知A是一种酯,其分子式为C4H8O2,B是食醋的主要成分。
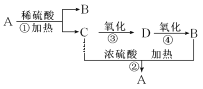
请回答下列问题:
(1)写出C和D含有的官能团名称___________、_____________;
(2)写出B和D的结构简式___________、_____________;
(3)写出B和C生成A的化学方程式___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲酸乙酯是重要的精细化工试剂,常用于配制水果型食用香精。实验室制备流程如下:
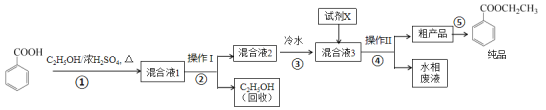
试剂相关性质如下表:
苯甲酸 | 乙醇 | 苯甲酸乙酯 | |
常温性状 | 白色针状晶体 | 无色液体 | 无色透明液体 |
沸点/℃ | 249.0 | 78.0 | 212.6 |
相对分子量 | 122 | 46 | 150 |
溶解性 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 | 与水任意比互溶 | 难溶于冷水,微溶于热水,易溶于乙醇和乙醚 |
回答下列问题:
(1)为提高原料苯甲酸的纯度,可采用的纯化方法为_________。
(2)步骤①的装置如图所示(加热和夹持装置已略去),将一小团棉花放入仪器B中靠近活塞孔处,将吸水剂(无水硫酸铜的乙醇饱和溶液)放入仪器B中,在仪器C中加入 12.2 g纯化后的苯甲酸晶体,30 mL无水乙醇(约0.5 mol)和3 mL浓硫酸,加入沸石,加热至微沸,回流反应1.5~2 h。仪器A的作用是_________;仪器C中反应液应采用_________方式加热。
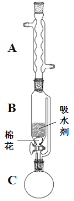
(3)随着反应进行,反应体系中水分不断被有效分离,仪器B中吸水剂的现象为_________。
(4)反应结束后,对C中混合液进行分离提纯,操作I是_________;操作II所用的玻璃仪器除了烧杯外还有_________。
(5)反应结束后,步骤③中将反应液倒入冷水的目的除了溶解乙醇外,还有_____;加入试剂X为_____(填写化学式)。
(6)最终得到产物纯品12.0 g,实验产率为_________ %(保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回 答下列问题:
(1)键线式![]() 的系统命名为____________;
的系统命名为____________;
(2)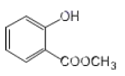 中含有官能团的名称为____________;
中含有官能团的名称为____________;
(3)2-甲基-1-丁烯的结构简式____________;
(4)相对分子质量为72且一氯代物只有一种的烷烃的结构简式____________;
(5) 的最简式为____________。
的最简式为____________。
(6)写出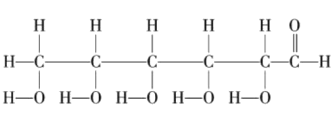 中所含官能团的电子式:____________、____________。
中所含官能团的电子式:____________、____________。
(7)分子式为C2H6O的有机物,有两种同分异构体,乙醇(CH3CH2OH)、甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是____________;
A.红外光谱 B.核磁共振氢谱 C.元素分析仪 D.与钠反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组用废旧镀锌铁皮按下列流程制备七水硫酸锌(ZnSO4·7H2O)

相关信息如下:
①金属离子形成氢氧化物沉淀的pH,如图A所示。
②ZnSO4的溶解度(物质在100g水中溶解的质量)随温度变化曲线如图B所示。

请回答:
(1)为提高镀锌铁皮中金属离子的浸出率,除了可适当增加硫酸的浓度,还可以采取的措施有:_______(任写一条)。
(2)步骤Ⅱ中需加入过量H2O2,请用离子方程式表示H2O2的作用________。
(3)步骤Ⅲ中调节pH范围为_______,调节pH宜选用的试剂为_______。
A.稀硫酸 B.氢氧化锌 C.氢氧化钠 D.氧化锌
(4)检验步骤Ⅲ所得滤液中是否含有Fe3+可采用的实验方法是_______。
(5)步骤Ⅳ需要用到下列所有操作:a.蒸发至溶液出现晶膜 b.在60℃蒸发溶剂 c.冷却至室温 d.在100℃蒸发溶剂 e.过滤
请给出上述操作的正确顺序______(操作可敢复使用)。
(6)步骤V中,某同学采用不同降温方式进行冷却结都,测得ZnSO4·7H2O颗粒大小分布如图所示。根据该实验结果,为了得到颗粒大小相对均的较大晶粒,宜选择______方式进行冷却结晶。
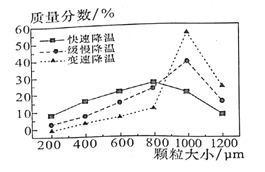
A.快速降温 B.级慢降温 C.变速降温
(7)ZnSO4可用于制备金属锌。用锌和高铁酸钾制成的高铁碱性电池,能储存比普通碱性电池多50%的电能,已知该电池的总反应是2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2。该电池正极反应式是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】那可汀是—种药物,该药适用于剌激性干咳病人服用,无成瘾性。化合物I是制备该药物的重要中间体,合成路线如下:
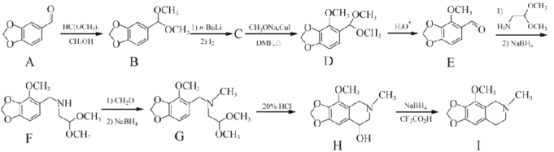
(1)化合物A中的官能团名称为____________(写两种)。
(2)I的分子式为____________。
(3)设计反应A-B的目的为____________。
(4)化合物C的分子式为C10H11O4I,写出C的结构简式:____________。
(5)化合物I的—种同分异构体同时满足下列条件,写出该同分异构体的结构简式:____________。
①分子中含有硝基(—NO2)且直接连在苯环上;②分子中只有3种不同化学环境的氢。
(6)写出以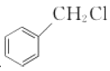 和
和 为原料制备
为原料制备![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。____________
查看答案和解析>>
科目: 来源: 题型:
【题目】空气吹出法工艺是目前“海水提溴”的最主要方法之一。其工艺流程如图所示,其中不正确的是

A.步骤④⑤是为了富集溴
B.步骤③说明溴具有挥发性
C.步骤④的离子方程式为Br2+SO2+H2O![]() 2H++2Br-+SO32-
2H++2Br-+SO32-
D.步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物可用分液漏斗分离
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)材料是人类赖以生存和发展的重要物质基础。
①下列物品的构成材料中主要是合成高分子材料的是____________(填字母).
a.宣纸 b.羊毛衫 c.保鲜膜
②橡胶是制造轮胎的主要原料,天然橡胶是____________结构(填“线型”或“体型”)'需经过硫化处理改变其结构,增强其机械强度。
(2)百合是江苏某地区的特产,富含有蛋白质、淀粉、脂肪,维生素B1、维生素B2、维生素C、泛酸、胡萝卜素科和丰富的钙、铁、磷等元素,其中:
①属于人体所需的微量元素的是____________。
②能提供能量的主要营养物质为蛋白质、淀粉和____________,淀粉在人体内完全水解的化学方程式____________。
③维生素C也称为____________,是一种无色的晶体,其水溶液显酸性,化学特性是易失电子,可以使食物中的Fe3+转化为Fe2+,这一过程体现了维生素C的____________(填“氧化性”或“还原性”)。水果、蔬菜中富含维生素C,组成维生素C的元素是____________(填写元素符号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com