
科目: 来源: 题型:
【题目】在体积不变的密闭容器中,保持一定的温度发生下列反应:4A(g)+B(?)2C(g)+2D(g),请用“增大”“减小”“不变”或“能”“不能”填空。
(1)当B为固体时,若反应向右进行,容器内混合气体的密度___________;若反应向左进行,容器内混合气体的密度___________;当容器内混合气体的密度不变时___________说明反应已经达到平衡。
(2)当B为气体时,不论向哪个方向反应,容器内混合气体的密度___________,故当容器内混合气体的密度不变时___________说明反应已经达到平衡。
(3)当B为固体时,无论向哪个方向反应,容器内混合气体的压强___________,故当容器内混合气体的压强不变时___________说明反应已经达到平衡。
查看答案和解析>>
科目: 来源: 题型:
【题目】以A、B为原料制备线型高分子化合物M和抗凝血药N的一种路线如下(部分反应条件和试剂略去):

已知:I. 烃A的密度是相同条件下H2密度的14倍;
I.![]()
II. ![]()
请回答下列问题:
(1)B的化学名称为____。F的结构简式为______。
(2)N中含氧官能团的名称为 _______。
(3)D→E的反应类型为_____。
(4)I的核磁共振氢谱中有_______组吸收峰。G分子中最多有____个原子共平面。
(5)B+C→M的化学方程式为_______。
(6)同时满足下列条件的J的同分异构体有_____种(不考虑立体异构)。
①苯环上连有2个取代基
②1mol该物质与足量的NaHCO3反应,生成2molCO2
(7)参照上述信息和合成路线,以HO![]() CH3和(CH3CO)2O为起始原料(其他无机试剂任选),设计制备
CH3和(CH3CO)2O为起始原料(其他无机试剂任选),设计制备![]() 的合成路线 _______。
的合成路线 _______。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色透明的溶液中: Fe3+、Mg2+、SCN 、Cl –
B.![]() =1×10-12的溶液中:K+、Na+、CO
=1×10-12的溶液中:K+、Na+、CO![]() 、NO
、NO![]()
C.![]() 的溶液中: K+、NH
的溶液中: K+、NH![]() 、MnO
、MnO![]() 、SO
、SO![]()
D.能使甲基橙变红的溶液中: Na+、NH![]() 、SO
、SO![]() 、HCO
、HCO![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 定温度下,下列溶液的离子浓度关系式正确的是
定温度下,下列溶液的离子浓度关系式正确的是![]()
A.![]() 的
的![]() 溶液中,
溶液中,![]()
B.稀释氨水溶液10倍后,其![]() 为原來的
为原來的![]()
C.pH之和为14的![]() 与NaOH溶液混合:
与NaOH溶液混合:![]()
D.将等物质的量的![]() 和
和![]() 混合溶于水中:
混合溶于水中:
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氯(ClO2)是一种黄绿色易溶于水的气体,常用作饮用水消毒。实验室通过如下过程制备二氧化氯。下列说法正确的是

A. 电解时发生反应的离子方程式为NH4++3Cl-![]() 2H2↑+NCl3
2H2↑+NCl3
B. 溶液X中大量存在的阴离子有Cl-、OH-
C. 可用饱和食盐水除去ClO2中的NH3
D. 常用作净水剂的明矾可除去饮用水中残留的NaClO2
查看答案和解析>>
科目: 来源: 题型:
【题目】某三元羧酸H3A在表面活性剂、洗涤剂、润滑剂等方面具有重要的地位。常温时,向10mL0.01mol·L-1的H3A溶液中滴入0.01mol·L-1的NaOH溶液,H3A、H2A-、HA2-、A3-的物质的量分数与溶液的pH的关系如图所示。则下列说法中错误的是( )

A.常温时,0.01mol·L-1的H3A溶液的pH介于2~3之间
B.常温时,反应A3-+H2O ![]() HA2-+OH-的平衡常数为K=10c-14
HA2-+OH-的平衡常数为K=10c-14
C.若b=7,则将等物质的量的NaH2A与Na2HA加入到适量蒸馏水中使其完全溶解,则所得的溶液的pH一定等于7
D.加入NaOH溶液的体积为30mL时,所得溶液中存在有:c(OH-)=3c(H3A)+2c(H2A-)+c(HA2-)+c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】根据如图所示示意图,下列说法不正确的是
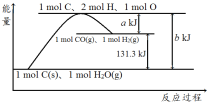
A. 反应的热化学方程式可表示为C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=(b-a) kJ·mol-1
CO(g)+H2(g) ΔH=(b-a) kJ·mol-1
B. 该反应过程反应物断键吸收的能量一定大于生成物成键放出的能量
C. 使用催化剂无法改变该反应的ΔH
D. nmol C和n mol H2O反应生成nmol CO和nmol H2吸收的热量一定为131.3nkJ
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 时,向
时,向![]() 的NaOH溶液中逐滴加入某浓度的
的NaOH溶液中逐滴加入某浓度的![]() 溶液,滴定过程中,溶液的pH与滴入
溶液,滴定过程中,溶液的pH与滴入![]() 溶液的体积的关系如图所示,②点时NaOH溶液恰好被中和,则下列说法中,正确的是
溶液的体积的关系如图所示,②点时NaOH溶液恰好被中和,则下列说法中,正确的是![]()

A.该滴定过程应该选择甲基橙作为指示剂
B.点④所示溶液中存在:![]()
C.图中点①到点③所示溶液中,水的电离程度先减小后增大
D.点①所示溶液中存在:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】酯类物质M是一种药物的主要合成中间体,其合成路线如下:

已知以下信息:
①芳香烃A的相对分子质量在100~110之间,1molA完全燃烧可消耗10molO2。
②H的核磁共振氢谱显示其有3种氢。
③RCH=CH2![]() RCHClCH3
RCHClCH3
④RX+Mg![]() RMgX(X代表卤素)
RMgX(X代表卤素)
⑤
![]()


回答下列问题:
(1)A的结构简式为______,H中官能团的名称为______。
(2)由E和H生成M的化学方程式为______。
(3)属于氧化反应的是______(填序号)。
(4)同时符合下列条件的E的同分异构体有______种(不考虑立体异构),其中苯环上一氯代物只有两种的结构简式为______。(任写一种)
①能与碳酸钠溶液发生反应;②苯环上的取代基数目有2个
(5)请结合所给信息,由苯合成苯乙烯,合成路线如图所示,请回答下列问题。

试剂②为______,最后一步反应的化学方程式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁稀土合金广泛应用于航空、航天、电子、通讯和汽车制造业等领域。熔盐电解法是一种高效制备镁稀土合金的方法,实验室制取Mg-Gd合金(物质的量比为1:1)的电解槽示意图如下(相对原子质量Mg—24,Gd—157),下列说法正确的是

A.添加LiF、BaF2的作用是催化剂
B.阳极的电极反应式为2F——2e—= F2 ↑
C.当电路中通过0.1mol电子时,生成Mg- Gd合金的质量为3.62 g
D.电解结束后,铝、碳电极质量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com