
科目: 来源: 题型:
【题目】向某氨水中加入醋酸溶液,反应方程式如下:NH3·H2O+CH3COOH=CH3COONH4+H2O滴加过程,溶液的导电能力(I)与加入醋酸溶液的体积(V)关系正确的是( )
A.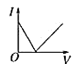 B.
B.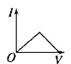 C.
C.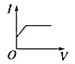 D.
D.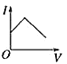
查看答案和解析>>
科目: 来源: 题型:
【题目】反应2X(g)+Y(g)![]() 2Z(g)(正反应放热),在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量(n)与反应时间(t)的关系如图所示。
2Z(g)(正反应放热),在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量(n)与反应时间(t)的关系如图所示。
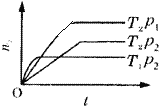
下述判断正确的是( )
A.T1>T2,p1>p2B.T1<T2,p1>p2
C.T1<T2,p1<p2D.T1>T2,p1<p2
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氮存在下列平衡2NO2 (g) ![]() N2O4(g);△H<0。在测定NO2 相对分子质量时,下列条件中较为适宜的是
N2O4(g);△H<0。在测定NO2 相对分子质量时,下列条件中较为适宜的是
A.温度130℃,压强3.03×105paB.温度25℃, 压强1.01×105pa
C.温度130℃,压强5.05×104paD.温度0℃, 压强5.05×104pa
查看答案和解析>>
科目: 来源: 题型:
【题目】将13.6gFe、Fe2O3和CuO的混合粉末加入到100mL一定物质的量浓度的盐酸中,充分反应,生成标准状况下的氢气896mL,过滤,滤渣经洗涤、干燥后得到1.28g固体纯净物,经检验滤液中只含有一种溶质。请回答:
(1)固体混合物中CuO的质量___。
(2)盐酸的浓度为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是人体必需元素,是合成血红素的重要原料,缺铁会造成贫血,市场上常见补血剂有硫酸亚铁、富马酸亚铁(分子式C4H2O4Fe)、葡萄糖酸亚铁、琥珀酸亚铁(速力菲片)等。某化学兴趣小组通过实验对硫酸亚铁补血剂成分进行探究并测定Fe2+的含量,可供选择的试剂有双氧水、KSCN溶液、盐酸、BaCl2溶液(已知KSCN可被双氧水氧化)。
(1)成分探究:小组成员发现硫酸亚铁补血剂外面糖衣是红色的,里面是淡蓝绿色的,甲同学对其组成进行如下探究:
实验探究 | 实验操作及现象 | 结论分析 |
探究一 | 将淡蓝绿色粉末溶解于盐酸溶液中,取上清液2份, ①1份滴加BaCl2溶液,产生白色沉淀,再加盐酸,无明显变化。 ②另1份溶液先滴加KSCN溶液,无明显变化,再滴加双氧水,后滴加___溶液,变成血红色。 | 证明淡蓝绿色粉末为FeSO4 |
探究二 | 将红色物质研成粉末,滴加盐酸,无明显变化,再滴加KSCN溶液,无明显现象。 | 证明:红色物质不是Fe2O3 |
(2)配制硫酸亚铁补血剂的待测溶液。
①补血剂(1片0.5克)![]() 浊液
浊液![]() 滤液
滤液![]() 配成1L待测液
配成1L待测液
步骤③浊液脱色后进行___(填标号)操作才能得到溶液。
A. B.
B.
C. D.
D.
②甲同学认为步骤③滤液直接蒸发结晶不能得到硫酸亚铁晶体,理由是___,你的方案是___。
③已知步骤④中加入足量的H2O2溶液,作用是___,然后微热并用玻璃棒搅拌至无气泡产生,目的是___。
④写出步骤④中发生反应的离子方程式:___。
(3)测定硫酸亚铁补血剂待测液的浓度
方法一:用紫外分光光度法:使用紫外分光光度计,将不同波长的光连续地照射到一定标准浓度滴加5mL0.2molL-1苯二甲酸氢钾缓冲液的硫酸亚铁标准溶液,得到与不同波长相对应的吸收强度,以硫酸亚铁标准溶液的浓度为横坐标,吸光度为纵坐标,绘出该物质的吸收光谱曲线如图。
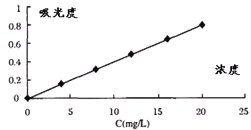
⑤取待测液10mL滴加5mL0.2molL-1苯二甲酸氢钾缓冲液,并稀释至60mL,用紫外分光光度法测得待测液的吸光度为0.4,则样品中铁元素的质量分数是___。
方法二:KMnO4标准溶液滴定法:称取4.0g的硫酸亚铁产品,溶于水,加入适量稀硫酸,用0.2molL-1KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液体积10.00mL。
⑥KMnO4溶液置于___式滴定管中,终点的颜色变化:___。
⑦要达到好的治疗效果,服用补血剂时需注意口服铁剂应同时并服维生素C,理由是 ___。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,对可逆反应A(g)+2B(g)![]() 3C(g)的下列叙述中,能说明反应已达到平衡的是( )
3C(g)的下列叙述中,能说明反应已达到平衡的是( )
A.A物质与C物质的反应速率之比为1∶2
B.单位时间内消耗a mol A,同时消耗3a mol C
C.容器内的压强不再变化
D.混合气体的物质的量不再变化
查看答案和解析>>
科目: 来源: 题型:
【题目】铝硅合金材料性能优良。铝土矿(含 30% SiO2、40.8% Al2O3和少量Fe2O3等)干法制取该合金的工艺如下:
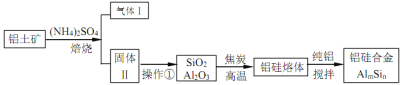
(1)铝硅合金材料中若含铁,会影响其抗腐蚀性。原因是______________。
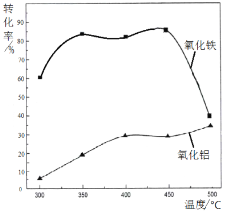
(2)焙烧除铁反应时 Fe2O3 转化为NH4Fe(SO4)2,Al2O3少部分发生类似反应。写出 Fe2O3发生反应的方程式:______________。 氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为______________。
(3)若操作①中所得溶液中加入过量NaOH 溶液,含铝微粒发生反应的离子方程式为:______________。
(4)用焦炭还原SiO2、Al2O3会产生SiC等中间体。写出中间体 SiC 再与Al2O3反应生成铝、硅单质的化学方程式并表出电子转移的方向和数目:______________ 。
(5)已知25℃时Ksp[Al(OH)3]=1.0×10-33,Ksp[Fe(OH)3]=4.0×10-38。向 FeCl3和 AlCl3的混合溶液中逐滴加入NaOH 溶液,生成 Al(OH)3和Fe(OH)3沉淀,当两种沉淀共存时,上层溶液中 c(Al3+):c(Fe3+)=__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X(g)+3Y(g)2Z(g) ΔH=-a kJ·molˉ1,一定条件下,将1 mol X和3 mol Y通入2 L的恒容密闭容器中,反应10 min,测得Y的物质的量为2.4 mol。下列说法正确的是
A. 10 min内,Y的平均反应速率为0.03 mol·Lˉ1·sˉ1
B. 第10 min时,X的反应速率为0.01 mol·Lˉ1·minˉ1
C. 10 min内,消耗0.2 mol X,生成0.4 mol Z
D. 第10 min时,Z的物质的量浓度为0.4mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】已知4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系式为
4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系式为
A.4v(NH3)=5v(O2)B.5v(O2)=6v(H2O)
C.2v(NH3)=3v(H2O)D.4v(O2)=5v(NO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com