
科目: 来源: 题型:
【题目】如图所示,甲池的总反应式为:CH4+2O2+2KOU=K2CO3+3H2O,下列说法正确的是( )
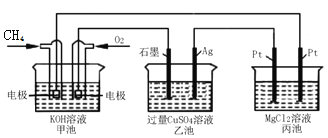
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B. 甲池中正极的电极反应式是O2+4e-+4H+=2H2O
C. 反应过程中,乙池的pH逐渐减小
D. 甲池中消耗O2的体积与丙池生成气体的总体积在相同条件下的比值为1∶2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A为一种盐,C、D、F、N、O在常温常压下均为无色气体,E在常温常压下为无色、无味的液体,N、H、L为高中常见的单质,I为常见的无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
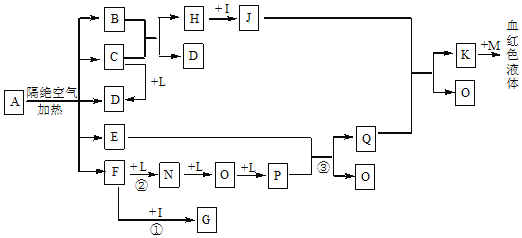
(1)写出D的电子式:___;
(2)写出反应②的化学方程式:___;
(3)已知B中氧元素的质量分数为22.2%,且A分解产生的各物质的物质的量之比为n(B):n(C):n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】(NH4)2Cr2O7可用作有机合成催化剂、媒染剂、显影液等。某化学兴趣小组对(NH4)2Cr2O7的部分性质及组成进行探究。已知:Cr2O72-(橙色)+H2O=2Cr2O42-(黄色)+2H+。请回答下列问题:
(1)在试管中加入少量(NH4)2Cr2O7固体,滴加足量浓KOH溶液,振荡、微热,观察到的主要现象是___。
(2)为探究(NH4)2Cr2O7(摩尔质量为252g/mol)的分解产物,按如图连接好装置,在A中加入5.040g样品进行实验。

①仪器B的名称是___。
②C的作用是___。
③反应结束后,依然要通一段时间的氮气的原因是___。
④加热A至恒重,观察到D中溶液不变色,同时测得A、B中质量的变化分别为200g、1.44g,写出重铬酸铵加热分解反应的化学方程式:___。
(3)实验室常用甲醛法测定含(NH4)2Cr2O7的样品中氮的质量分数,其反应原理为 2Ba2++Cr2O72-+H2O=2BaCrO4↓+2H+、4NH4++6HCHO=3H++6H2O+(CH2)6N4H滴定时,1mo1(CH2)N4H+与1mo1H+相当],然后用NaOH标准溶液滴定反应生成的酸。
实验步骤:称取样品2.800g,配成250mL溶液,移取25.00mL样品溶液于250mL锥形瓶中,用氯化钡溶液使Cr2O72-完全沉淀后,加入10mL2.000 mo1L-1的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用0.200mo1L-1NaOH 标准溶液滴定至终点。重复上述操作3次,最终滴定用去NaOH标准溶液体积的平均值为20.00mL。
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则滴定时用去的NaOH标准溶液的体积___(填“偏大”“偏小”或“无影响”)。
②滴定计算得该样品中氮的质量分数为___。
查看答案和解析>>
科目: 来源: 题型:
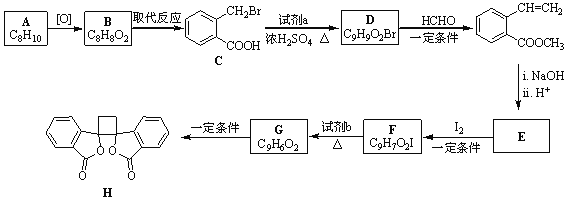
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如图所示:
已知:i.RCH2Br![]() R-HC=CH-R’;
R-HC=CH-R’;
ii.R-HC=CH-R’![]() ;
;
iii.R-HC=CH-R’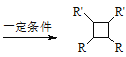 (以上R、R’、R”代表氢原子、烷基或芳基等)
(以上R、R’、R”代表氢原子、烷基或芳基等)
(1)A属于芳香烃,A的名称是___。
(2)由C生成D的化学方程式是___。
(3)由E与I2在一定条件下反应生成F的化学方程式是___;此反应同时生成另外一种与F互为同分异构体的有机副产物(不考虑立体异构),此有机副产物的结构简式是___。
(4)下列说法正确的是___(填字母代号)。
a.G存在顺反异构体
b.由G生成H的反应是加成反应
c.1mo1G最多可以与1mo1H2发生加成反应
d.1mo1F或1mo1H与足量NaOH溶液反应,均消耗2mo1NaOH
(5)试剂b是___。
(6)E有多种同分异构体,其中属于芳香族化合物,并既能发生加聚反应又能发生水解反应的有___种(不考虑立体异构)。写出其中任意一种核磁共振氢谱为5组峰,且峰面积之比为1:1:2:2:2的物质的结构简式:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究CO、CO2的回收利用既可变废为宝,又可减少碳的排放。请回答下列问题:
(1)二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料”,由CO和H2制备二甲醚的反应原理如下:
CO(g)+2H2(g)CH3OH(g) △H=-90.1kJ/mol
2CH3OH(g)CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
已知:CO(g)+H2O(g)CO2(g)+H2(g) △H=-41.0kJ/mol
则2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g)的△H=________
(2)T1K时,将1mol二甲醚引入一个抽真空的150L恒容密闭容器中,发生分解反应CH3OCH3(g)CH4(g)+H2(g)+CO(g)。
在不同时间测定容器内的总压,所得数据见下表,
反应时间t/min | 0 | 6.5 | 13.0 | 26.5 | 52.6 | ∞ |
气体总压p总/kPa | 50.0 | 55.0 | 65.0 | 83.2 | 103.8 | 125.0 |
①由表中数据计算,0~6.5min内的平均反应速率)(CH3OCH3)=___
molL-1min-1(结果保留两位有效数字)反应达平衡时,二甲醚的分解率为___,该温度下平衡常数K=___。
②反应达到平衡后,若升高温度,CH3OCH3的浓度增大,则该反应为___反应(填“放热”或“吸热”)。
在T2K、1.0×104kPa下,等物质的量的CO与CH4混合气体发生如下反应:CO(g)+CH4(g)=CH3CHO(g)
反应速率v=v正-v逆=k正p(CO)p(CH4)-k逆p(CH3HO),k正、k逆分别为k正、k逆向反应速率常数,p为气体的分压(气体分压p=气体总压p总×体积分数)。用气体分压表示的平衡常数KP=4.5×10-5kPa-1,则CO的转化率为20%时,![]() =___。
=___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用化学平衡移动原理解释的是( )
A.用排饱和食盐水法收集氯气
B.加压条件有利于N2和H2反应生成NH3
C.将盛有NO2的球浸泡在热水中颜色加深
D.加催化剂,使N2和H2在一定的条件下转化为NH3
查看答案和解析>>
科目: 来源: 题型:
【题目】已知HX和HY是两种一元弱酸,常温下用NaOH溶液分别滴定这两种弱酸溶液,若pKa=-lgKa,y=![]() 或lg
或lg![]() ,得到y和溶液pH的变化关系如图所示。下列有关叙述错误的是( )
,得到y和溶液pH的变化关系如图所示。下列有关叙述错误的是( )
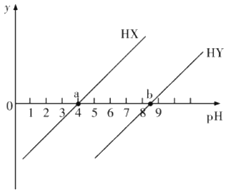
A.常温下,Ka(HX)=10-4,Ka(HY)=10-8.5
B.a点溶液中,c(X-)=c(HX)>c(Na+)>c(H+)>c(OH-)
C.常温下,0.1mol/LNaX溶液pH大于0.1mol/LNaY溶液的pH
D.往HY溶液中滴入NaOH溶液后所得的混合溶液中,![]() =10pH-pKa(HY)
=10pH-pKa(HY)
查看答案和解析>>
科目: 来源: 题型:
【题目】温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应: 2NO2(g)![]() 2NO(g)+O2(g) (正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗= 2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。
2NO(g)+O2(g) (正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗= 2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。
下列说法正确的是
容器 编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 设k为该反应的化学平衡常数,则有k=k逆:k正
B. 达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比为20∶17
C. 容器Ⅱ中起始平衡正向移动,达平衡时,容器Ⅱ中NO2的转化率比容器Ⅰ中的小
D. 若改变温度为T2,且T2>T1,则k正:k逆<0.8
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上由黄铜矿(主要成分为CuFeS2)冶炼铜的主要流程如图所示:
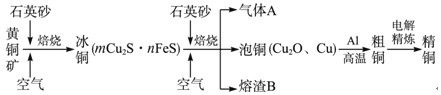
下列说法正确的是( )
A.由黄铜矿到冰铜的反应中,氧化剂是空气,还原剂是CuFeS2
B.气体A中的大气污染物可以用NaOH溶液或氨水吸收
C.将熔渣B用稀硫酸浸泡,取少量所得溶液,滴加KSCN溶液后呈红色,说明熔渣B 中的铁元素显+3价
D.由泡铜到粗铜的反应为吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:298K时,四种物质的溶度积如表所示。下列说法正确的是( )
化学式 | CH3COOAg | AgCl | Ag2CrO4 | Ag2S |
Ksp | 2.3×10-3 | 1.56×10-10 | 1.12×10-12 | 6.3×10-50 |
A.298K时,将0.001molL-1的AgNO3溶液逐滴滴入0.001molL-1的KCl和0.001molL-1的K2CrO4的混合液中,则先产生Ag2CrO4沉淀
B.298K时,向2.0×10-4molL-1的K2CrO4溶液中加入等体积的2.0×10-4molL-1的AgNO3溶液,则有Ag2CrO4沉淀生成(忽略混合时溶液体积的变化)
C.298K时,向CH3COOAg悬浊液中加入盐酸,发生反应的离子方程式为CH3COOAg+H++Cl-CH3COOH+AgCl
D.已知:![]() =0.65,298K时,四种物质的饱和溶液的物质的量浓度:c(CH3COOAg)>c(AgCl)>c(Ag2CrO4)>c(Ag2S)
=0.65,298K时,四种物质的饱和溶液的物质的量浓度:c(CH3COOAg)>c(AgCl)>c(Ag2CrO4)>c(Ag2S)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com