
科目: 来源: 题型:
【题目】下列图象正确的是( )
A. 向 Ca(OH)2和 NaOH的混合溶液中通 入CO2
B. 向 FeCl3 溶液中加入锌粉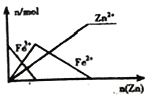
C. 向 NaOH 溶液中通入CO2
D. HCl与Cl2的混合气体通入NaOH溶液中
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量的CuS和![]() 的混合物投入足量的
的混合物投入足量的![]() 中,收集到气体
中,收集到气体![]() 标准状况
标准状况![]() ,向反应后的溶液中
,向反应后的溶液中![]() 存在
存在![]() 和
和![]() 加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到
加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到![]() ,若上述气体为NO和
,若上述气体为NO和![]() 的混合物,且体积比为
的混合物,且体积比为![]() ,则V可能为
,则V可能为![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,将气体 X 和气体 Y 各 0.16 mol 充入 10 L 恒容密闭容器中,发生反应:X(g)+Y(g) ![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A.该温度下,此反应的平衡常数 K=1.44
B.4min 时,ν(逆)>ν(正)
C.反应前 2min 的平均速率 ν(Z)=2.0×10-3mol/(L·min)
D.7min 时,反应还未达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】38.4 mg铜跟适量的浓硝酸反应,铜全部作用后,共收集到22.4 mL(标准状况下)气体,反应消耗的HNO3的物质的量可能是 ( )
A.1.0×10-3 molB.1.6×10-3 molC.2.2×10-3 molD.2.4×10-3 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出。在反应结束后的溶液中,逐滴加入4 mol/LNaOH 溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。下列说法不正确的是

A. O处溶液中的阳离子为:H+、Fe2+、Fe3+、Al3+
B. DE段反应的离子方程式为:NH4++OH-=NH3·H2O
C. 合金中,n(Al)=0.008mol
D. 欲测定F点沉淀的质量,实验步骤是:过滤、洗涤、干燥、称量
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.增大反应物浓度,可以增大单位体积的活化分子的百分数,使有效碰撞次数增大,反应速率加快
B.H2O2(l)=== ![]() O2(g)+H2O(l) △H=-98 kJ·mol-1,该反应在任何温度下均能自发进行
O2(g)+H2O(l) △H=-98 kJ·mol-1,该反应在任何温度下均能自发进行
C.有气体参加的反应,通入惰性气体,压强增大,从而反应速率加快
D.催化剂不影响反应的活化能,但能增大单位体积的活化分子百分数,加快反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将一定浓度的盐酸和醋酸加水稀释,溶液的导电能力随溶液体积变化的曲线如图所示。下列说法中正确的是( )
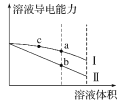
A.两溶液稀释前的浓度相同
B.a、b、c三点溶液的pH由大到小顺序为a>b>c
C.a点的Kw值比b点的Kw值大
D.a点水电离的c(H+)大于c点水电离的c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量Na2O2和NaHCO3均匀混合物分成质量相等的甲乙两份。将甲投入100mL稀盐酸,固体完全溶解,收集到标况下的干燥气体2.24L。再将生成的气体全部导入装有乙的干燥管中,充分吸收后,收集到一种单质气体,标准状况下体积为2.016L。根据以上信息,下列有关推断不正确的是( )
A. 甲乙两份混合物中均含Na2O2 0.16mol
B. 甲乙两份混合物中均含NaHCO3 0.02mol
C. 原混合物中Na2O2和NaHCO3物质的量之比无法确定
D. 盐酸物质的量浓度可能为3.4mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的( )
A.常温下,将 1mL pH=3 的醋酸溶液加水稀释到 100mL,测得其 PH<5
B.红棕色的 NO2,加压后颜色先变深后变浅
C.工业合成氨中通常采取高温及加入催化剂,提高生产效益
D.实验室制取氨气利用浓氨水和固体氢氧化钠混合的方法
查看答案和解析>>
科目: 来源: 题型:
【题目】现取![]() 铝镁合金,使其在一定浓度的稀硝酸中恰好完全溶解
铝镁合金,使其在一定浓度的稀硝酸中恰好完全溶解![]() 假定硝酸的还原产物只有
假定硝酸的还原产物只有![]() ,向反应后的混合溶液中滴加
,向反应后的混合溶液中滴加![]() 溶液,当滴加
溶液,当滴加![]() 时,得到沉淀的质量恰好为最大值
时,得到沉淀的质量恰好为最大值![]() ,则下列有关说法不正确的是
,则下列有关说法不正确的是![]()
![]()
A.沉淀中氢氧根离子的质量为![]() B.恰好溶解后溶液中的
B.恰好溶解后溶液中的![]() 的物质的量为
的物质的量为![]()
C.生成标准状况下NO气体的体积为![]() D.与合金反应的硝酸的物质的量为
D.与合金反应的硝酸的物质的量为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com