
科目: 来源: 题型:
【题目】I.利用如图所示装置测定中和热的实验步骤如下:
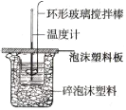
①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL0.55mol·L-1 NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,使之混合均匀,测得混合溶液最高温度。
回答下列问题:
(1)所用NaOH溶液要稍过量,理由是__。
(2)环形玻璃搅拌棒搅拌溶液的操作是__。
(3)___(填“能”或“不能”)用Ba(OH)2溶液和H2SO4溶液代替NaOH溶液和盐酸,理由__。
(4)现将一定量的稀NaOH溶液、Ca(OH)2溶液、稀氨水分别和1L1mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔΗ1、ΔΗ2、ΔΗ3,则ΔΗ1、ΔΗ2、ΔΗ3的大小关系为___。
II.实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验。请你完成下列填空:
步骤一:配制250mL0.1000mol/L NaOH标准溶液。
步骤二:取20.00mL待测稀盐酸放入锥形瓶中,并滴加2–3滴酚酞溶液作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作4次,记录数据如下。
实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,消耗NaOH溶液的体(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 20.02 | 20.00 |
2 | 0.10 | 20.00 | 20.00 |
3 | 0.10 | 19.00 | 20.00 |
4 | 0.10 | 19.98 | 20.00 |
(1)步骤一需要称量氢氧化钠固体的质量为___g,配制标准溶液需要用到玻璃棒,烧杯外,还需要的玻璃仪器有___。
(2)根据上述数据,可计算出该盐酸的浓度为___(保留小数点后2位)。
(3)在上述实验中,下列操作(其他操作正确)会造成测定结果(待测液浓度值)偏高的有__。
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗
D.滴定到达终点时,仰视读出滴定管读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
III.氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.1000mol/L的酸性KMnO4溶液进行滴定,回答下列问题:
(1)配平离子方程式:__MnO4-+__HSO3-+__H+=__
(2)用KMnO4进行滴定时,KMnO4溶液应装在___滴定管中(填酸式或碱式),判断滴定终点的现象是:滴入最后一滴KMnO4溶液时,___。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求回答下列问题:
(1)生活中明矾常作净水剂,其净水的原理是___(用离子方程式表示)。
(2)在25℃时,pH等于9和pH等于11的两种氢氧化钠溶液等体积混合后(忽略溶液体积的变化),溶液中的氢离子浓度为___。
(3)现将0.2mol·L-1的NH3·H2O溶液与0.1mol·L-1的HCl溶液等体积混合,写出该混合溶液质子守恒式:___。
(4)FeCl2溶液蒸干并灼烧得到的物质是___(填化学式)。
(5)浓度均为0.1molL﹣1的①H2S、②NaHS、③Na2S、④H2S和NaHS混合液,溶液pH从大到小的顺序是___。(用序号表示)
(6)在常温下,现有下列四种溶液:①0.1mol·L-1 CH3COONH4溶液,②0.1mol·L-1NH4HSO4溶液,③0.1mol·L-1 NH3·H2O和0.1mol·L-1 NH4Cl混合溶液,④0.1mol·L-1 NH3·H2O溶液。比较①、②、③、④溶液中c(NH4+)由小到大的顺序为___(用序号表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
请回答下列问题:
(1) 同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是_________。
(2) 0.1mo1/L的H2C2O4溶液与0.1mo1/L的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为________________。
(3)pH相同的NaC1O和CH3COOK溶液中,[c(Na+)-c(C1O-)]______[c(K+)-c(CH3COO-)](填“>”、“<”或“=”) 。
(4) 向0.1mo1/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此时溶液pH=_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组用100 mL 1 mol/L NaOH溶液完全吸收了a mol CO2后得到溶液A(液体体积无变化)。为了确定溶液A的溶质成分及a值,该兴趣小组的同学进行了如下实验。请帮助他们完成下列相应实验内容。
[提出假设]
假设Ⅰ:溶液A的溶质为NaOH、Na2CO3;
假设Ⅱ:溶液A的溶质为Na2CO3;
假设Ⅲ:溶液A的溶质为Na2CO3、NaHCO3;
假设Ⅳ:溶液A的溶质为___。
[实验过程]
(1)甲同学取少量溶液A于试管,再向试管中滴加几滴酚酞溶液,溶液A变红,由此得出假设I成立。
(2)乙同学分析后认为甲同学的实验结论有误。请用离子方程式说明乙同学的判断依据_____;他进一步提出,应先取少量溶液,向其中加入足量的___溶液,来检验溶液A是否含___,结果加入检验溶液后观察到溶液A变浑浊。
(3)丙同学为了检验溶液A是否还含其它溶质,他将乙同学所得浑浊溶液进行过滤,并把滤液分为两份,向其中的一份加入稀硫酸,有无色气体生成,则假设___正确。
(4)为准确测定a值,丁同学取了10 mL 溶液A在锥形瓶中,用滴定管向其中加入某浓度的稀硫酸,记录加入硫酸的体积与生成气体的情况,并绘制成如图:

则a=___,所加硫酸的物质的量浓度为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是有关外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是( )
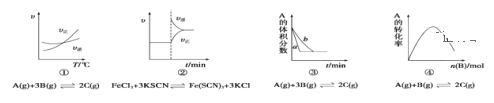
A.①是其他条件一定时,反应速率随温度变化的图像,则逆反应ΔH>0
B.②是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像
C.③是在有无催化剂存在条件下,建立平衡过程的图像,a是使用催化剂时的曲线
D.④是一定条件下,向含有一定量A的恒容密闭容器中逐渐加入B,达平衡时A的转化率的图象
查看答案和解析>>
科目: 来源: 题型:
【题目】NaHSO3可被过量KIO3氧化,当NaHSO3完全消耗时即有I2析出。某课题组用淀粉作指示剂,通过测定溶液变蓝所用时间来探究影响化学反应速率的因素。
(1)写出NaHSO3溶液与过量KIO3溶液反应生成I2的离子方程式:____________。
(2)调节反应物浓度和温度进行对比实验,记录结果如下:
编号 | 0.02mol/LNaHSO3溶液/mL | 0.02mol/LKIO3溶液/mL | H2O/mL | 反应温度/℃ | 溶液变蓝的时间t/s |
① | 10 | 15 | a | 10 | t1 |
② | 10 | 40 | 0 | 10 | t2 |
③ | 10 | b | 0 | 20 | t3 |
表中a=________,b=________。
(3)改变反应温度,重复实验③,得到温度(T)与溶液变蓝所需时间(t)的关系如下图所示(“×××”表示超过50℃后溶液不会再变蓝)。
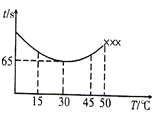
①在30℃下,若溶液变蓝时,I2的物质的量为n mol,则从反应开始至溶液变蓝,IO3-的平均反应速率______mol·L-1·s-1(写出表达式即可,不要化简)。
②根据图像,请你分析温度低于50℃时,溶液变蓝所需时间与反应温度的关系:____。
(4)将NaHSO3溶液与KIO3溶液混合(预先加入可溶性淀粉为指示剂),用速率检测仪检测出起始阶段反应速率逐渐增大,一段时间后反应速率又逐渐减小。课题组对起始阶段反应速率逐渐增大的原因提出如下假设,请你完成假设二:
假设一:反应生成的I2对反应起催化作用;
假设二:_________________________________________;
(5)请你设计实验验证上述假设一,完成下表中内容(反应速率可用测速仪测定):____。
实验方案(不要求写出具体操作过程) | 预期实验现象和结论 |
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应①:CO(g)+CuO(s) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2该温度下反应③:CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1=![]()
B.对于反应③,恒容时,温度升高,H2浓度减小,则K变大
C.反应③的平衡常数K=![]()
D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关叙述中正确的是( )
A.常温下,pH=4的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-)
B.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
C.已知25℃时NH4CN溶液显碱性,则25℃时的电离平衡常数K(NH3·H2O)<K(HCN)
D.0.1mol/L醋酸溶液加少量水稀释![]() 增大
增大
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某温度下水的离子积常数为Kw,下列溶液一定呈中性的是( )
A.pH=7的溶液B.c(H+)=![]() mol·L-1的溶液
mol·L-1的溶液
C.由强酸、强碱等物质的量反应得到的溶液D.非电解质溶于水得到的溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在水溶液中1 mol ClOx-(x=0,1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法错误的是
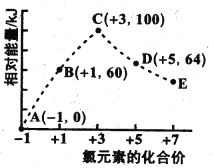
A. 上述离子中结合H能力最强的是E
B. 上述离子中最稳定的是A
C. C→B+D反应的热化学方程式为2ClO2-(aq)=ClO3-(ag)+ClO-(aq) △H=-76kJ·mol-1
D. B→A+D的反应物的键能之和小于生成物的键能之和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com