
科目: 来源: 题型:
【题目】某原电池的装置如图所示,总反应为 H2(g)+HgO(s)=H2O(1)+Hg(1),其中阴离子交换膜只允许阴离子和水分子通过。下列说法正确的是 ( )
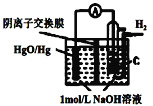
A.正极反应为:HgO(s)2e+H2O=Hg(l)+2OH
B.放电结束后,溶液的碱性不变
C.OH通过离子交换膜从负极向正极移动,保持溶液中电荷平衡
D.每反应 2.24 L(标准状况下)氢气,交换膜通过 0.2 mol 离子
查看答案和解析>>
科目: 来源: 题型:
【题目】对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ(pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ(pH=4,含Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是
A. 在0~20min内,I中M的分解速率为0.015 mol·L-1·min-1
p>B. 水样酸性越强,M的分解速率越快C. 在0~25min内,III中M的分解百分率比II大
D. 由于Cu2+存在,IV中M的分解速率比I快
查看答案和解析>>
科目: 来源: 题型:
【题目】沙利度胺是一种重要的合成药物,具有镇静、抗炎症等作用。有机物H是合成它的一种中间体,合成路线如图(部分反应条件和产物未列出)。
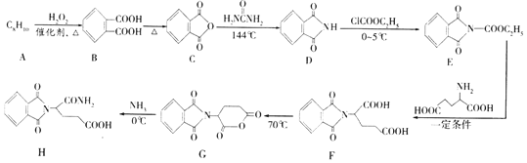
回答下列问题:
(1)A的化学名称为______,E→F的反应类型为______,H中官能团的名称为______。
(2)判断化合物F中有______个手性碳原子。D→E的反应方程式为______。
(3)写出符合下列条件的B的同分异构体______(写出一种即可,不考虑立体异构)
①能与FeC13溶液发生显色反应
②1mol该化合物能与4mol[Ag(NH3)2]OH反应
③其核磁共振氢谱显示有4种不同化学环境的氢
(4)结合上述流程中的信息,写出以1,4-丁二醇为原料制备化合物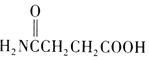 的合成路线(其他试剂任选)______。
的合成路线(其他试剂任选)______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)△H=+100kJ/mol的能量变化如图所示,判断下列叙述中正确的是
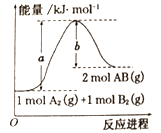
A. 加入催化剂,该反应的反应热△H将减小
B. 每生成2molA-B键,将吸收bkJ能量
C. 每生成2分子AB吸收(a-b)kJ能量
D. 该反应正反应的活化能大于100kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子电池的广泛应用要求处理锂电池废料以节约资源、保护环境。锂离子二次电池正极铝钴膜主要含有LiCoO2、A1等,处理该废料的一种工艺如下图所示:
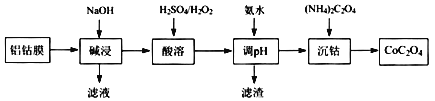
回答下列问题:
(l) Li元素在元素周期表中的位置为____________,LiCoO2中Co的化合价是____。
(2)“碱浸”时Al溶解的离子方程式为________。
(3)“酸溶”时加入H2O2的目的是____,调节pH后所得滤渣主要为____。
(4)“沉钴”的离子方程式为________。
(5)配制100 mL l.0 mol/L (NH4)2C2O4溶液,需要的玻璃仪器除玻璃棒、烧杯外,还需要_________。
(6)取CoC2O4固体4.41 g在空气中加热至300℃,得到钴的氧化物2.41 g,则该反应的化学方程式为 _________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】锂离子二次电池正极材料磷酸亚铁锂是应用广泛的正极材料之一。一种制备磷酸亚铁锂的化学方法为:C+4FePO4+2Li2CO3![]() 4LiFePO4+3CO2↑.回答下列问题:
4LiFePO4+3CO2↑.回答下列问题:
(1)Fe失去电子变成为阳离子时首先失去______轨道的电子。
(2)C、O、Li原子的第一电离能由大到小的顺序是______;PO43-的空间构型为______。
(3)C与Si同主族,CO2在高温高压下所形成的晶体结构与SiO2相似,该晶体的熔点比SiO2晶体______(填“高”或“低”)。硅酸盐和SiO2一样,都是以硅氧四面体作为基本结构单元,下图表示一种含n个硅原子的单链式多硅酸根的结构(投影如图1所示),Si原子的杂化类型为______,其化学式可表示为______。

(4)图2表示普鲁士蓝的晶体结构(![]() 个晶胞,K+未标出,每隔一个立方体在立方体体心有一个钾离子)。
个晶胞,K+未标出,每隔一个立方体在立方体体心有一个钾离子)。
①普鲁士蓝晶体中每个Fe3+周围最近且等距离的Fe2+数目为______个。
②晶体中该立方体的边长为a nm,设阿伏加德罗常数为NA,其晶体密度为______gcm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁及其化合物在生产和生活中有着广泛的应用.
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
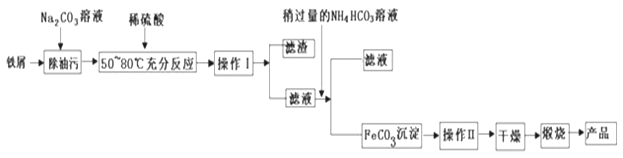
回答下列问题:
(1)操作Ⅰ、II的名称分别是______、_______.写出在空气中煅烧FeCO3生成Fe2O3的化学方程式__________________________。
(2)某同学在实验室中用KMnO4溶液滴定的方法来测定绿矾(FeSO47H2O)样品的纯度,操作过程如下:
a.称取3.00g绿矾(FeSO47H2O)样品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①滴定达到终点时锥形瓶中溶液颜色变化为:__________________且半分钟内不恢复原色
②计算上述样品中FeSO47H2O的质量分数为_______ 已知(M(FeSO47H2O)=278g/mol)
③写出酸性KMnO4溶液与FeSO4溶液反应的离子方程式_________________________
④下列操作会导致样品中FeSO47H2O的质量分数的测定结果偏高的有_________.
a.盛装标准液的滴定管没有用标准液润洗
b.未干燥锥形瓶
c.滴定终点时滴定管尖嘴中产生气泡
d.量取待测液,视线注视刻度时开始平视、结束俯视.
查看答案和解析>>
科目: 来源: 题型:
【题目】乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为:C2H5OH(g)+IB(g)ETBE(g)△H.回答下列问题:
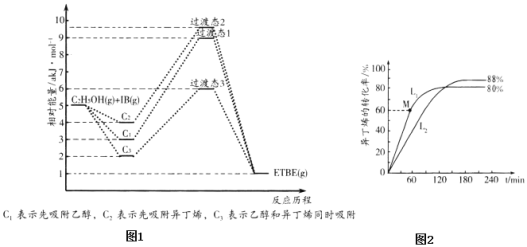
(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图1所示,该反应的△H=______a kJmol-1.反应历程的最优途径是______(填C1、C2或C3)。
(2)在刚性容器中按物质的量之比1:1充入乙醇和异丁烯,在378K与388K时异丁烯的转化率随时间变化如图2所示。
①378K时异丁烯的转化率随时间变化的曲线为______(填L1或L2)。
②388K时,以物质的量分数表示的化学平衡常数K=______。(物质的量分数为某组分的物质的量与总物质的量的比)
③已知反应速率v=v正-v逆=k正x(C2H5OH)x(IB)-k逆x(ETBE),其中秒正为正反应速率,v逆为逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数,计算M点![]() =______(保留到小数点后 1位)。
=______(保留到小数点后 1位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用所学化学反应原理,解决以下问题:
(1)一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示,请回答下列问题:
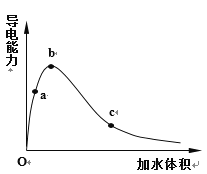
①写出冰醋酸电离方程式____________
②加水过程中,其水溶液导电能力变化的原因是:_______________________________________
③a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:__________(填“相同”、“a点大”、“b点大”、“c点大”)
(2)常温下,将0.2 mol·L-1的CH3COOH和0.1 mol·L-1的NaOH溶液等体积混合,所得溶液的pH=5(溶液体积变化忽略不计),则该溶液中:
c(CH3COO) + c(CH3COOH)= _______mol/L
c(H+) - c(CH3COO)+ c(Na+) = _______mol/L
(3)KAl(SO4)2·12H2O可做净水剂,其原理是____________________________________(用离子方程式表示)
(4)在0.10 mol·L-1 Na2SO3溶液中,离子浓度由大到小的顺序为___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮元素可形成多种化合物,在工业生产中具有重要价值。 请回答下列问题:
(1)已知拆开1molH-H 键,1molN-H键, 1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应合成NH3的热化学方程式为___________________________________。
(2)在绝热、容积固定的密闭容器中发生反应:N2(g)+3H2(g) ![]() 2NH3(g),下列说法能说明上述反应达到平衡的是___________(填序号)。
2NH3(g),下列说法能说明上述反应达到平衡的是___________(填序号)。
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N—H键的同时生成n mol N≡N键
③N2、H2、NH3的物质的量浓度之比为1∶3∶2
④混合气体的平均摩尔质量不变。
⑤容器内的气体密度不变
(3)一定温度下,2L密闭容器中充入0.40 mol N2O4,发生反应:N2O4(g) ![]() 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
时间/s | 20 | 40 | 60 | 80 | 100 |
C(NO2)/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
①升高温度时,气体颜色加深,则正反应是_________(填“放热”或“吸热”)反应。
②该温度下反应的化学平衡常数数值为_____________。
③相同温度下,若开始向该容器中充入0.80molN2O4,则达到平衡后: c(NO2) ______ 0.60mol·L-1(填“>”、 “=”或“<”)
(4)N2O5是一种新型硝化剂,其性质和制备受人们关注。现以 H2、O2、熔融盐 Z(Na2CO3)组成的燃料电池电解制备N2O5,装置如图所示,其中Y为CO2。
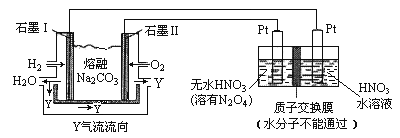
①写出石墨I电极上发生反应的电极反应式 _______________________________________;
②在电解池中生成N2O5的电极反应式为_______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com