
科目: 来源: 题型:
【题目】固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H= -49.0 kJ/mol
CH3OH(g)+H2O(g) △H= -49.0 kJ/mol
某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标):
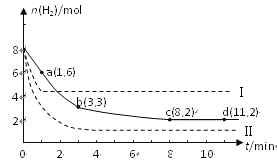
回答下列问题:
(1)该反应在_____条件下能自发进行(填编号)。
A.高温 B.低温 C.任何温度
(2)该反应在0~8 min内CO2的平均反应速率是_________mol/(Lmin)。
(3)该反应的平衡常数K=_______。
(4)仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,曲线Ⅰ改变的条件可能是__________,曲线Ⅱ改变的条件可能是_______________。
若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是______________。
(5)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是
________。
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.有效碰撞理论可指导怎样提高原料的转化率
C.勒夏特列原理可指导怎样使用有限原料多出产品
D.催化剂的使用是提高产率的有效方法
E.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将 0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成 NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H = -38.6kJ·mol-1
2NH3(g) △H = -38.6kJ·mol-1
C.HCl 和 NaOH 反应的中和热△H=-57.3 kJ·mol-1 ,则H2SO4和Ba(OH)2反应的中和热 △H = 2×(-57.3)kJ·mol -1
D.在101kPa 时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1) △H =-571.6 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】将4molA气体和2molB气体在2L的容器中发生如下反应:2A(g)+B(g)![]() 2C(g)。若经2s后测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是
2C(g)。若经2s后测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是
①用物质A表示的反应的平均速率为0.3mol/(L.s)
②用物质B表示的反应的平均速率为0.6mol/(L.s)
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol/L
A.①③B.②④C.①④D.②③
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法或表示方法中正确的是
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(s,石墨) = C(s,金刚石) ΔH=+1.9kJ/mol可知,金刚石比石墨稳定
C.在101kPa、25℃时,H2的燃烧热为ΔH= —285.8kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g) = 2H2O(g) ΔH= —285.8kJ/mol
D.稀溶液中:H+(aq)+OH-(aq) = H2O(l) ΔH= —57.3kJ/mol ,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学欲探究FeCl3溶液与NaHSO3溶液的反应,设计、完成实验并记录如下:
装置 | 反应时间 | 实验现象 |
| 0~1 min | 产生红褐色沉淀Fe(OH)3,有刺激性气味气体SO2逸出 |
1~30 min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 | |
30 min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
已知: Fe(OH)3+SO32-![]()
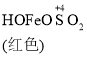
![]()
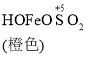
![]() Fe2++SO42-
Fe2++SO42-
下列有关反应速率和化学平衡说法不正确的是
A. 生成红色配合物的反应速率较快,红色配合物生成橙色配合物的速率较慢
B. 增大溶液中SO32-浓度可以加速红褐色沉淀Fe(OH)3迅速溶解
C. O2的作用下,橙色HOFeOSO2浓度下降,平衡![]() 不断正向移动
不断正向移动
D. 30min时,若向该无色溶液中滴加少量FeCl3溶液,无明显现象
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,可逆反应A(气)+3B(气)![]() 2C(气)达到平衡的标志是( )
2C(气)达到平衡的标志是( )
A. C的生成速率与B的生成速率相等B. A、B、C的浓度不再发生变化
C. A、B、C的分子数之比为1∶3∶2D. 单位时间内消耗nmolA,同时消耗3nmolB
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应2A(g) + 3B(g) = 2C(g) + D(g),下列表示反应速率最快的是( )
A. υ(A) =0.5mol·L-1·min-1B. υ(B)=1.2mol·L-1·min-1
C. υ(C)=0.4mol·L-1·s-1D. υ(D)=0.3mol·L-1·s-1
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭容器中充入3 mol A和2 mol B发生如下反应:3A(g)+B(g)![]() xC(g)。该反应达到平衡后,C的体积分数为W%。若维持容器的容积和温度不变,按起始物质的量A 0.6 mol、B 1.2 mol、C 1.6 mol充入容器达到平衡后,C的体积分数还为W%。则x的值( )
xC(g)。该反应达到平衡后,C的体积分数为W%。若维持容器的容积和温度不变,按起始物质的量A 0.6 mol、B 1.2 mol、C 1.6 mol充入容器达到平衡后,C的体积分数还为W%。则x的值( )
A. 只能为2 B. 只能为4 C. 可能为2,可能为4 D. 无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.将FeCl3饱和溶液煮沸可得到带正电荷的Fe(OH)3胶体
B.0.5 molH2SO4与0.5 molBa(OH)2完全反应所放出的热量即为中和热
C.H2O的沸点高于H2S是因为O-H键的键能大于S-H键的键能
D.向新制氯水中加入CaCO3可使溶液中HClO浓度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com