
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП![]() ФГЮоЩЋШмвКжаПЩФмКЌга
ФГЮоЩЋШмвКжаПЩФмКЌга![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() жаЕФШєИЩжжЃЌвРДЮНјааЯТСаЪЕбщЁЃЙлВьЕНЯжЯѓШчЯТЃК
жаЕФШєИЩжжЃЌвРДЮНјааЯТСаЪЕбщЁЃЙлВьЕНЯжЯѓШчЯТЃК
ЂйгУpHЪджНМьбщЃЌШмвК![]() ЃЛ
ЃЛ
ЂкЯђШмвКжаЕЮМгТШЫЎЃЌЮоЦјЬхВњЩњЃЌдйМгШы![]() еёЕДЁЂОВжУЃЌ
еёЕДЁЂОВжУЃЌ![]() ВуГЪГШКьЩЋЃЌгУЗжвКТЉЖЗЗжвКЃЛ
ВуГЪГШКьЩЋЃЌгУЗжвКТЉЖЗЗжвКЃЛ
ЂлЯђЗжвККѓЕФЫЎШмвКжаМгШы![]() КЭ
КЭ![]() ЛьКЯвКЃЌгаАзЩЋГСЕэВњЩњЁЃ
ЛьКЯвКЃЌгаАзЩЋГСЕэВњЩњЁЃ
ЂмСэШЁдШмвКЩйСПМгШы![]() КЭбЮЫсЕФЛьКЯвКЃЌВњЩњАзЩЋГСЕэЁЃ
КЭбЮЫсЕФЛьКЯвКЃЌВњЩњАзЩЋГСЕэЁЃ
ЛиД№ЯТСаЮЪЬтЃК
(1)ШмвКжаПЯЖЈКЌгаЕФРызгЪЧ_________ЃЛПЯЖЈУЛгаЕФРызгЪЧ_________ЁЃ
(2)аДГіВНжшЂкжаЕФРызгЗНГЬЪН_________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕААзжЪжаКЌгаCЁЂHЁЂOЁЂNЁЂSЕШдЊЫиЃЌЪГЮяжаЕФЬњжївЊвдШ§МлЬњгыЕААзжЪКЭєШЫсНсКЯГЩТчКЯЮяЕФаЮЪНДцдкЁЃ
(1)дкЕААзжЪжаЩцМАЕФЬМЁЂЕЊЁЂбѕдЊЫиЕквЛЕчРыФмгЩаЁЕНДѓЕФЫГађЪЧ________________ЃЛЛљЬЌЬњдзгЕФМлЕчзгХХВМЪНЮЊ____________ЁЃ
(2)KSCNЪЧМьбщFe3ЃЋЕФЪдМСжЎвЛЃЌгыSCNЃЛЅЮЊЕШЕчзгЬхЕФвЛжжЗжзгЮЊ________(ЬюЛЏбЇЪН)ЁЃ1 mol CNЃжаКЌгаЕФІаМќЕФЪ§ФПЮЊ____________________ЁЃ
(3)FeCl3жаЕФЛЏбЇМќОпгаУїЯдЕФЙВМладЃЌеєЦћзДЬЌЯТвдЫЋОлЗжзгЃЈЦфЗжзгЪНЮЊFe2Cl6ЃЉДцдкЕФНсЙЙЪНЮЊ________________ЃЌЦфжаFeЕФХфЮЛЪ§ЮЊ____________ЁЃ
(4)Н№ЪєЛЏКЯЮяCu2ZnКЯН№ФмЕМЕчЃЌШлЕуНЯИпЃЌЧПЖШЁЂгВЖШНЯДѓЁЃCu2ZnКЯН№ЕФОЇЬхРраЭЪЧ_______ЁЃ
(5)ФГКЌЭЛЏКЯЮяЕФРызгНсЙЙШчЭМЫљЪОЁЃ
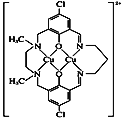
ЂйИУРызгжаДцдкЕФзїгУСІга_______________ЃЛ
a.РызгМќЁЁЁЁb.ЙВМлМќЁЁЁЁ c.ХфЮЛМќЁЁЁЁd.ЧтМќ e.ЗЖЕТЛЊСІ
ЂкИУРызгжаNдзгЕФдгЛЏРраЭга________ЁЃ
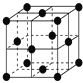
(6)ЭОЇЬхЮЊУцаФСЂЗНзюУмЖбЛ§ЃЌМДдкОЇЬхНсЙЙжаПЩвдЗжИюГівЛПще§СЂЗНЬхЕФНсЙЙЕЅдЊЃЌН№ЪєдзгДІгке§СЂЗНЬхЕФАЫИіЖЅЕуКЭСљИіУцЩЯЃЌвбжЊЭЕФдзгАыОЖЮЊ127.8 pmЃЌСаЪНМЦЫуОЇЬхЭЕФУмЖШЃКІб=______________gЁЄcm-3(СаГіМЦЫуЪНМДПЩ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдЊЫиXЁЂQЁЂYЁЂZЁЂMЁЂRОљЮЊЖЬжмЦкжїзхдЊЫиЃЌЧвдзгађЪ§вРДЮдіДѓЁЃвбжЊYдзгзюЭтВуЕчзгЪ§гыКЫЭтЕчзгзмЪ§жЎБШЮЊ3ЁУ4ЃЌMдзгЕФзюЭтВуЕчзгЪ§гыДЮЭтВуЕчзгЪ§жЎБШЮЊ3ЁУ4ЃЛRЃЁЂZЃЋЁЂXЃЋРызгАыОЖж№НЅМѕаЁЃЛЛЏКЯЮяXRГЃЮТЯТЮЊЦјЬхЃЌQКЭYдкжмЦкБэжаЕФЮЛжУЯрСкЁЃЧыЛиД№ЯТСаЮЪЬтЁЃ
(1)MдзгЕФМлЕчзгХХВМЭМЪЧ__________ЃЌQЕФГЃМћЧтЛЏЮяЕФСЂЬхЙЙаЭЪЧ_________________ЁЃ
(2)аДГіXЁЂYЁЂRАДдзгИіЪ§жЎБШ1ЁУ1ЁУ1аЮГЩЕФЛЏКЯЮяЕФНсЙЙЪН:_______________ЁЃ
(3)XгыYПЩЗжБ№аЮГЩ10ЕчзгКЭ18ЕчзгЕФЗжзгЃЌаДГіИУ18ЕчзгЗжзгзЊЛЏГЩ10ЕчзгЗжзгЕФЛЏбЇЗНГЬЪН:_________ЁЃ
(4)аДГіЕЅжЪRЕФвЛжжЙЄвЕгУЭО:_______________ЁЃ
(5)ЭМБэЪОгЩЩЯЪідЊЫижаЕФФГСНжждЊЫизщГЩЕФЦјЬхЗжзгдквЛЖЈЬѕМўЯТЕФУмБеШнЦїжаГфЗжЗДгІЧАКѓЕФзЊЛЏЙиЯЕЃЌаДГіИУзЊЛЏЙ§ГЬЕФЛЏбЇЗНГЬЪН:_______ЁЃ
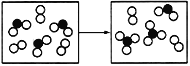
(6)гЩXЁЂYЁЂZЁЂMЫФжждЊЫиПЩаЮГЩвЛжжРызгЛЏКЯЮяAЃЌвбжЊAМШФмгыбЮЫсЗДгІЃЌгжФмгыЧтбѕЛЏФЦШмвКЗДгІЃЌЛЙФмКЭТШЫЎЗДгІЃЌаДГіAгыТШЫЎЗДгІЕФРызгЗНГЬЪН:_____ЁЃ
(7)ПЦбЇМвШЯЮЊДцдкQX5етжжЮяжЪЃЌЧвдЄВтЦфгыЫЎОчСвЗДгІЗХГіЦјЬхЃЌЫљЕУЫЎШмвКГЪШѕМюадЃЌаДГіИУЗДгІЕФЛЏбЇЗНГЬЪН:______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП![]() ФГаЫШЄаЁзщбаОП
ФГаЫШЄаЁзщбаОП![]() ЦјЬхЛЙд
ЦјЬхЛЙд![]() ЁЂ
ЁЂ![]() ЃЌЫћУЧЪЙгУЕФвЉЦЗКЭзАжУШчЭМЫљЪОЃК
ЃЌЫћУЧЪЙгУЕФвЉЦЗКЭзАжУШчЭМЫљЪОЃК
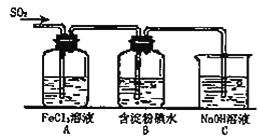
(1)![]() ЦјЬхгы
ЦјЬхгы![]() ЗДгІЕФжївЊВњЮяЪЧ___________ЁЃ
ЗДгІЕФжївЊВњЮяЪЧ___________ЁЃ![]() ЬюРызгЗћКХ
ЬюРызгЗћКХ![]()
(2)ЯТСаЪЕбщЗНАИПЩвдгУгкдкЪЕбщЪвжЦШЁЫљаш![]() ЕФЪЧ________ЁЃ
ЕФЪЧ________ЁЃ
A. ![]() ШмвКгы
ШмвКгы![]() B.
B. ![]() ЙЬЬхгыХЈСђЫс
ЙЬЬхгыХЈСђЫс
C. ЙЬЬхСђдкДПбѕжаШМЩе D. ЭгыШШХЈ![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП(1)500ЁцЪБЃЌдк2LУмБеШнЦїФкЗЂЩњ2SO2(g)+O2(g)![]() 2SO3(g)ЕФЗДгІЃЌЦфжаn(SO2)ЫцЪБМфЕФБфЛЏШчЯТБэ:
2SO3(g)ЕФЗДгІЃЌЦфжаn(SO2)ЫцЪБМфЕФБфЛЏШчЯТБэ:
ЪБМф(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
ЂйдкЕк5sЪБЃЌSO2ЕФзЊЛЏТЪЮЊ__________________ЁЃ
ЂкФмЫЕУїИУЗДгІвбДяЕНЦНКтзДЬЌЕФЪЧ_________________ЁЃ
a. v(SO2)=v(O2) b.ЛьКЯЦјЬхжаSO2ЕФЬхЛ§ЗжЪ§БЃГжВЛБф
c.vФц(SO2)=2vе§(O2) d.ШнЦїФкУмЖШБЃГжВЛБф
(2)ЙшЪЧаХЯЂММЪѕЕФЙиМќВФСЯЁЃ
ЛЏбЇМќ | HЃH | SiЃCl | SiЃSi | HЃCl |
E/kJЁЄmol-1 | 436.0 | 360 | 176 | 431.8 |
гУH2ЛЙдЦјЬЌSiCl4жЦЕУ28gЙшЕФЗДгІШШЮЊ__________________ЁЃ
(3)ФПЧАЃЌЯћГ§ЕЊбѕЛЏЮяЮлШОгаЖржжЗНЗЈЁЃ
гУCH4ДпЛЏЛЙдЕЊбѕЛЏЮяПЩвдЯћГ§ЕЊбѕЛЏЮяЕФЮлШОЁЃвбжЊ:
ЂйCH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ІЄH=Ѓ574 kJЁЄmol-1
ЂкCH
ЂлH2O(g)=H2O(l) ІЄH=Ѓ44.0 kJЁЄmol-1
аДГіCH4(g)гыNO2(g)ЗДгІЩњГЩN2(g)ЁЂCO2(g)КЭH2O(l)ЕФШШЛЏбЇЗНГЬЪН_______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЖдЗжзгаджЪЕФНтЪЭжаЃЌВЛе§ШЗЕФЪЧ(ЁЁ )
A.SO2взШмгкЫЎжЛЪЧвђЮЊЯрЫЦЯрШмдРэ
B.ШщЫс(![]() )ЗжзгжаКЌгавЛИіЪжадЬМдзг
)ЗжзгжаКЌгавЛИіЪжадЬМдзг
C.H3PO4ЗжзгжаPдзгВЩШЁsp3дгЛЏ
D.гЩЭМжЊЫсадЃКH3PO4>HClOЃЌвђЮЊH3PO4жаЗЧєЧЛљбѕдзгЪ§ДѓгкДЮТШЫсжаЗЧєЧЛљбѕдзгЪ§

ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПТШЛЏЬњЪЧвЛжжГЃМћЕФЫЎДІРэМСЃЌЮоЫЎТШЛЏЬњгіГБЪЊПеЦјЃЌМЋвзЮќЫЎЩњГЩ![]() ЁЃдкЪЕбщЪвжаЃЌПЩвдВЩгУЯТСавЧЦїКЭвЉЦЗжЦШЁНЯДПЕФЮоЫЎТШЛЏЬњЙЬЬхЁЃ
ЁЃдкЪЕбщЪвжаЃЌПЩвдВЩгУЯТСавЧЦїКЭвЉЦЗжЦШЁНЯДПЕФЮоЫЎТШЛЏЬњЙЬЬхЁЃ

(1)ЪЕбщПЊЪМЪБЃЌЯШЕуШМ______ДІЕФОЦОЋЕЦ![]() ЬюAЛђ
ЬюAЛђ![]() ЁЃAжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ______ЁЃ
ЁЃAжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ______ЁЃ
(2)![]() зАжУжаЪЂЗХЕФЪЧБЅКЭЪГбЮЫЎЃЌЦфзїгУЮЊ______ЁЃ
зАжУжаЪЂЗХЕФЪЧБЅКЭЪГбЮЫЎЃЌЦфзїгУЮЊ______ЁЃ
(3)![]() зАжУжаЕФЪдМСЮЊХЈСђЫсЃЌЦфзїгУЪЧ______ЁЃгУвЛМўвЧЦїзАЬюЪЪЕБЪдМСКѓЃЌвВПЩЦ№ЕНFКЭGЕФзїгУЃЌЫљзАЬюЕФЪдМСЮЊ______ЁЃ
зАжУжаЕФЪдМСЮЊХЈСђЫсЃЌЦфзїгУЪЧ______ЁЃгУвЛМўвЧЦїзАЬюЪЪЕБЪдМСКѓЃЌвВПЩЦ№ЕНFКЭGЕФзїгУЃЌЫљзАЬюЕФЪдМСЮЊ______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУ98%ЕФХЈСђЫсЃЈУмЖШЮЊ1.84gЁЄcm-3ЃЉХфжЦ1molЁЄL-1ЕФЯЁСђЫс100 mLЃЌЯжИјГіЯТСавЧЦї(ХфжЦЙ§ГЬжаПЩФмгУЕН)ЃКЂй100 mLСПЭВ Ђк10 mLСПЭВ Ђл50 mLЩеБ ЂмЭаХЬЬьЦН Ђн100 mLШнСПЦП ЂоНКЭЗЕЮЙм ЂпВЃСЇАєЁЃАДЪЕбщЪБЪЙгУвЧЦїЕФЯШКѓЫГађЃЌХХСае§ШЗЕФЪЧ ЃЈ ЃЉ
A.ЂкЂоЂлЂпЂнЂоB.ЂкЂлЂпЂнЂоC.ЂйЂлЂнЂпЂмЂоD.ЂмЂпЂлЂнЂо
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌгУХЈЖШЮЊ![]() ЕФбЮЫсЗжБ№ж№ЕЮМгШыЕН
ЕФбЮЫсЗжБ№ж№ЕЮМгШыЕН![]() ЕФСНжжвЛдЊМюMOHЁЂROHШмвКжаЃЌpHЫцбЮЫсШмвКЬхЛ§ЕФБфЛЏШчЭМЫљЪОЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЕФСНжжвЛдЊМюMOHЁЂROHШмвКжаЃЌpHЫцбЮЫсШмвКЬхЛ§ЕФБфЛЏШчЭМЫљЪОЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧ![]()
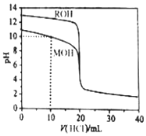
A.![]() ЪБЃЌШмвКжаЮЂСЃХЈЖШЕФЙиЯЕЪЧЃК
ЪБЃЌШмвКжаЮЂСЃХЈЖШЕФЙиЯЕЪЧЃК![]()
B.НЋЩЯЪіMOHЁЂROHШмвКЕШЬхЛ§ЛьКЯКѓЃЌгУбЮЫсЕЮЖЈжСMOHЧЁКУЗДгІЪБЃЌШмвКжаРызгХЈЖШЕФЙиЯЕЪЧЃК![]()
C.![]() ЪБЃЌШмвКжаЮЂСЃХЈЖШЕФЙиЯЕЪЧЃК
ЪБЃЌШмвКжаЮЂСЃХЈЖШЕФЙиЯЕЪЧЃК![]()
D.![]() ЪБЃЌВЛПЩФмДцдкЃК
ЪБЃЌВЛПЩФмДцдкЃК![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЭЌбЇЩшМЦШчЭМЫљЪОЪЕбщЃЌЬНОПЗДгІжаЕФФмСПБфЛЏЁЃ
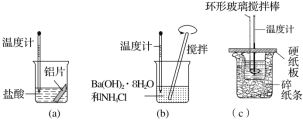
ЯТСаХаЖЯе§ШЗЕФЪЧ(ЁЁЁЁ)
A.гЩЪЕбщПЩжЊЃЌ(a)ЁЂ(b)ЁЂ(c)ЫљЩцМАЕФЗДгІЖМЪЧЗХШШЗДгІ
B.НЋЪЕбщ(a)жаЕФТСЦЌИќЛЛЮЊЕШжЪСПЕФТСЗлКѓЪЭЗХГіЕФШШСПгаЫљдіМг
C.ЪЕбщ(c)жаНЋЛЗаЮВЃСЇНСАшАєИФЮЊЬњжЪНСАшАєЖдЪЕбщНсЙћУЛгагАЯь
D.ШєгУNaOHЙЬЬхВтЖЈжаКЭШШЃЌдђВтЖЈжаКЭШШЕФЪ§жЕЦЋИп
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com