
科目: 来源: 题型:
【题目】25° C时,0.100 mol· L-1盐酸滴定25. 00 mL0. 1000 mol . L-1'氨水的滴定曲线如图所示。下列说法正确的是

A.滴定时,可迄用甲基橙或酚酞为指示剂
B.a、b两点水电离出的OH-浓度之比为10-4. 12
C.c点溶液中离子浓度大小顺序为c(Cl-) >c(NH4+)>c(H+ ) >c(OH-)
D.中和等体积等pH的氨水和NaOH溶液时消耗相同浓度盐酸的体积相等
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年2月27日,科技日报报道中科院大连化学物理研究所创新性地提出锌碘单液流电池的概念,锌碘单液流电池中电解液的利用率达到近100% ,进而大幅度提高了电池的能量密度,工作原理如图所示。下列说法正确的是

A.该电池放电时电路中电流方向为A→a→b→B→A
B.M为阴离子交换膜,N为阳离子交换膜
C.如果使用铅蓄电池进行充电,则B电极应与铅蓄电池中的Pb电极相连
D.若充电时C区增加的离子数为2NA,则A极增重65 g
查看答案和解析>>
科目: 来源: 题型:
【题目】利用图示实验装置可完成多种实验,其中不能达到相应实验目的的是

选项 | 试剂1、试剂2 | 实验目的 |
A | 过量锌粒、食醋溶液 | 测定食醋中醋酸浓度 |
B | 粗锌、过量稀硫酸 | 测定粗锌(含有不参与反应的杂质)纯度 |
C | 碳酸钠固体、水 | 证明碳酸钠水解吸热 |
D | 过氧化钠固体、水 | 证明过氧化钠与水反应产生气体 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】欲测定某NaOH溶液的物质的量浓度,可用0.100 0 mol·L-1的HCl标准溶液滴定待测碱(用甲基橙作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为________。
(2)滴定至终点的颜色变化为____________。
(3)若甲学生在实验过程中做了三组平行实验,数据记录如下,则此时消耗标准溶液的体积为__________。计算出待测NaOH溶液的物质的量浓度为______。(保留四位有效数字)
实验 序号 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1 HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.29 |
2 | 25.00 | 1.00 | 31.00 |
3 | 25.00 | 1.00 | 27.31 |
查看答案和解析>>
科目: 来源: 题型:
【题目】人类的生产、生活与化学息息相关,下列说法不正确的是![]()
![]()
A.将铝制品置于电解液中作为阳极,用电化学氧化的方法,可以在铝制品表面生成坚硬的氧化膜。
B.防治酸雨的措施可以对煤燃烧后形成的烟气脱硫,目前主要用石灰法。
C.压敏胶黏剂(即时贴)只需轻轻一压就能黏结牢固,其黏附力为分子间作用力。
D.人体所需六大营养物质:糖类、油脂、蛋白质、维生素、无机盐和水,其中产能最高的是糖类。
查看答案和解析>>
科目: 来源: 题型:
【题目】有下列六种物质的溶液:①NaCl ②NH4Cl ③Na2CO3 ④Al2(SO4)3 ⑤CH3COOH ⑥NaHCO3。
(1)25℃时,0.1mol·L-1②溶液的pH________7(填“>”、“=”或“<”);其原因是_____________(用离子方程式表示);
(2)常温下,浓度均为0.1mol/L的③和⑥的溶液中离子种类________(填“相同”或是“不相同”);
(3)常温下0.1 mol/L的⑤溶液加水稀释过程中,下列表达式的数据一定变大的是_________。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-)
(4)室温下,使用pH计测定0.1 mol/LNH4Cl溶液的pH=5.12。由此可以得到的结论是_______(填字母)。
a.溶液中c(H+)>c(OH-) b.NH4+水解是微弱的
c.NH3·H2O是弱碱 d.由H2O电离出的c(H+)<10-7 mol/L
e.物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
(5)某温度下,相同体积、相同pH的氨水和氢氧化钠溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是____,

A.a点导电能力比b点强
B.b点的KW值大于c点
C.与盐酸完全反应时,消耗盐酸体积Va>Vc
D.a、c两点c(H+)相等
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y 、Z、W是原子序数依次增大的短周期主族元素,其中Z的最外层电子数与X的核外电子总数相等。X、Z、W形成的一种化合物结构为![]() ,该物质常用于制备纳米材料以及工业催化剂。下列说法正确的是
,该物质常用于制备纳米材料以及工业催化剂。下列说法正确的是
A.元素非金属性:X>Y>Z
B.简单离子半径:Y<Z< W
C.工业上常通过电解W与Z形成的化合物制备W单质
D.简单气态氢化物的稳定性:X<Z
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空
(1)写出下列物质在水中电离方程式:
NaHSO4_____________________________NH3·H2O______________________________________________________
(2)写出下列物质水解的离子方程式:
NaHCO3___________________________ FeCl3_____________________________
(3)常温时,0.1mol/L的NaOH和0.06mol/L 的H2SO4溶液等体积混合,求混合溶液的pH为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】“碳九”是在石油提炼时获得的一系列含碳数量在9左右的烃,沸点处于汽油和柴油之间。“碳九”有两种,分为裂解碳九和重整碳九,前者主要为烷烃.烯烃等链烃,后者主要为丙苯、对甲乙米等芳香烃。下列有关说法错误的是
A.若将“碳九"添加到汽油中,可能会使汽油燃烧不充分而形成积炭
B.用溴水可以区分裂解碳九和重整碳九
C.均三甲苯( )的二氯代物有5种
)的二氯代物有5种
D.异丙苯[![]() ]和对甲乙苯(
]和对甲乙苯(![]() )互为同系物
)互为同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,它可由冰醋酸与过氧化氢在一定条件下制得;它可以迅速杀灭多种微生物,包括多种病毒(如:SARS病毒、禽流感病毒)、细菌、真菌及芽孢。下面是市售过氧乙酸商品标签:

有关资料:H2O2是极弱的电解质,在酸性介质中才能稳定存在,是一种强氧化剂。过氧乙酸消毒液是由H2O2、H2O、CH3COOH及少量H2SO4混合后,反应生成过氧乙酸(CH3COOOH)。CH3COOOH容易放出氧原子,它与空气中微生物机体作用,达到灭菌目的,是消毒液的主要成分。
(1)某研究性学习小组为了弄清配制过氧乙酸消毒液的甲、乙溶液的主要成分各是什么?进行以下科学探究,请你完成下列相关内容:
①提出假设:甲溶液的主要成分为_________,乙溶液的主要成分为_________。
②实验验证:取甲、乙两种溶液少许,分别加入几滴_________试液,若①中假设正确,则甲溶液的现象为_____________________,乙溶液的现象为__________。
(2)有关过氧乙酸的叙述正确的是_________ (填编号)
A.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
B.过氧乙酸与苯酚混合使用可增强消毒效果
C.过氧乙酸与乙酸属于同系物
D.氧元素的化合价为-2价
(3)实验室制备少量过氧乙酸,可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
①在三颈烧瓶中加入一定量冰醋酸与浓H2SO4的混合液体,再缓缓加入适量30%的双氧水。
②不断搅拌并控制B中混合液的温度为20~30℃至反应结束。
③接入冷凝管和抽气泵,在锥形瓶中收集得到产品。
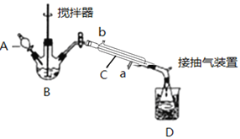
请回答下列问题:
①仪器C的名称是_______________;
②为更好地控制反应温度,应采用方法是_________________;
③生成过氧乙酸的化学方程式为________________________________________;
④碘量法取2.00mL过氧乙酸试样稀释成100mL,从中取出5.00mL,滴加酸性KMnO4溶液至恰好粉红色以除去残余H2O2,再加入10mL 10%KI溶液和几滴淀粉溶液,摇匀,反应完全后再用0.1000mol/L的Na2S2O3标准液滴定至终点(反应方程式为2Na2S2O3+I2=Na2S4O6+2NaI),共消耗14.30mL Na2S2O3标准液。该样品中过氧乙酸的物质的量浓度是_____mol/L。(结果保留小数点后两位)(提示:CH3COOOH+2I+2H+ =I2+CH3COOH +H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com