
科目: 来源: 题型:
【题目】(1)已知:N2(g)+O2(g)=2NO(g); △H=+180.5 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905 kJ·mol-1
2H2(g)十O2(g)=2HO(g):△H=--483.6 kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的△H=___________。
2NH3(g)的△H=___________。
(2)在一定条件下,将2mol N2与5mol H2混合于一个10 L的密闭容器中,反应情况如图1所示:
①求5min内的平均反应速率v(NH3)______________;
②达到平衡时NH3的体积分数为______________________。
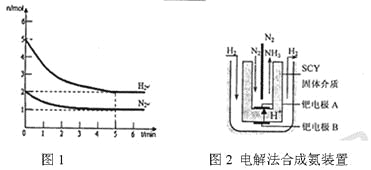
(3)近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图2)。钯电极A上发生的电极反应式是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知X、Y、Z、W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物(10e或18e)在常温下均为气态,在元素周期表中Z与W相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的外成层电子数相同。
(1)Z离子的结构示意图是_____________________________。
(2)X、Y、W可组成一种化合物,原子个数比为4:1:1,该化合物的化学式是_______,其中含有的化学键有__________________。
(3)X与Y所形成的分子的电子式为__________,它比同主族其他元素的氢化物沸点高的原因是__________________。
(4)请从Z、W的结构上说明Z、W两种元素非金属性的强弱_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下两种难溶性盐的沉淀溶解平衡曲线如图所示,图中X2-表示CO32-、SO42-,且MSO4不溶于酸,下列有关说法错误的是( )
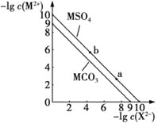
A.MSO4的饱和溶液中c(M2+)=1×10-5molL-1
B.MCO3(s)+SO42-(aq)![]() MSO4(s)+CO32-(aq)的平衡常数K为10
MSO4(s)+CO32-(aq)的平衡常数K为10
C.用盐酸和浓Na2CO3溶液有可能将MSO4转化为MCl2
D.向a点含MSO4的分散系中加入M(NO3)2固体后,体系有可能转化为b点的分散系
查看答案和解析>>
科目: 来源: 题型:
【题目】硫铁矿烧渣的主要成分为 Fe2O3、Fe3O4,以及少量 SiO2、Al2O3 等。由硫铁矿烧渣制备铁红(Fe2O3) 的一种工艺流程如下:

已知:还原焙烧时,大部分 Fe2O3、Fe3O4 转化为 FeO。 几种离子开始沉淀和完全沉淀时的 pH 如下表所示:

(1) “酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号)______________。
(2)Fe 粉除调 pH 外,另一作用是___________;Fe 粉调节溶液的 pH 范围为__________。
(3) 已知“沉铁、过滤”中生成沉淀为碳酸铁沉淀,则高温条件下,“氧化”步骤中发生反应的化学方程式为______________。
(4) Fe2O3 也是赤铁矿的主要成分,工业上若要得到 120t 纯度为 93%生铁需要含杂质 20%的(杂质不含铁 元素)赤铁矿的质量为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物是药物生产的中间体,其结构简式如图。下列有关叙述正确的是( )

A. 该有机物能与溴水发生加成反应
B. 该有机物与浓硫酸混合加热可发生消去反应
C. 1 mol 该有机物与足量NaOH溶液反应最多消耗3 mol NaOH
D. 该有机物经催化氧化后能发生银镜反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A.明矾能水解生成Al(OH)3胶体,可用作净水剂
B.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
C.水解反应NH4++H2O![]() NH3·H2O+H+达到平衡后,升高温度平衡逆向移动
NH3·H2O+H+达到平衡后,升高温度平衡逆向移动
D.盐类水解反应的逆反应是中和反应
查看答案和解析>>
科目: 来源: 题型:
【题目】金属铝在生产生活中有广泛用途。
(1)铝元素在元素周期表中位于______________。
(2)用化学方程式表示工业制备铝单质______________。 铝热反应可用于焊接钢轨,下图为铝热反应的实验装置图。
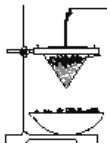
(3) 该铝热反应的化学方程式是______________。铝热反应的反应现象说明反应物的总能量___________生成物的总能量(填“<”、“>”或“=”)。
(4)铝热反应在工业上用于冶炼______________金属(填编号)。
A. 强还原性 B. 难熔性 C. 易导电 D. 活泼
(5)反应结束后,从沙中取出生成的固体物质,有同学推测该固体是铁铝合金,他设计了如下实验证明此 固体中含有金属铝:取少量固体于试管中,滴加______________,当观察到______________现象时,证明固体中含有金属铝。
查看答案和解析>>
科目: 来源: 题型:
【题目】以水为溶剂进行中和滴定的原理是:H3O++OH-=2H2O.已知液态SO2和纯水的导电性相近,因为液态SO2也会发生自离解:SO2(l)+SO2(l)![]() SO32-+SO2+.若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是 ( )
SO32-+SO2+.若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是 ( )
A. 该滴定反应可以表示为:SO32-+ SO2+=2SO2
B. 在一定温度下,液态SO2中c(SO32-)与c(SO2+)的乘积是一个常数
C. 自离解的存在,说明SO2是离子化合物
D. 可通过导电能力变化来判断是否到达滴定终点
查看答案和解析>>
科目: 来源: 题型:
【题目】已知298K时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子[-lgc(M2+)]与溶液pH的变化关系如a、b所示,已知:该温度下Kap[Cu(OH)2]<Kap[Fe(OH)2]下列说法中正确的是
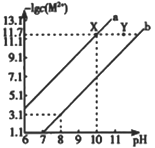
A. a线表示Fe(OH)2饱和溶液中的变化关系
B. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中c(Fe2+):c(Cu2+)=104.6:1
C. 除去CuSO4溶液中少量的Fe2+,可加入适量CuO
D. 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,用0.1molL-1Na2S溶液分别滴定10mL0.1molL-1CuCl2溶液以及10mL0.1molL-1ZnCl2溶液,溶液中-lgc(M2+)(M2+代表Zn2+或Cu2+)与Na2S溶液体积(V)的关系如图所示, b、c分别为滴定终点。下列有关说法错误的是[已知相同温度下:Ksp(CuS)<Ksp(ZnS)]( )
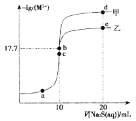
A.a点溶液中Cu2+、Zn2+的浓度相等
B.b、d两点中,水的电离程度d点大
C.曲线乙代表Na2S溶液滴定CuCl2溶液
D.可用ZnS固体除去ZnCl2溶液中的少量Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com