
科目: 来源: 题型:
【题目】25℃时,用0.1000mol·L-1的NaOH溶液分别滴定20.00mL均为0.1000mol·L-1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法错误的是( )
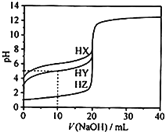
A.HZ是强酸,HX、HY是弱酸
B.根据滴定曲线,可得Ka(HY)≈10-5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D.向上述HY溶液中滴加任意NaOH溶液时,均存在c(H+)+c(Na+)=c(OH-)+c(Y-)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.1mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B.![]() 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-)
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是几种常见的化学电源示意图,有关说法不正确的是

A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池在长时间使用后,锌筒被破坏
C. 铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
D. 氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目: 来源: 题型:
【题目】1L某溶液中含有的离子如下表:
离子 |
|
|
|
|
物质的量浓度
| 1 | 1 |
| 1 |
用惰性电极电解该溶液,当电路中有![]() 通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是
通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是
A.电解后混合溶液的pH=0B.a=3
C.阳极生成![]() D.阴极析出的金属是铜与铝
D.阴极析出的金属是铜与铝
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.氢气的燃烧热为![]() ,则电解水的热化学方程式
,则电解水的热化学方程式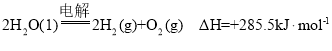
B.密闭容器中,![]() 硫粉与
硫粉与![]() 铁粉混合加热生成硫化亚铁
铁粉混合加热生成硫化亚铁![]() 时,放出
时,放出![]() 热量。
热量。![]()
C.500℃、![]() 下,将
下,将![]() 和
和![]() 置于密闭的容器中充分反应生成
置于密闭的容器中充分反应生成![]() ,放热
,放热![]() ,其热化学方程式
,其热化学方程式![]()
D.相同条件下,在两个相同的恒容密闭容器中,![]() 和
和![]() 反应放出的热量与
反应放出的热量与![]() 和
和![]() 反应放出的热量一样多
反应放出的热量一样多
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡: CH3COOH ![]() CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】H2S2O3是一种弱酸,实验室欲用0.01mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,下列说法合理的是( )
A.该滴定可用甲基橙作指示剂
B.Na2S2O3是该反应的还原剂
C.该滴定可选用如图所示装置
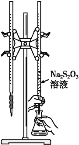
D.该反应中每生成1molNaI,电子转移数为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验过程如图所示,则图③试管中的现象是( )
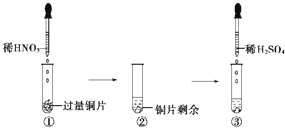
A.铜片溶解,产生无色气体,该气体遇空气变为红棕色
B.铜片溶解,产生无色气体,该气体遇到空气不变色
C.铜片溶解,放出红棕色有刺激性气味的气体
D.无明显现象,因稀硫酸不与铜反应
查看答案和解析>>
科目: 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的数值,下列说法正确的是( )
为阿伏加德罗常数的数值,下列说法正确的是( )
A.电解精炼铜时,若阳极质量减少![]() ,则转移到阴极的电子数不一定等于
,则转移到阴极的电子数不一定等于![]()
B.![]() 晶体中共含有
晶体中共含有![]() 个离子
个离子
C.![]() 的
的![]() 水溶液中含有的氧原子数为
水溶液中含有的氧原子数为![]()
D.常温下![]() 的
的![]() 溶液中,
溶液中,![]() 的浓度为
的浓度为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲酰氯(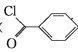 )是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
)是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
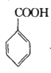 +COCl2
+COCl2![]()
![]() +CO2+HCl
+CO2+HCl
已知物质性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
苯甲酸 | 122.1 | 249 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
碳酰氯(COCl2) | -188 | 8.2 | 较易溶于苯、甲苯等。遇水迅速水解,生成氯化氢,与氨很快反应,主要生成尿素[CO(NH2)2]和氯化铵等无毒物质 |
苯甲酰氯 | -1 | 197 | 溶于乙醚、氯仿和苯。遇水或乙醇逐渐分解,生成苯甲酸或苯甲酸乙酯和氯化氢 |
三氯甲烷(CHCl3) | -63.5 | 63.1 | 不溶于水,溶于醇、苯。极易挥发,稳定性差,450℃以上发生热分解 |
I.制备碳酰氯
反应原理:2 CHCl3+O2![]() 2HCl+COCl2
2HCl+COCl2
甲. 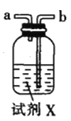 乙.
乙. 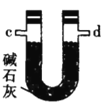 丙.
丙. 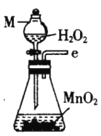 丁.
丁.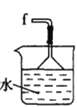 戊.
戊. 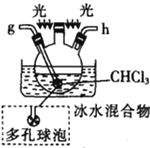
(1)仪器M的名称是____________
(2)按气流由左至右的顺序为___________→c→d→_________→_________→_________→_________→_________.
(3)试剂X是_______________(填名称)。
(4)装置乙中碱石灰的作用是____________。
(5)装置戊中冰水混合物的作用是____________;多孔球泡的作用是________________。
Ⅱ.制备苯甲酰氯(部分夹持装置省略)
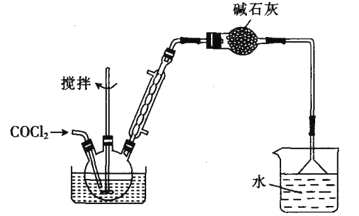
(6)碳酰氯也可以用浓氨水吸收,写出该反应的化学方程式:______________。
若向三颈烧瓶中加入610g苯甲酸,先加热至140~150℃,再通入COCl2,充分反应后,最后产品经减压蒸馏得到562g苯甲酰氯,则苯甲酸的转化率为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com