
科目: 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种肉制品生产中常见的食品添加剂,使用时必须严格控制其用量。在漂白、电镀等方面应用也很广泛。某兴趣小组设计了如下图所示的装置制备NaNO2(A中加热装置已略去)。
已知:室温下,①2NO+Na2O2===2NaNO2
②酸性条件下,NO 或NO2-都能与MnO4-反应生成NO3-和Mn2+
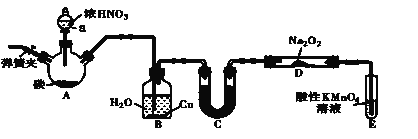
(1)A中发生反应的化学方程式为_________________________________。
(2)检查完该装置的气密性,装入药品后,实验开始前通入一段时间N2,然后关闭弹簧夹,再滴加浓硝酸,加热。通入N 2的作用是______________。
(3)装置B中观察到的主要现象为_________________
(4)①为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是___________(填字母序号)。
A.P2O5 B.无水CaCl2 C.碱石灰 D.浓硫酸
②如果取消C装置,D中固体产物除NaNO2外,可能含有的副产物有________ 写化学式)。
(5)E中发生反应的离子方程式为____________。
(6)将1.56g Na2O2完全转化为NaNO2,理论上至少需要木炭__________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】a、b、c、d、e是元素周期表中前四周期的元素,其原子序数依次增大,a为元素周期表中原子半径最小的元素,b的基态原子中占有电子的3个能级上的电子总数均相等,d与b同族,c与b同周期,且c的所有p轨道上的电子总数与所有s轨道上的电子总数相等,e的次外层电子数是其最外层电子的7倍。回答下列问题:
(1)c、d形成的化合物的晶体类型为___________;
(2)b、a c形成的三原子分子中,c原子的杂化方式为___________;
(3)b、c、d三种元素的电负性由小到大的顺序为___________;(用元素符号表示),d元素基态原子价层电子排布式为_________;
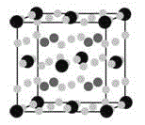
(4)金属Mg与a、e形成的化合物是目前人类已发现的体积储氢密度最高的储氢材料之一,其晶胞结构如图所示,其中黑球代表e,深灰色小球代表Mg,浅灰色小球代表a,其中浅灰色小球除在棱上、面上以外,在晶胞内部还有6个。试写出该化合物的化学式:__________________。
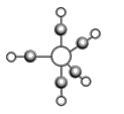
(5)b、c、e能形成如图所示三角双锥构型的配合物分子,三种元素的原子分别用大白球、小白球和灰色小球代表。该配合物形成配位键时提供空轨道的原子是___________(填元素符号),该配合物中大白球代表的元素的化合价为___________。
(6)①在水溶液中,水以多种微粒的形式与其他化合物形成水合物。试画出如下微粒的结构图式。H5O2+______________________
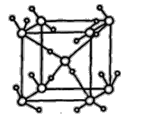
②如图为冰的一种骨架形式,依此为单位向空间延伸该冰中的每个水分子有___________个氢键;如果不考虑晶体和键的类型,哪一物质的空间连接方式与这种冰的连接类似_______
查看答案和解析>>
科目: 来源: 题型:
【题目】当今环境问题越来越受到人们的重视。汽车尾气中含有较多的NO和CO,两种气体均会使人体中毒。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题。请回答下列问题
(1)用还原法将NO转化为无污染的物质。已知:
2C(s)+O2(g)![]() 2CO △H1=-221.0KJ/mol
2CO △H1=-221.0KJ/mol
N2(g)+O2(g)![]() 2NO △H2=+180.5KJ/mol
2NO △H2=+180.5KJ/mol
2NO+C(s)![]() CO2(g)+N2(g) △H3=-573.75KJ/mol
CO2(g)+N2(g) △H3=-573.75KJ/mol
请写出CO与NO生成无污染气体CO2与N2的热化学方程式_______________________。
(2)在一定温度下,向甲、乙、丙三个恒容密闭容器中加入一定量的NO和足量的焦炭,反应过程中测得各容器中c(NO)(mol/L)随时间(s)的变化如下表。
已知:三个容器的反应温度分别为T甲= 500℃、T乙= 500℃、T丙= a℃
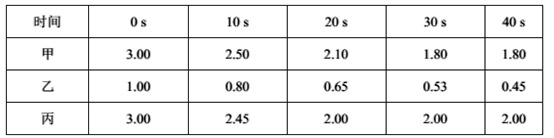
甲容器中,该反应的平衡常数K=_______。丙容器的反应温度a _______500℃(填“”、“<”或“=”),理由是_______________________________。
(3)某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。
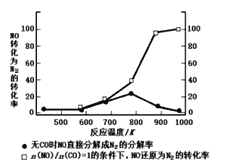
①若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为_________。
②在n(NO)/n(CO)=1的条件下,为更好的除去NO物质,应控制的最佳温度在_____K左右。
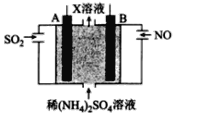
(4)利用电解原理也可以处理NO。下图为工业生产模拟装置。其中A、B为多孔电极(外接电源未画出),则B为___________极(填“正”“负”“阴”或“阳”,),A电极反应式为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20mL、浓度均为0.1mol·L-1的氢氧化钠溶液、氨水中分别滴加0.1mol·L-1盐酸,溶液导电性如图所示(已知:溶液导电性与离子浓度相关)。下列说法正确的是

A.a点溶液pH=11
B.曲线1中c与e之间某点溶液呈中性
C.c点溶液中:c(H+)=c(OH-)+c(N3H·H2O)
D.在a、b、c、d、e中,水电离程度最大的点是d
查看答案和解析>>
科目: 来源: 题型:
【题目】锂—铜空气燃料电池(如图)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是
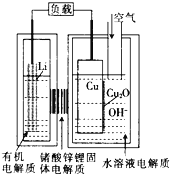
A.放电时,当电路中通过0.2mol电子的电量时,有0.2mol Li+透过固体电解质向Cu极移动,有标准状况下1.12L氧气参与反应
B.通空气时,铜被腐蚀,表面产生Cu2O
C.放电时,正极的电极反应式为:Cu2O+H2O+2e-=2Cu+2OH-
D.整个反应过程,空气中的O2起了催化剂的作用
查看答案和解析>>
科目: 来源: 题型:
【题目】设阿伏加德罗常数的数值为NA,下列说法正确的是
A.1L 1 mol·L-1 的NaHCO3溶液中含有的离子数为3NA
B.22.4 L的CO2与过量Na2O2充分反应转移的电子数为NA
C.常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA
D.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】在10mL pH=4的盐酸中加水,稀释到100mL时,溶液pH为______;若加水稀释到1000mL时,溶液pH为________;若加水稀释到10000L时,溶液pH________
查看答案和解析>>
科目: 来源: 题型:
【题目】呋喃酚是生产呋喃丹、好安威等农药的主要中间体,是高附加值的精细化工产品。一种以邻氯苯酚(A)为主要原料合成呋喃酚(F)的流程如下:

回答下列问题:
(1)A物质核磁共振氢谱共有______个峰,④的反应类型是_______,C和D中含有的相同官能团的名称是________。
(2)下列试剂中,能和D反应的有__________(填标号)。
A.溴水 B.酸性K2Cr2O7溶液 C.FeCl2溶液 D.纯碱溶液
(3)写出反应①的化学方程式是__________(有机物用结构简式表示,下同)。
(4)有机物B可由异丁烷经三步反应合成:
![]()
条件a为________, Y 生成 B 的化学方程式为 _______。
(5)呋喃酚的同分异构体很多,写出符合下列条件的所有同分异构体的结构简式____ 。
①苯环上的一氯代物只有一种 ②能发生银镜反应的芳香酯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com