
科目: 来源: 题型:
【题目】氮氧化物(NOx)造成酸雨、光化学烟雾、臭氧层破坏等危害,不仅破坏自然生态环境,而且严重危害人类健康。采用合适的还原剂能够实现烟气的高效脱硝。
(1)活性炭还原脱硝可防止氮氧化物污染,已知:
①N2(g)+O2(g)═2NO(g) △H1=+180.5kJmol-1
②2C(s)+O2(g)═2CO(g) △H2=-221.0kJmol-1
③2CO(g)+O2(g)═2CO2(g) △H3=-556.0kJmol-1
则反应C(s)+2NO(g)![]() N2(g)+CO2(g)△H=__kJmol-1
N2(g)+CO2(g)△H=__kJmol-1
(2)用活性炭对NO进行还原,采用相同质量不同粒径的同种催化剂M和N,测量相同时间内烟气的脱氮率,结果如图所示。
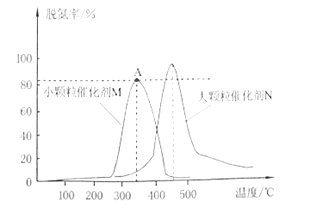
①在M、N两种不同粒径催化剂作用下,出现M和N两条不同的脱氮率与温度的变化曲线的原因是___。
②判断M曲线上最高点A点对应的脱氮率__(填“是“或“不是”)该温度下的平衡脱氮率。
③25℃下,用NaOH溶液作捕提剂吸收产生的CO2,不仅可以降低碳排放,而且可得到重要的化工产品。某次捕捉后得到pH=12的溶液,已知:25℃下Ka2(H2CO3)=5.6×10-11,试通过计算溶液中c(CO32-):c(HCO3-)=__。
(3)在一恒容密闭容器中,使用某种催化剂对反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)△H<0进行相关实验探究。改变投料比(n0(SO2):n0(NO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定SO2的平衡转化率[α(SO2)]。已知:KR=16,KZ=1,部分实验结果如图所示。
SO3(g)+NO(g)△H<0进行相关实验探究。改变投料比(n0(SO2):n0(NO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定SO2的平衡转化率[α(SO2)]。已知:KR=16,KZ=1,部分实验结果如图所示。

①如果要将图中R点的平衡状态改变为X点的平衡状态,应采取的措施是__。
②图中R、X、Y、Z四点对应的实验温度分别为TR、TX、TY,TZ通过计算选择下列选项中两个温度相等是__(填标号)。
A.TR和TY B.TR和TZ C.TX和TZ D.TY和TZ
查看答案和解析>>
科目: 来源: 题型:
【题目】含硫化合物在生活和生产中有着重要应用,科学使用含硫化合物对人体健康及环境保护意义重大。
(1)葡萄酒中添加微量的SO2可抑制细菌生长,防止葡萄酒被__(填“氧化”、“还原”)。
(2)氢的硫化物有多种:H2Sx(x=1,2,3,…),如H2S2,其结构与H2O2相似。请写出H2S3的结构式__。
(3)固体硫酸氢钾在加热熔化时,生成了焦硫酸钾(K2S2O7),反应中断裂的化学键类型为__。
(4)淮北某课题小组对连二亚硫酸钠(Na2S2O4)进行了如下探究。将0.050ml·L-1Na2S2O4溶液在空气中放置,其溶液的pH与时间(t)的关系如图所示(忽略溶液体积的变化)。
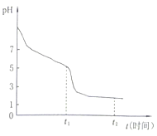
①Na2S2O4溶液显__性,原因是__(用离子方程式表示)。
②t1时溶液中只有一种溶质,此时含硫元素的粒子浓度由大到小的顺序为___。
0-t1段发生反应的离子方程式为__,t1-t2段溶液的pH变小的原因是__(用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,部分含铁元素的微粒在溶液中的物质的量分数与溶液pH的关系如图所示。下列说法错误的是( )

A.pH=4时,溶液中存在下列关系c(HFeO4-)>c(H2FeO4)>c(FeO42-)
B.H2FeO4的第一步电离平衡常数Ka1=4.15×10-4
C.B点溶液加NaOH溶液到pH为4的过程中,![]() 减小
减小
D.B、C两点对应溶液中水的电离程度:B<C
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:I2+2S2O32-=S4O62-+2I-;CuI是不溶于水的白色沉淀。
相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入_________,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是(用文字叙述):____________________________________________。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是______________________________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用_______________作滴定指示剂,滴定终点的现象是________________________。
②CuCl2溶液与KI反应的离子方程式为___________________________________________。
③该试样中CuCl2·2H2O的质量百分数为__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学探究铁离子与硫离子的反应,实验操作及现象如表:下列有关说法错误的( )
| 滴入FeCl3溶液立刻有黑色沉淀生成继续滴入FeC13溶液,黑色沉淀增多后又逐渐转化为黄色沉淀 |
| 滴入Na2S溶液立刻生成黑色沉淀,沉淀下沉逐渐转化为黄色。继续滴入Na2S溶液,最后出现黑色的沉淀 |
A.两次实验中,开始产生的黑色沉淀都为Fe2S3
B.两次实验中,产生的黄色沉淀是因为发生了反应Fe2S3+4FeCl3═6FeCl2+3S
C.向稀FeCl3溶液中逐滴加入稀Na2S溶液至过量最后生成的黑色沉淀为FeS
D.在Na2S溶液过量的情况下,黑色沉淀中存在较多的Fe(OH)3
查看答案和解析>>
科目: 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NO,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)NaClO2中Cl元素的价态为_______。
(2)在鼓泡反应器中通入含有含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol·L1 。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①在NaClO2溶液脱硝的主要反应中,参加反应的n(ClO2-):n(NO)=_________,增加压强,NO的转化率______(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐_______(填“升高”“不变”或“降低”)。
③由实验结果可知,脱硫反应速率______脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
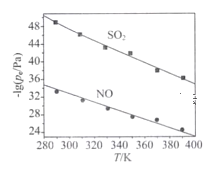
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pc如下图所示:
 =
=
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均____(填“增大”“不变”或“减小”)。
②反应ClO2+2SO32===2SO42+Cl的平衡常数K表达式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】高能固氮反应条件苛刻,计算机模拟该历程如图所示,在放电的条件下,微量的O2或N2裂解成游离的O或N原子,分别与N2和O2发生以下连续反应生成NO。下列说法错误的( )
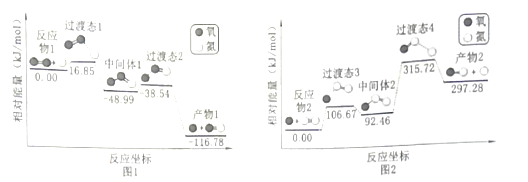
A.图1中,中间体1到产物1的方程式为O-O═N→O+N═O
B.NO的生成速率很慢是因为图2中间体2到过渡态4的能垒较大
C.由O和N2制NO的活化能为315.72kJmol-1
D.由N和O2制NO的过程比由O原子和N2制NO的过程速率慢
查看答案和解析>>
科目: 来源: 题型:
【题目】图所示装置中,甲、乙、丙三个烧杯依次分别盛放NaOH溶液、足量的CuSO4溶液和足量的 K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加6.4g。以下说法不正确的是:
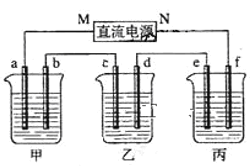
A.电源的N端为正极
B.电极b上发生的电极反应为4OH--4e-=2H2O+O2↑
C.b电极上生成气体1.12L,e电极上生成气体0.2 g
D.如果电解过程中铜全部析出,此时电解继续进行
查看答案和解析>>
科目: 来源: 题型:
【题目】镍-铁碱性电池十分耐用,但其充电过程中正负极得到的产物对电解水有很好的催化作用,因此电池过充时会产生氢气和氧气,限制了其应用。科学家将电池和电解水结合在起,制成新型的集成式电池电解器,可将富余的能量转化为氢能储存。已知镍铁碱性电池总反应方程式为:Fe+2NiOOH+2H2O![]() Fe(OH)2+2Ni(OH)2。下列有关说法错误的是( )
Fe(OH)2+2Ni(OH)2。下列有关说法错误的是( )
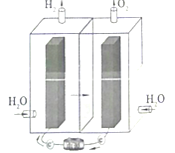
A.电能、氢能属于二次能源
B.该储能装置中的交换膜为阴离子交换膜
C.该装置储氢能发生的反应为:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D.镍-铁碱性电池放电时正极的反应为:Ni(OH)2+OH--e-═NiOOH+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3DZn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3DZn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。下列说法错误的是
ZnO(s)+2Ni(OH)2(s)。下列说法错误的是
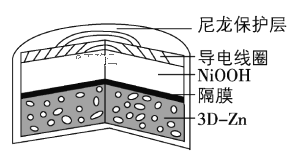
A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B.放电过程中OH通过隔膜从负极区移向正极区
C.充电时阴极反应为ZnO(s)+H2O(l) +2e= Zn(s)+2OH(aq)
D.放电时正极反应为NiOOH(s)+H2O(l) +e =Ni(OH)2(s)+OH(aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com